
题目列表(包括答案和解析)
8.(2010年宁波质检)用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是
( )
|
选项 |
操作及现象 |
溶液 |
|
A |
通入CO2,溶液变浑浊。继续通CO2至过量,浑浊不消失 |
Na[Al(OH)4] 溶液 |
|
B |
通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失 |
Na2SiO3溶液 |
|
C |
通入CO2,溶液变浑浊。再加入品红溶液,红色褪去 |
Ca(ClO)2溶液 |
|
D |
通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。再加入足量NaOH溶液,又变浑浊 |
Ca(OH)2溶液 |
[解析] A项,2[Al(OH)4]-+CO2(少量)===2Al(OH)3↓+CO+H2O,继续通CO2,Al(OH)3不溶解,但生成HCO。B项,CO2+Na2SiO3+H2O===Na2CO3+H2SiO3↓,H2SiO3与CO2不反应,浑浊不会消失。C项,CO2+Ca(ClO)2+H2O===CaCO3↓+2HClO,所以溶液变浑浊,加入品红被HClO氧化褪色。D项,首先,CO2+Ca(OH)2===CaCO3↓+H2O,继续通CO2,产生可溶于水的Ca(HCO3)2,再加入足量的NaOH,则2NaOH+Ca(HCO3)2===CaCO3↓+Na2CO3+2H2O,溶液又变浑浊。
[答案] B
7.下列说法正确的是
( )
A.二氧化硅溶于水显酸性
B.光导纤维传导光的能力非常强,利用光缆通讯,能同时传送大量信息
C.因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强
D.二氧化硅可作半导体材料
[解析] 二氧化硅难溶于水,二氧化硅用于制作光导纤维而不是半导体材料,高温时,二氧化硅与碳酸钠反应放出CO2,不能说明硅酸的酸性比碳酸强,常温时,硅酸钠溶液和CO2反应生成硅酸,说明碳酸的酸性比硅酸强。
[答案] B
6.下列试剂可用带玻璃塞的玻璃瓶存放的是
( )
A.NaOH溶液 B.Na2SiO3溶液
C.盐酸 D.氢氟酸
[解析] 由于SiO2+2OH-===SiO+H2O,因而不可用带玻璃塞的试剂瓶保存NaOH溶液;氢氟酸可以与SiO2反应,即SiO2+4HF===SiF4↑+2H2O,故不可用玻璃瓶保存。
[答案] C
5.常温下,下列不发生反应的一组物质是
( )
①硅与NaOH溶液 ②硅与盐酸 ③硅与氢氟酸 ④二氧化硅与碳酸钠 ⑤二氧化硅与NaOH溶液 ⑥二氧化硅与浓硝酸
A.①②④ B.③④⑥
C.②⑤⑥ D.②④⑥
[解析] 硅的化学性质稳定,常温下除了与氟气、氢氟酸和强碱反应外,它不易与其他物质如氢气、氧气、氯气等反应。
[答案] D
4.下列说法中,不正确的是
( )
A.SiO2和CO2都是酸性氧化物,均可与NaOH溶液反应
B.SiO2不能与任何酸发生反应
C.SiO2和CO2在一定条件下,均可与CaO发生反应
D.SiO2不溶于水,而CO2可与水反应,生成H2CO3
[解析] SiO2是一种酸性氧化物,但是可与HF溶液发生反应,生成SiF4和H2O。
[答案] B
3.下列表述正确的是
( )
①人造刚玉的熔点很高,可用做高级耐火材料,主要成分是二氧化硅 ②化学家采用玛瑙研钵摩擦固体反应物进行无熔剂合成,玛瑙的主要成分是硅酸盐 ③提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料 ④夏天到了,游客佩戴添加了氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛 ⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能
A.①②③ B.②④
C.③④⑤ D.③⑤
[解析] 人造刚玉的主要成分是氧化铝;玛瑙是含有有色杂质的石英晶体,主要成分是二氧化硅;有色玻璃是在制造玻璃的过程中加入某些金属氧化物(加入Co2O3后呈蓝色,加入Cu2O后呈红色),但不是变色玻璃,变色玻璃是含有AgBr的玻璃(AgBr具有感光性);水泥、玻璃、陶瓷都是硅酸盐材料。
[答案] D
2.下列关于碳和硅的叙述中,不正确的是
( )
A.+4价氧化物都与氢氧化钠溶液反应
B.单质在加热时都能与氧气反应
C.氧化物都能溶于水生成相应的酸
D.碳和硅两种元素都有能导电的单质
[解析] SiO2不溶于水,不与H2O反应。
[答案] C
1.下列说法正确的是
( )
A.硅材料广泛应用于光纤通讯
B.工艺师利用盐酸刻蚀石英制作艺术品
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品
D.粗硅制备单晶硅不涉及氧化还原反应
[解析] 光纤的主要成分为SiO2;B项,工艺师利用HF刻蚀石英制作艺术品;C项,水晶项链的主要成分是SiO2,餐桌上的瓷盘是硅酸盐制品;D项,粗硅制备单晶硅先利用氧化反应即用Cl2氧化粗硅为SiCl4,再利用还原反应即用H2还原SiCl4。
[答案] A
17.(2009年海南高考)有关物质存在如下图所示的转化关系(部分产物已省略)。
通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。
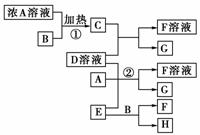
请回答下列问题:
(1)反应①的化学方程式为__________________________________________________。
(2)反应②的离子方程式为________________________________________________。
(3)写出另外一种实验室制取H的化学方程式______________________
(4)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。将等体积的D溶液与Pb(NO3)2溶液混合,若D的浓度为1×10-2 mol/L,则生成沉淀所需Pb(NO3)2溶液的最小浓度为________。
[答案] (1)MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
(2)6I-+ClO+6H+===3I2+Cl-+3H2O
(3)2H2O22H2O+O2↑或2KMnO4K2MnO4+MnO2+O2↑
(4)5.6×10-4 mol·L-1
16.(2009年天津高考) 海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:
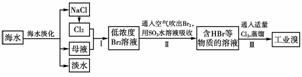
(1)请列举海水淡化的两种方法:__________、__________。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、________、________或H2、________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为____________________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为________________________________________________________________________,
由此反应可知,除环境保护外,在工业生产中应解决的主要问题是________________ ________________________________________________________。
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图:
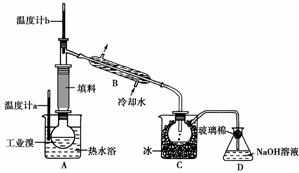
请你参与分析讨论:
①图中仪器B的名称:________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因为___________________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:________________________________________________________________________。
④C中液体产物颜色为____________,为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是____________。
[解析] (2)电解NaCl溶液:2NaCl+2H2OH2↑+Cl2↑+2NaOH,由以上反应生成的Cl2和NaOH进一步反应:Cl2+2NaOH===NaCl+NaClO+H2O,也可得到H2和NaClO。
(3)步骤Ⅰ中获得低浓度Br2溶液,再经过步骤Ⅱ、Ⅲ可富集溴元素。
(4)SO2与Br2发生氧化还原反应:SO2+Br2+2H2O===H2SO4+2HBr,产物是两种强酸,故在工业生产中要注意强酸对设备的严重腐蚀。
(5)由已知信息Br2的强腐蚀性可得出Br2腐蚀橡胶,故装置中不能用橡胶塞和橡胶管。再由Br2的沸点为59 ℃可知用该套装置提纯溴关键要控制温度计b的温度,收集59 ℃时的馏分。C中收集到的是深红棕色的液溴,要除去该产物中残留的少量Cl2,可向其中加入NaBr充分反应后,利用Br2易溶于CCl4的性质进行分液来分离,或利用Br2易挥发的特点用蒸馏法分离。
[答案] (1)蒸馏法、电渗析法、离子交换法及其他合理答案中的任意两种 (2)Cl2 NaOH NaClO (3)富集溴元素
(4)Br2+SO2+2H2O===4H++SO+2Br- 强酸对设备的严重腐蚀 (5)①冷凝管 ②Br2腐蚀橡胶 ③控制温度计b的温度,并收集59 ℃时的馏分 ④深红棕色 分液(或蒸馏)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com