
题目列表(包括答案和解析)
5.等质量的下列物质分别与等浓度的NaOH溶液反应至完全溶解,耗碱量最多的是
A.Al B.Al(OH)3 C.AlCl3 D.Al2O3
4.下列除去杂质的方法正确的是 ( )
A.除去CO2中混有的CO:用澄清石灰水洗气
B.除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤
C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤
D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤
3. 将等物质的量的镁和铝均匀混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是 ( )
将等物质的量的镁和铝均匀混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是 ( )
A.3 mol·L-1 HCl溶液 B.4 mol·L-1 HNO3溶液
C.5 mol·L-1 NaOH溶液 D.18.4 mol·L-1 H2SO4溶液
2.用铜来制备等质量的Cu(NO3)2,下列方法中最合理的方案是 ( )
A.Cu 与浓HNO3反应 B.Cu 与稀HNO3反应
C.CuO与稀HNO3反应 D.Cu(OH)2与稀HNO3反应
1.下列叙述正确的是 ( )
A.氯水通入SO2后溶液的酸性减弱
B.向明矾溶液中加入过量NaOH溶液会产生大量白色沉淀
C.Na、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的碱
D.浓硫酸、浓硝酸在加热条件下能将木炭氧化为二氧化碳k
14.A、B、C、D、E五种物质中均含有同一种元素,它们能发生如下图所示的变化。且该元素的单质(用R表示)能与强碱溶液反应生成盐(Na2RO3)和氢气。
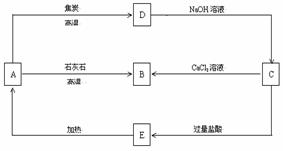
(1) 写出这五种物质的化学式:A 、B 、C 、D 、E 。
(2) 写出下列反应的化学方程式:
A ® D:
A ® B:
13.A、B为两种单质,常温下均为固体。在元素周期表中,A、B两种元素同周期且原子半径A>B。分别取三份完全相同的质量均为1.520g的A、B混合物粉末进行如下实验。
①向第一份试样中加入过量的盐酸,充分反应后放出0.896L气体(标准状况,下同),还余下0.560g残渣。
②向第二份试样中加入过量的10%的NaOH溶液,充分反应后放出0.896L气体,还余下0.960g残渣。
③将第三份试样隔绝空气加强热后,生成一种固体。冷却后,在隔绝空气的条件下加入足量稀盐酸,该固体全部溶解,产生xL气体。
(1)单质A是___________。
(2)混合物中B的质量分数为_______________。
(3)写出实验③中有关反应的化学方程式,并计算x的值。
12.关于氮化硅陶瓷的性能,下列说法不正确的是 ( )
A. 是一种超硬物质,本身具有润滑性且耐磨损
B. 抗腐蚀能力强,不与任何酸反应
C. 耐高温,不易传热
D. 高温时也能抗氧化,且能抗冷热冲击
D.奥赛一瞥
11.下列化合物中,氧化钙的质量分数为48.3%的是 ( )
A. 3CaO·SiO2 B. CaO·SiO2 C. 2CaO·SiO2 D. 3CaO·Al2O3
10.下列叙述中,错误的是 ( )
A. 硅在地壳中的含量仅次于氧,居第二位
B. 硅是构成矿物和岩石的主要元素
C. 硅和锗相似,是良好的半导体材料
D. 硅的化学性质不活泼,常温下与氧气、酸、碱都不反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com