
题目列表(包括答案和解析)
8.把浓硫酸滴入浓盐酸中,会有氯化氢气体逸出,对此现象的合理解释是( )
A.氯化氢难溶于水
B. 浓硫酸有脱水性
C. 浓硫酸是一种高沸点的酸
D.浓硫酸溶于水放出大量的热,降低了氯化氢的溶解度
7.把碘滴入硫化钠溶液中,溶液变混浊,将溴水滴入碘化钾溶液中,溶液呈黄褐色,由
此得出的正确结论是( )
A.离子的氧化性:S2-<I-<Br-
B. 离子的还原性:Br-<I-<S2-
C. 元素的非金属性:Br>S>I
D.单质的氧化性: Br2>I2>S
6.关于硒的叙述正确的是( )
A.作半导体材料,熔点很高
B. 硫化导体材料,熔点很高
C. H2SeO3有酸性,又有氧化性和还原性
D.硒与铁反应生成Fe2Se3
5.在某无色透明的溶液中下列各组离子能大量共存的是( )
A.K+,H+,I-,NO3- B.Mg2+,Cu2+,Cl-,SO2-4
C.K+,Na+,Br-,MnO4- D.K+,OH-,S2-,NO3-
4.能正确表示下列反应的离子方程式是( )
A. 铁跟盐酸反应:2Fe+6H+ 2Fe3++3H2↑
铁跟盐酸反应:2Fe+6H+ 2Fe3++3H2↑
B.
 磷酸二氢钙溶液与氢氧化钙溶液反应:H2PO4-+2OH-
PO43-+2H2O
磷酸二氢钙溶液与氢氧化钙溶液反应:H2PO4-+2OH-
PO43-+2H2O
C.
 碳酸钙与醋酸反应:CaCO3+2CH3COOH Ca2++2CH3COO-+H2O+CO2↑
碳酸钙与醋酸反应:CaCO3+2CH3COOH Ca2++2CH3COO-+H2O+CO2↑
D. 铜与稀硝酸反应:Cu+NO3-+4H+
Cu2++NO↑+2H2O
铜与稀硝酸反应:Cu+NO3-+4H+
Cu2++NO↑+2H2O
3. 下列各组溶液,不用其他试剂就可以将它们区别开的是( )
下列各组溶液,不用其他试剂就可以将它们区别开的是( )
A.KOH,K2CO3,MgSO4,KHSO4 B.NaNO3,HCl,NH4Cl,KOH
C.BaCl2,CaCl2,Na2SO4,KNO3 D.HCl,KOH,K2SO4,K2CO3
2.能区别NaBr,KI,NaCl,Na2Cl,Na2CO3和Na2SO4五种固体的试剂是(可加热)( )
A.AgNO3溶液 B.溴水 C.BaCl2溶液 D.浓硫酸
1.下列物的南的名称、化学式、主要用途都正确的是( )
A.石膏(CaSO4·2H2O)用于制造各种模型
B. 皓矾(ZnSO4)用于医药、木材防腐剂、媒染剂
C. 硫酸钡(BaSO4)作白色颜料、“钡餐”
D.胆矾(CuSO4)用于制造农药
9.离子共存问题如何考虑?
[例题解析]
[例1]把硫与强碱加热至沸,反应后硫转化为S2-和SO32-,则反应的S和生成的S2-、SO32-的物质的量之比为:( )
A.2:1:1 B.3:2:1 C.3:1:2 D.4:1:3
[解法一] 根据反应的化学方程式分析:
[解法二]根据氧化还原反应中,得失电子总数应相等关系进行分析:
解题思路: 。
易错点: 。
[例2]m克铁粉与n克硫粉放入试管中混合加热,反应完全后将混合物与过量的稀盐酸作用,问在标准状况下,能制得气体多少升?
解题思路: 。
易错点: 。
[考题再现]
例1. 将含有0.5NA个H2S分子的H2S与50.4升(标况)空气混合,在一定条件下,恰好完全反应。求生成物中含硫元素的物质的量是多少?(设空气中O2体积占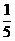 )
)
思维方法: 。
展望高考:
例2. 将过量铁片投入含有硫酸的硫酸铜溶液中,充分反应后,把铁片取出
洗净,干燥称量,结果与原铁片质量相同。求原溶液中硫酸铜和硫酸物质
的量之比。
思维方法: 。
展望高考:
[针对训练]
A.基础训练
8.判断离子反应方程式主要从哪几方面进行考虑?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com