
题目列表(包括答案和解析)
4.将0.2 mol某烷烃完全燃烧后,生成的气体缓慢通过盛有0.5 L 2 mol·L-1的NaOH溶液中,生成的Na2CO3和NaHCO3的物质的量之比为1∶3。则该烷烃为( )
A.甲烷 B.乙烷 C.丙烷 D.丁烷
解析:因生成物中Na2CO3、NaHCO3共存,故烷烃完全燃烧产生的CO2与NaOH完全反应。
n(NaOH)=2 mol·L-1×0.5 L=1 mol
n(Na2CO3)=×1 mol=0.2 mol
n(NaHCO3)=×1 mol=0.6 mol
总碳量(即CO2的物质的量)为:0.2 mol+0.6 mol=0.8 mol
1 mol烷烃中含C的物质的量为×1 mol=4 mol因此该烃为丁烷。
答案:D
3. 有关烷烃性质的叙述中,正确的是( )
A.烷烃能与氯气、溴蒸气在光照和适当的温度下发生取代反应
B.烷烃中除甲烷外,很多都能使酸性高锰酸钾溶液的紫色退去
C.标准状况下,以任意比例混合的甲烷和丙烷的混合物22.4 L,所含有的分子数为
NA(NA 表示阿伏加德罗常数的值)
D.标准状况下,1 L辛烷完全燃烧后,所生成气态产物的分子数为NA
解析:烷烃的化学性质与CH4相似,能发生燃烧、取代反应,均不能使KMnO4(H+)溶液退色,故A对,B错。辛烷在标准状况下为液体,1 mol辛烷不是22.4 L,标准状况下22.4 L任何气体的物质的量均为1 mol,即6.02×1023个分子,故C对,D错。
答案:AC
2. 将标准状况下的11.2 L甲烷和22.4 L氧气混合后点燃,恢复到原状况时,气体的体积为( )
A.11.2 L B.22.4 L C.33.6 L D.44.8 L
解析:甲烷燃烧的化学方程式为:CH4+2O2CO2+2H2O,因此,当温度超过100℃时(即水为气态),反应前后气体的体积不变,而在标准状况下水是液态,此时11.2 L甲烷与22.4 L氧气恰好反应,最后只剩下CO2,其体积为11.2 L。
答案:A
1.下列关于同系物的说法中,错误的是( )
A.同系物具有相同的最简式
B.同系物都符合同一通式
C.同系物中,相邻的同系物彼此在组成上相差一个CH2原子团
D.同系物的化学性质基本相似,物理性质随着碳原子数的增加而呈规律性变化
解析:同系物不一定具有相同的最简式,如甲烷、乙烷、丙烷是烷烃的同系物,但它们的最简式分别为CH4、CH3、C3H8;结构相似,分子组成上相差一个或若干个“CH2”原子团的化合物互称为同系物,同系物具有同一通式,并且其物理性质随碳原子数增加而呈规律性变化。
答案:A
10.某气态烃在标准状况下密度为2.59 g/L,其相对分子质量等于________,该烃的含碳量为82.8%,则分子中碳、氢原子的个数比是________,分子式是________可能的结构简式是________。
解析:M=2.59×22.4=58。C∶H=∶=2∶5,则烃的最简式为C2H5。设其分子式为(C2H5)x,则有(12×2+5)·x=58,x=2,所以烃的分子式为C4H10,可能的结构简式为
CH3CH2CH2CH3、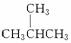 。
。
答案:58 2∶5 C4H10 CH3CH2CH2CH3、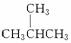
9. 下列物质中,互为同系物的有________,互为同分异构体的有________,互为同素异形体的有________,属于同位素的有________,是同一种物质的有________。
①液氯 ②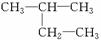 ③白磷 ④氯气 ⑤2,2二甲基丁烷 ⑥氯水
③白磷 ④氯气 ⑤2,2二甲基丁烷 ⑥氯水
⑦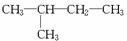 ⑧
⑧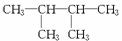 ⑨Cl ⑩红磷 ⑪Cl
⑨Cl ⑩红磷 ⑪Cl
⑫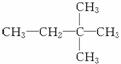
解析:先将比较容易判断的找出;①④为同一种物质,⑨⑪为同位素,③⑩为同素异形体;然后在有机物中先找同一种物质:②⑦及⑤⑫具有相同的碳原子数,且结构相同,为同一种物质;再找同分异构体:⑤⑧⑫具有相同的碳原子数,而⑤⑫是同一种物质,因此⑤⑧互为同分异构体,⑧⑫互为同分异构体;最后确定同系物:②(或⑦)与⑤(或⑫),②(或⑦)与⑧互为同系物;⑥为混合物。
答案:②(或⑦)与⑤(或⑫),②(或⑦)与⑧⑤(或⑫)与⑧ ③⑩ ⑨⑪ ①和④,②和⑦,⑤和⑫
8. 化学上常用燃烧法确定有机物的组成。这种方法是在电炉加热时用纯氧氧化管内样品,根据产物质量确定有机物的组成,装置如下图所示,是用燃烧法确定有机物化学式常用的装置。
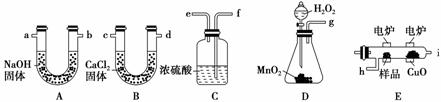
回答下列问题:
(1)产生的氧气按从左到右流向,所选择装置各导管的连接顺序是____________。
(2)C装置中浓H2SO4的作用为____________。
(3)D装置中MnO2的作用为____________。
(4)E中CuO的作用为______________。
(5)若准确称取0.90 g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,A管质量增加1.32 g,B管质量增加0.54 g,则该有机物最简式为______________。
解析:实验原理是测定一定质量的有机物完全燃烧时生成CO2和H2O的质量,来确定是否含氧及C、H、O的个数比,求出最简式。因此生成O2后必须除杂(主要是除H2O)。然后与样品完全反应……。(5)m(CO2)=1.32 g⇒n(CO2)=0.03 mol⇒m(C)=0.36 g;m(H2O)=0.54 g⇒n(H2O)=0.03 mol⇒m(H)=0.06 g⇒m(O)=0.48 g⇒n(O)=0.03 mol。则n(C)∶n(H)∶n(O)=1∶2∶1,有机物的最简式为CH2O。
答案:(1)g f e h i c d(d、c) a b(b,a) (2)吸收水分、干燥氧气 (3)催化剂、加快产生O2的速率 (4)使有机物更充分氧化为CO2、H2O (5)CH2O
7.含有2-5个碳原子的直链烷烃沸点和燃烧热的数据见下表:
|
烷烃名称 |
乙烷 |
丙烷 |
丁烷 |
戊烷 |
|
沸点/℃ |
-88.6 |
-42.1 |
-0.5 |
36.1 |
|
*燃烧热/kJ·mol-1 |
1 560.7 |
2 219.2 |
2 877.6 |
3 535.6 |
*燃烧热:1 mol物质完全燃烧,生成二氧化碳、液态水时所放出的热量。
根据表中数据,下列判断错误的是( )
A.正庚烷在常温常压下肯定不是气体
B.烷烃燃烧热和其所含碳原子数成线性关系
C.随碳原子数增加,烷烃沸点逐渐升高
D.随碳原子数增加,烷烃沸点和燃烧热都成比例增加
解析:随碳原子数增加,烷烃沸点升高,正戊烷在常温常压下已不是气体,A对;随碳原子数增加,烷烃燃烧热逐渐增大,成线性关系,B对;随碳原子数增加,烷烃沸点和燃烧热都升高或增大,但并不成比例,C对,D错。
答案:D
6.某烷烃分子量为72,跟氯气反应生成的一氯代物只有一种,它是( )
A.CH3-CH3 B.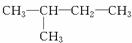
C.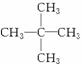 D.
D.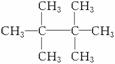
解析:由题目所给的条件可知,烷烃的分子量为72,可根据烷烃的通式CnH2n+2求出该烷烃分子中的碳原子个数:12n+2n+2=72,14n=70,解得n=5,含5个碳原子的烷烃的一氯取代物只有一种,说明烃分子中12个氢原子的位置均是等效的,分子结构对称,只有C符合,故正确答案为C。
答案:C
5. (2009·海南单科)下列化合物的核磁共振氢谱中出现三组峰的是( )
A.2,2,3,3四甲基丁烷 B.2,3,4三甲基戊烷
C.3,4二甲基己烷 D.2,5二甲基己烷
解析:本小题实际应为等效氢的判断问题。等效氢应为以下三种情况:①同一碳原子上的氢原子等效;②同一碳原子的甲基上的氢原子等效;③关于镜面对称碳原子上的氢原子等效。根据以上原则,可判断出A:1种;B:4种;C:4种;D:3种。
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com