
题目列表(包括答案和解析)
3.用 NA 表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.1.0L l mol·L-1氨水中 NH3·H2O 的分子数为 NA
B.标准状况下, 11.2 L 氯仿中含有的C-Cl 键的数目为 1.5NA
C.0.6 g CaCO3 与 KHCO3 的混合物中所含质子数为 0.3NA
D.工业上铜的电解精炼,电解池中每转移 1 mol 电子时阳极上溶解的铜原子数为 0.5NA
2. A、B、C、D四种短周期元素,其核电荷数依次增大,已知元素A和D可形成两种常温下均为液体的化合物,B原子最外层电子数是最内层电子数的两倍。则下列由四种元素形成的化合物的化学式不正确的是 ( )
A.B2A6CD2 B.B2A5D2C C.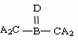 D.
D.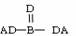
1.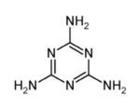 1食品安全专项整治紧急会议安排从2010年2月1日开始为期10天的乳品和乳制品专项整治三聚氰胺魅影重现 国内紧急启动乳业大清查。三聚氰胺简称三胺,也被人们称为“蛋白精”,其结构简式如下,下列说法正确的是 ( )
1食品安全专项整治紧急会议安排从2010年2月1日开始为期10天的乳品和乳制品专项整治三聚氰胺魅影重现 国内紧急启动乳业大清查。三聚氰胺简称三胺,也被人们称为“蛋白精”,其结构简式如下,下列说法正确的是 ( )
A.三聚氰胺从中学常见物质分类上看,即属于有机物,也属于碱类,
所以能与盐酸反应
B.1mol三聚氰胺可以与3mol氢气发生加成反应
C.三聚氰胺所有原子有可能共平面
D.三聚氰胺的分子式为C3N6H6,含氮量较高,奶粉中可以适当添加
12.(15分)某校学生小组为探究乙酸、碳酸和苯酚的酸性强弱并证明乙酸为弱酸,进行下述实验。
Ⅰ.探究乙酸、碳酸和苯酚的酸性强弱关系,该校学生设计了如下实验装置(夹持仪器已略去)。
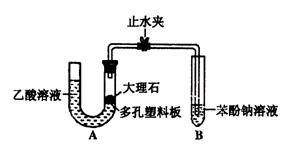
(1)实验前如何检查装置A的气密性?
;大理石与乙酸溶液反应的化学方程式为 。
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为
,反应的离子方程式为 。
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是
,改进该装置的方法是 。
Ⅱ.证明乙酸为弱酸。
(4)现有pH=3的乙酸溶液、蒸馏水、石蕊试液及pH试纸,用最简便的实验方法证明乙酸为弱酸: 。
11.(14分)已知一个碳原子上连有两个羟基时,易发生下列转化:
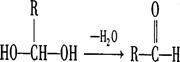
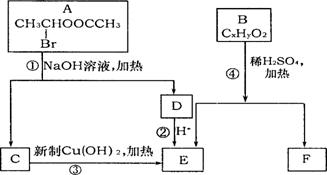
请根据右图回答:
(1)E中含有的官能团的名称是 ;
反应③的化学方程式为: _________
(2)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1,则B的分子式为 。
(3)F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 _____________________________。
(4)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有多种结构,写出其中两种环上取代基个数不同的同分异构体的结构简式_______________________
10.(16分)某些物质的转化关系如下图所示。其中甲可由两种单质直接化合得到;乙为金属单质,常温下,它在G的浓溶液中不溶解;F的溶液中只含一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)。
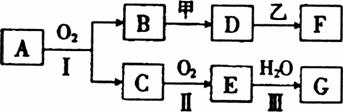
(1)若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近时,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性。
① 写出B和甲反应的化学方程式 。
② 1.7 g A与O2反应生成气态的B和C时放出22.67 kJ热量,写出该反应的热化学方程式 。
③D与乙反应的离子方程式是 。
(2)若B为红棕色固体,C能使品红试液褪色,D的水溶液中加人HNO3酸化的AgNO3溶液有白色沉淀生成,向F中加入过量的NaOH溶液,有沉淀产生。
① 工业上反应II在 中进行。
② D和乙反应的化学方程式是 。
③ B、D、F中含同一种元素,该元素在周期表中的位置是: 。
④写出由B为原料,得到该元素单质的化学方程式: _______。
9.(12分) X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是________________________。
(2)ZW2的电子式是______________,它在常温下呈液态,形成晶体时,属于_________晶体。
(3)工业生产单质Y的原理是_____________________________(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是___________________。
(5)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是_________________。
8.下列有关热化学方程式的叙述正确的是 ( )
A.已知C(石墨,s) C(金刚石,s);△H>0,则金刚石比石墨稳定
C(金刚石,s);△H>0,则金刚石比石墨稳定
B.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(ag)+HCl(aq) NaCl(aq)+H2O(l);△H=-57.4 kJ· mol-1
NaCl(aq)+H2O(l);△H=-57.4 kJ· mol-1
C.已知2H2(g)+O2(g) 2H2O(g);△H=-483.6 kJ· mol-1,则氢气的燃烧热为241.8kJ
2H2O(g);△H=-483.6 kJ· mol-1,则氢气的燃烧热为241.8kJ
D.己知2C(s)+2O2(g)=2CO2(g);△H1 2C(s)+O2(g)=2CO(g);△H2,则△H1>△H2
7.下列各溶液中,微粒的物质的量浓度关系正确的是 ( )
A.10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:c(Cl-)>c(Na+)>c(OH-) >c(H+)
B.0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
D.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:
c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl)
6.下列各组离子,在指定环境中一定能大量共存的是 ( )
A.pH=7的溶液中:Al3+、K+、SO42-、HCO3-
B.加入铝粉能放出氢气的溶液中:CO32-、AlO2-、I-、NO3―
C.能使pH试纸变深蓝色的溶液中:S2-、SO32-、S2O32-、SO42-
D.由水电离出的[OH-]=10-13mol/L的溶液中:Fe3+、NH4+、ClO-、Cl-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com