
题目列表(包括答案和解析)
4.用惰性电极实现电解,下列说法正确的是 ( )
A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变
B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小
C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为
D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为
答案:4.D
3.用惰性电极电解下列溶液,电解一段时间后,阴极质量增加,电解质溶液的pH下降的是 ( )

答案: 3.B 由题可知:阴极金属离子放电,阳极OH-放电
2.1LO.1mol/LagNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是(设电解按理论进行,溶液不蒸发) ( )
A.溶液的浓度变为0.08mol/L
B.阳极上产生112MlO2(标准状况)
C.转移的电子数是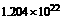 个
个
D.反应中有0.0l mol的Ag被氧化
答案:

转移的电子数为:
电解后溶液中溶质为AgNO3,浓度不变(A错),
1.在一定温度下,用铂电极电解饱和Na2S04溶液,对电解质溶液判断正确的是 ( )
A.不会有晶体析出 B.浓度变大
C.浓度变小 D.pH不变
答案:1.D 电解饱和NaSO4溶液,实质是电解水,c(Na2SO4)不改变,pH也不变,且有晶体析出
26.(6分)为了预防碘缺乏病,国家规定每千克食盐中应含40mg-50mg的碘酸钾。为检验某种食盐是否为加碘的合格食盐,某同学取食盐样品428g,设法溶解出其中全部的碘酸钾,将溶液酸化并加入足量的碘化钾淀粉溶液,溶液呈蓝色,再用o.03m01/L的硫代硫酸钠溶液滴定,用去18.oomL时蓝色刚好褪去。试通过计算说明该加碘食盐是否合格。
有关反应如下:


答案:26.利用关系式计算。合格。
25.(4分)含FeS280%的硫铁矿燃烧时损失硫5%,用SO2氧化成SO2时利用率为99%,问生产l t98%的硫酸需这种硫铁矿多少吨?
答案:25.解:设需80%的FeS2为xt

x=0.797t
24.(12分)有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验。通人SO2气体,将带余烬的木条插入试管C中,木条复燃。
请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了Na2O2与SO2,该反应的化学方程式是:
(2)请设计一种实验方案证明Na2o2与SO2反应生成的白色固体中含有Na2SO3
。
(3)第2小组同学认为Na2O2与SO2反应生成了Na2SO4与O2外,还有Na2SO4生成。为检验是否有Na2S04生成,他们设计了如下方案:

上述方案是否合理? 。
请简要说明理由:
① ;② 。
答案:24(1)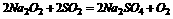
(2)取白色固体,加稀硫酸,产生能使晶红溶液褪色的气体
(3)不合理;稀硝酸能将亚硫酸钡氧化为硫酸钡;如果反应后的固体中还残留Na2O2,它溶于水后能将亚硫酸根氧化成硫酸根。
23.(10分)如下图:实验室为验证某铜银合金完全溶解于一定量浓硝酸,生成NO2气体中含有NO的实验装置。常温下NO2与N2O4混合存在,在低于0℃时几乎只有无色N2O4晶体存在。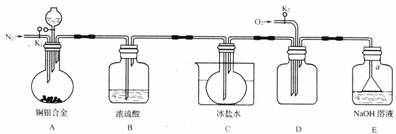
(1)反应前先打开A部分的活塞 ,并持续通一段时间的 ,其理由是 .
(2)若装置中缺B部分,其后果是 。
(3)E部分中a仪器所起的作用是 。
(4)如何证明含有NO: 。
 答案: 23.(1)排除装置中的空气,以防干扰验证实验 (2)未能吸收H2O、H2O与 NO2反应生成NO,干扰实验 (3)防止液体倒吸 (4)实验结束后,打开K2后通入O2,如变红棕色有NO生成,反之则没有
答案: 23.(1)排除装置中的空气,以防干扰验证实验 (2)未能吸收H2O、H2O与 NO2反应生成NO,干扰实验 (3)防止液体倒吸 (4)实验结束后,打开K2后通入O2,如变红棕色有NO生成,反之则没有
22.(12分)将a、b、c、d四全铂电极,插入甲、乙两电解池中进行电解,如下图所示。工作一段时间后,甲池中电解液的pH升高,乙池中的电解液pH下降,同时凸\c两极放电的离子数之比为2:1,可供选择的电解液有四组(见下表)。
|
项目 |
A |
B |
C |
D |
|
甲 |
AgNO3 |
NaCl |
K2S |
KOH |
|
乙 |
CuCl2 |
CuSO4 |
H2SO47 |
AgNO3 |
 (1)符合上述情况的电解池溶液是
组。
(1)符合上述情况的电解池溶液是
组。
(2)甲池中得到的电解产物是 。乙池中电解总的化学反应方程式是 。
(3)工作一段时间,a、b、c、d四极生成物的物质的量之比为 。
(4)若甲、乙两池中的电解溶液各为500 mL,通电后,a极生成产物0.01 g时,甲池的pH约为 ,乙池的pH约为 .
答案: (3)2:2:2:1
(3)2:2:2:1
(4)12;1
提示:电解时放电顺序 用电解过程中各电极通过的电子数目相等来计算。
用电解过程中各电极通过的电子数目相等来计算。
21.(6分)1986年,化学上第一次用非电解法制得氟气。
(1)试配平用该方法制氟的化学方程式:

(2)氰(CN2)、硫氰(SCN)2的化学性质与卤素单质(X2)相似,如: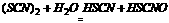 ,它们的阴离子还原性强弱为
,它们的阴离子还原性强弱为 。
。
写出(CN)2和KOH溶液反应的化学方程式 。
写出在NaBr和KSCN的混合液中加入(CN2)反应的离子方程式 。
答案:21.(1)2、4、4、2、1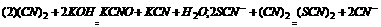
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com