
题目列表(包括答案和解析)
1.用稀H2SO4溶液和金属铝为原料制取Al(OH)3,甲、乙、丙三个学生的途径分别是:
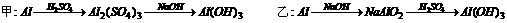

若要得到等量的Al(OH)3,则 ( )
A.三者消耗原料相同 B.甲消耗原料最多 C.乙消耗原料最多 D.丙消耗原料最少
答案:1.BD 以制1molAl(OH)3为例,甲用3NaOH、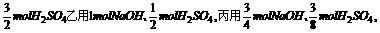 所以甲用的最多,丙用的最少
所以甲用的最多,丙用的最少
3.掌握各类无机物、有机物之间的相互联系及内在规律,各类物质相互反应的客观规律,在生产、实验上有很重要的意义,可以指导无机物、有机物的制备。
潜能开发
[例1] 下列三个问题均与右图中实验装置有关,请选择 A-D序号填入空格中。
[例2]
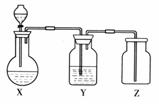
(1)制取某五色非金属氧化物气体时,烧瓶X内的药品应是 ( )
(2)洗气瓶Y中所装液体应是(不允许非水杂质混在气体中)(
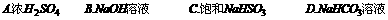
(3)检验集气瓶口是否集满气体,置于瓶口的滤纸应沾上的溶液是 ( )
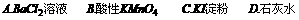
思路分析
(1) 铜与稀HNO3反应需加热,且得到的五色NO气体易被空气中O2氧化为红棕色NO2 。铜与浓HNO3反应直接生成NO3,均不符合题意。CaOC3与稀H2SO4反应生成CaCO4覆盖在CaCO3表面,反应逐渐停止,不能制得CO2。Na2SO4与浓盐酸常温下反应生成无色气体,符合题意。
(2)从X中出来的SO2中将混有较多的HCl和少量的水蒸气,应选用饱和NaHSO3除掉HCl,而SO2反应,能实现除去气体中非水杂质的目的。
(3)SO2与BaCl2、KI不反应;SO2与石灰水反应生成CaSO4沉淀,在滤纸上不易观察,也不能作为检测手段;SO2遇强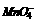 可被氧化,可使酸性 KMnO4溶液褪色,现象明显,易于观察,符合题意。
可被氧化,可使酸性 KMnO4溶液褪色,现象明显,易于观察,符合题意。
[答案](1)D(2)C(3)B
[例2]试用空气、焦炭、水为原料制备硝酸。
思路分析
从HXO3的组成看包含三种元素H、N、O,欲提供N元素,首先应从空气中分离出N2,而N2转为化合态,已学过的途径有N2与O2反应, 反应,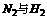 反应,前者反应条件不合适,应选后者,H2的产生可用电解法、水煤气法。前者反应慢,选后者。
反应,前者反应条件不合适,应选后者,H2的产生可用电解法、水煤气法。前者反应慢,选后者。
[答案]①从空气中分离出N2

思维诊断
除掉气体的杂质,所选择的试剂应具备以下条件:与主要气体不反应、不吸收,可去掉气体杂质且不引入新的气体杂质。
用试纸检验时应注意试纸本身的颜色。
思维诊断
一般不用电解水法制 H2。制备途径尽可能在已学知识中查寻,然后考虑量、反应条件、安全、可操作性等因素,择优选用。
知能达标训练
2.熟练掌握常见单质、化合物的制备方法
1.熟练掌握常见气体的制备方法,在气体实验室制备方案设计时应遵循以下原则:
(1)实验室制备各种气体应以实验室常用药品为原料,以方便、经济、安全为原则,而且在几种简单易解的方法中又要选择那些能制取并收集较纯气体的方法。
(2)选择实验仪器要根据反应原理及制取气体量的多少来决定,必须是干净的,有时还需是干燥的仪器。
(3)选择试剂要注意浓度,特别是盐酸、硫酸、硝酸的浓度对制取气体及纯度都有很大的影响。
(4)熟悉装置图,根据仪器装配顺序(由低到高,由左到右,先里后外)、装置顺序(制气装置 净化装置
净化装置 干燥装置
干燥装置 收集装置
收集装置 尾气吸收装置)准确组装仪器并掌握检查气密性的方法。
尾气吸收装置)准确组装仪器并掌握检查气密性的方法。
5.由给定废料,回收、提取或制备某一物质。
制备实验方案设计,主要涉及原料、基本化学反应原理、实验程序和仪器、设备。核心是原料,由原料可确定反应原理,推导出实验步骤及所用仪器。
学法建议
制备实验方案设计可考查各个层次的多种能力,特别是创新能力。从发展趋势看,今后高考对考生设计简单实验能力的考查将予以较多的关注和尝试,但考虑到高考的时限性,加之理科综合考试的形式,这种题的难度将不会太大,建议本节复习应掌握以下几点:
4.用含杂质的物质为原料,提纯某一纯净物。
3.自选原料,制备某一指定物质。
2.限定几种原料,要求用几种不同的方法制备一种物质。
1.限定几种原料,制备一种或几种物质。
2.希尔将分离出的叶绿体加入到草酸高铁钾盐溶液中,经过光照以后放出氧气,同时草酸高铁被还原成草酸低铁,这一反应被称为“希尔反应”。
(1)写出希尔反应的化学方程式: 并指出希尔实验中每生成l molO2,电子转移数约为 个。
(2)希尔反应是 反应。
A.水解反应 B.光反应 C.氧化还原反应 D.以上都不是
(3)通过该反应证明了光合作用中氧气来源于 。
答案:2.该题是一道化学与生物渗透的综合题。重点考查了氧化还原反应原理、电子转移的计算以及光合作用、光反应等概念的理解。因此考生务必重视加强理、化、生各学科的重要概念的理解,达到掌握应用的能力要求
(1)根据题中信息可知: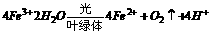 每生成1molO2应转移4mol电子即4×6.02×1023=2.408×1024个。
每生成1molO2应转移4mol电子即4×6.02×1023=2.408×1024个。
(2)该反应很明显发生了价态变化,属于氧化还原反应。水解反应无化合价变化,同时,从生物学知识角度看,该反应应为暗反应而非常光反应,所以答案选C
(3)从反应知氧气中的氧只能来源于反应物H2O中。所以答案应为:水分子的分解
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com