
题目列表(包括答案和解析)
1.性质实验方案设计的题目所涉及的物质、化学反应最好是学生熟悉的,实验装置也不要太复杂,这样可以避免思维容量的扩大,使学生的思维焦点集中在操作步骤的设计上,但需注意整体操作过程的有序性、逻辑性、严密性、安全性和可操作性,同时要注意文字的表达。
4.最后得出结论。
中学阶段的性质实验主要指已知物质的化学性质实验,这些物质的性质尽管已被人们所掌握,但它们中的部分性质对中学生却是陌生的。对这样的一些物质进行性质探索或验证可进一步拓宽学生的知识面,培养学生的钻研求实精神和动手能力。它的意义远远超过纯粹的实验目标。
性质实验的目的是验证和比较元素的金属性、非金属性;氧化性、还原性;化合物的稳定性、酸碱性;指定离子和一些有机官能团的特征反应。
学法建议
3.选择适宜的试剂、装置(仪器)、反应条件实施方案。
2.设计具体实验方案来(探索)验证物质所具有的性质。
1.根据物质的组成、结构特征,结合已有知识及实验经验,预测可能具有的性质,例如通过分析乙醇分子结构特征可推测其性质有:
2.验证实验方案设计:对物质具备的性质求证,关键是设计出简捷、安全、现象明显的实验。
1.探索性实验方案设计:分析物质结构特点及从属类型的典型代表物去推测物质可能具有的性质,由此设计出合理的实验方案,去探索可能具有的性质。
2.工业上为了处理含有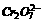 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)沉淀生成,工业废水中铬的含量已低于排放标准。请回答下列问题:
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)沉淀生成,工业废水中铬的含量已低于排放标准。请回答下列问题:
(1)两极发生反应的电极反应式
(2)写出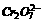 变为
变为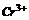 的离子方程式:
的离子方程式:
(3)212业废水由酸性变为碱性的原因是:
(4) (填“能”或“不能”)改用石墨电极,原因是.
答案:

1.100g无水氢氧化钾溶于100g水中,在T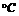 下电解该溶液,电流I=20A,电解时间为5 h。电解结束温度恢复至T℃,分离析出
下电解该溶液,电流I=20A,电解时间为5 h。电解结束温度恢复至T℃,分离析出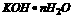 固体后,测得剩余溶液的总质量为150g,若T℃时无水氢氧化钾的溶解度为150g,求析出氢氧化钾晶体的化学式。(法拉第常量F=
固体后,测得剩余溶液的总质量为150g,若T℃时无水氢氧化钾的溶解度为150g,求析出氢氧化钾晶体的化学式。(法拉第常量F= )
)
答案:1.电解了的水m
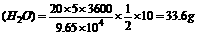

14.关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:观点一:“理论派”认为电解氯化铜溶液后溶液的pH升高。
观点二:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时pH的变化如右图曲线关系。
请回答下列问题:
(1)电解前氯化铜溶液的pH处于A点位置的原因是: 。(用离子方程式说明)
(2)“理论派”所持观点的理论依据是: 。
(3)“实验派”的实验结论是 ,他们所述“精确实验”是通过 确定的。
(4)你持何种观点?你所持观点的理由是(从化学原理加以简述) 。
答案:14.(1)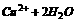 ⇌
⇌ (2)CuCl2溶液中存在上述平衡,电解时,Cu2+得电子被还原,致使水解平衡向左移动,c(H+)下降,pH升高 (3)pH降低,测定溶液的Ph(4)同意“实验派”的观点,由于2Cl--2e------------
(2)CuCl2溶液中存在上述平衡,电解时,Cu2+得电子被还原,致使水解平衡向左移动,c(H+)下降,pH升高 (3)pH降低,测定溶液的Ph(4)同意“实验派”的观点,由于2Cl--2e------------
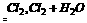 ⇌ CHl+HclO.生成HCl、HclO,故pH下降
⇌ CHl+HclO.生成HCl、HclO,故pH下降
综合能力训练
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com