
题目列表(包括答案和解析)
2.F2和Bt2的沸点 ( )
A.前者高 B.后者高 C.相等 D.无法确定
答案: 2.B组成和结构相似的物质,随着相对分子质量增大,熔、沸点升高
1.固体熔化时必须破坏非极性共价键的是 ( )
A.冰 B.晶体硅 C.溴 D.二氧化碳
答案: 1.B A选项熔化破坏的是分子间作用力,B选项破坏的是Si--Si非极性键,C、D选项破坏的是分子间作用力
4.氢键作为一种特殊的分子间作用力,要理解其成因和对物质特殊物理性质的影响作用。研究性学习学科内综合:
在学习晶体结构时,只有熟悉常见晶体的构型,才能进行有关计算。如求NaCl晶体密度:截取一个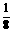 大的小立方体,因各顶点上
大的小立方体,因各顶点上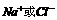 被8个小立方体共用,故小立方体
被8个小立方体共用,故小立方体
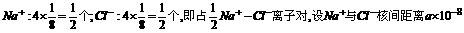 cm ,
cm ,
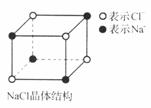 则立方体体积
则立方体体积
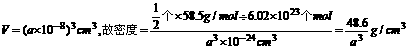 .
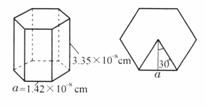
. 从教材上我们看到石墨晶体,能否也根据空间构型求出其密度?假设从石墨晶体图中截取上、下两个六元环,使其构成1个六棱柱,因每个C由6个六棱柱共用,则此六棱柱中含有
从教材上我们看到石墨晶体,能否也根据空间构型求出其密度?假设从石墨晶体图中截取上、下两个六元环,使其构成1个六棱柱,因每个C由6个六棱柱共用,则此六棱柱中含有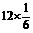 =2个C,从右图知
=2个C,从右图知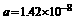 cm,柱高
cm,柱高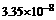 cm,柱底面面积
cm,柱底面面积
 。同样,CsCl、干冰的密度计算,有待于去进一步探究。
。同样,CsCl、干冰的密度计算,有待于去进一步探究。
 能力测试(时间:90分钟,总分:100分)
能力测试(时间:90分钟,总分:100分)
显能测试
3.强化对晶体结构图观察、分析和推测能力的培养。
(1)通过对晶体中粒子相对位置、晶胞中粒子数量的推算,发展空间想像能力。
(2)利用晶胞的粒子数量和构型,对粒子半径、键能、化学式等方面的延伸。
2.掌握晶体的类型、性质和判断方法
(1)通过四类晶体晶格粒子种类、粒子结构、半径、相互作用等,理解离子晶体、分子晶体、原子晶体、金属晶体的涵义,并能利用这些知识,比较、解释晶体的一些物理性质。
(2)能运用导电性、机械性能、熔、沸点等不同方法的比较和类推,判断晶体的类型。
1.本章考点
(1)晶体类型的判断,晶体类型与化学键之间的关系;(2)构成晶体的粒子与粒子间作用力之间的关系;(3)晶体类型与物理性质(熔、沸点,硬度)的关系;(4)有关晶体的熔、沸点比较;(5)晶体的空间结构及信息迁移式试题;(6)根据粒子空间排列推断化学式。
2.(1)A.Ca B.Cl C.N

(4)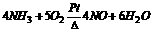
第1单元小 结
热点聚焦
2.有A、B、C三种元素。已知①4gA元素的单质与水作用,标况下放出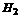 2.24 L,反应中有
2.24 L,反应中有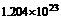 个电子发生转移。②B元素可与A形成
个电子发生转移。②B元素可与A形成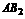 型的离子化合物,且知A、B的离子具有相同的核外电子排布。③元素C的气态氢化物可与其最高氧化物的水化物发生非氧化还原反应生成盐,1 mol该盐含42个电子。据此填写下列空白:
型的离子化合物,且知A、B的离子具有相同的核外电子排布。③元素C的气态氢化物可与其最高氧化物的水化物发生非氧化还原反应生成盐,1 mol该盐含42个电子。据此填写下列空白:
(1)元素符号:A ,B ,C 。
(2)A元素的离子结构示意图 。
(3)用电子式表示AB2的形成过程 。
(4)C的气态氢化物在催化剂作用下与02反应的化学方程式 。
(5)用电子式表示C的气态氢化物的形成过程 ;它与B的气态氢化物反应时有 现象发生,生成物的电子式 ,它属于 晶体。
答案:
1.某些金属晶体(Cu、Ag、Au)的原子按面心立方的形式紧密堆积,即在晶体结构中可以划出一块正立方体的结构单元,金属原子处于正立方体的8个顶点和6个侧面上,试计算这类金属晶体中原子的空间利用率。
答案:1.依题意画出侧面图,设正立方体边长为a,则体积为a3。原子半径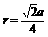 ,每个正立体包知金属原子
,每个正立体包知金属原子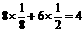 个,球体积共
个,球体积共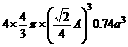 ,空间利用率为
,空间利用率为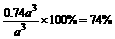
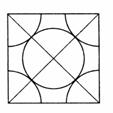
10.有下列八种晶体:A.水晶(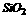 ) B.冰醋酸 C.氧化镁 D.白磷 D.晶体氩 F.氯化铵 G.铝 H.金刚石
) B.冰醋酸 C.氧化镁 D.白磷 D.晶体氩 F.氯化铵 G.铝 H.金刚石
用序号回答下列问题:
(1)属于原子晶体的化合物是 ,直接由原子构成的晶体是 ,直接由原子构成的分子晶体是 。
(2)由极性分子构成的晶体是 ,含有共价键的离子晶体是 。直接由原子构成的分子晶体是 。
(3)在一定条件下能导电而不发生化学变化的是 ,受热熔化后化学键不发生变化的是 。需克服共价键的是 。
答案:10.(1)A;AEH;E (2)B;F;DE·(3)G;BDE;AH 判断晶体类型的主要依据是:一看构成晶体的粒子 (分子、原子、离子);二看粒子间的相互作用
综合能力训练
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com