
题目列表(包括答案和解析)
5.离子方程式CO+2H+===CO2↑+H2O表示
( )
A.碳酸盐与盐酸之间的反应
B.一切碳酸盐与一切酸之间的反应
C.可溶性碳酸盐与酸之间的反应
D.可溶性碳酸盐与强酸之间的反应
解析:CO只代表可溶性的碳酸盐,而H+只代表强酸而不是一切酸,如CH3COOH等弱酸应用分子式表示.
答案:D
4.下列离子方程式正确的是
( )
A.氯气通入冷水中:Cl2+H2O Cl-+ClO-+2H+
Cl-+ClO-+2H+
B.氨气通入醋酸溶液中:
CH3COOH+NH3===CH3COONH4
C.碳酸氢钙溶液中加入过量的氢氧化钠溶液:
HCO+OH-===CO+H2O
D.澄清石灰水与盐酸反应:H++OH-===H2O
解析:A选项错.Cl2与H2O反应生成物为HCl和HClO,其中HClO属弱酸,应写成分子;B选项错,在溶液中,生成物CH3COONH4属强电解质,应写成离子形式;C选项错,Ca(HCO3)2与过量的NaOH反应,Ca2+与HCO应全部参加反应,生成物有沉淀CaCO3,该选项违背事实,D选项符合题意.
答案:D
3.下列物质的导电性能最差的是
( )
A.熔化的NaOH B.1 mol/L H2SO4
C.0.1 mol/L醋酸 D.KCl固体
解析:前三项物质均能导电,而KCl固体中无自由移动的离子,不能导电.
答案:D
2.下列各组在溶液中的反应,不管反应物的量是多少,都能用同一离子方程式表示的是
( )
A.FeBr2与Cl2
B.Ba(OH)2与H2SO4
C.HCl与Na2CO3
D.NaHCO3与Ca(OH)2
解析:B项,只发生反应Ba2++2OH-+2H++SO===BaSO4↓+2H2O;A项,Cl2少量时先氧化Fe2+,足量时Cl2将Br-、Fe2+都氧化;C项,H+少量时生成HCO,H+足量时生成CO2和H2O;D项NaHCO3少量时:HCO+Ca2++OH-===CaCO3↓+H2O,NaHCO3足量时:2HCO+Ca2++2OH-===2H2O+CaCO3↓+CO.
答案:B
1.下列物质的水溶液能导电,但属于非电解质的是
( )
A.CH3CH2COOH B.Cl2
C.NH4HCO3 D.SO2
解析:A、C为电解质,B既不是电解质,也不是非电解质.
答案:D
13.化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.(已知:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O)
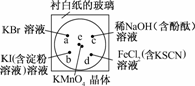
(1)e处反应的离子方程式为______________,该反应中发生反应的氧化剂和还原剂的物质的量之比为________.
(2)b处的实验现象为__________________,d处的实验现象为__________________.
(3)c处反应的化学方程式为____________________,标准状况下,当有0.224 L Cl2被NaOH溶液吸收后,转移电子的物质的量为________ mol.
(4)通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?________(填“能”或“不能”),若能,其氧化性由强到弱的顺序是________.
解析:(1)根据e处发生反应的化学方程式判断反应中的氧化剂为KMnO4,还原剂为HCl,其中氧化剂和还原剂的物质的量之比为2∶10=1∶5,而不是1∶8.
(2)b处发生的反应为2KI+Cl2===2KCl+I2,I2遇淀粉显蓝色;d处发生的反应为2FeCl2+Cl2===2FeCl3,Fe3+和SCN-反应使溶液变红色.
(3)Cl2与NaOH溶液反应的化学方程式:
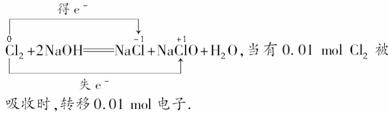
(4)e处实验说明氧化性KMnO4>Cl2,d处实验说明氧化性Cl2>FeCl3,因此,三种物质氧化性强弱顺序为KMnO4>Cl2>FeCl3.
答案:(1)2MnO+16H++10Cl-===2Mn2++5Cl2↑+8H2O 1∶5
(2)溶液由无色变为蓝色 溶液由无色变为红色
(3)Cl2+2NaOH===NaCl+NaClO+H2O 0.01
(4)能 KMnO4>Cl2>FeCl3
0.100 mol/L×0.100 L×=0.0150 mol.
V(Cl2)=0.0150 mol×22.4 L/mol=0.336 L.
答案:(1)①2 ②0.64 (2)0.336
0.2x mol×(4-)=0.4 mol,x=2
n(MnO)×5=0.4 mol
n(MnO)=0.08 mol
由电荷守恒可知:n(H+)×1-0.08 mol×1-0.2 mol×2=0.08 mol×2,故n(H+)=0.64 mol.
(2)FeBr2电离出的Fe2+和Br-都能被Cl2氧化,其反应方程式为2FeBr2+3Cl2===2FeCl3+2Br2,根据此化学方程式可知,2 mol FeBr2与3 mol Cl2完全反应,故至少需要Cl2
12.(2009·广东茂名调研)(1)已知下列变化过程中,0.2 mol RxO参加反应时,共转移0.4 mol电子.
RxO+MnO+H+―→RO2+Mn2++H2O
①x值为________.
②参加反应的H+的物质的量为________mol.
(2)在100 mL 0.100 mol/L的FeBr2溶液中通入Cl2,若要使反应完全,则至少需标准状况下Cl2________升.
解析:(1)由得失电子守恒可知:
11.(2009·上海单科高考)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X.
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是______________________.
(2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为______________.
(3)根据上述反应可推知________________.
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:
+
解析:此题为氧化还原反应题.
(1)此题考点为氧化还原反应,其特征为化合价升降,本质为电子的转移,要求能从化合价变化角度来判断氧化剂和还原剂.已知KBrO3为得电子物质,故其化合价必是降低,作氧化剂,那么还原剂只能是题目所提供的AsH3,AsH3中As为-3价,反应后变为H3AsO4,故还原剂为AsH3.
(2)此题出题的依据是氧化还原反应中得失电子守恒.0.2mol KBrO3在反应中得到1mol电子,故每1mol KBrO3得5mol电子,即反应后Br的化合价应降为零价,故另一物质为Br2,同时因为氧化剂、还原剂、氧化产物、还原产物已知,可直接进行配平.
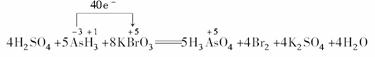
(还原剂) (氧化剂) (氧化产物) (还原产物)
根据化合价升降相等,则应在AsH3前配系数5,在Br2前配系数4,根据原子守恒KBrO3前配8;再根据K原子守恒,K2SO4应在生成物中,系数为4;则H2SO4在反应物中,系数为4;H2O在生成物中,系数为4;配平后用单线桥法标出电子转移方向和数目.
(3)此题的考点为氧化还原反应中的基本规律:氧化剂的氧化性大于氧化产物、还原剂的还原性大于还原产物.故选a、c.
答案:(1)AsH3 (2)Br2 (3)ac 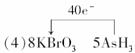
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com