
题目列表(包括答案和解析)
12.有两瓶失去标签的物质的量浓度相同的Na2CO3和NaHCO3稀溶液.下列鉴别方法和所得到的结论不正确的是
( )
A.取少量未知溶液,分别滴加Ba(NO3)2溶液,有沉淀生成的为Na2CO3溶液
B.取少量未知溶液,分别滴加CaCl2溶液,有沉淀生成的为Na2CO3溶液
C.分别滴加酚酞试液,红色较深的是Na2CO3溶液
D.用pH试纸测定两溶液的pH,pH较小的为Na2CO3溶液
解析:Ba(NO3)2、CaCl2均能与Na2CO3反应产生白色沉淀,而均不能与NaHCO3反应,故A、B正确;Na2CO3的碱性比NaHCO3的碱性强,pH大,故C正确,D错误.
答案:D
11.(2009·山东临沂测试)托盘天平的两盘中各放一只盛有等体积、等物质的量浓度盐酸的小烧杯,调整天平平衡后向两烧杯中分别加入等质量的Fe粉和Zn粉,下列现象不可能出现的是
( )
A.开始天平加锌的一端上升
B.最终天平加锌的一端上升
C.最终天平仍平衡
D.最终加铁的一端上升
解析:本题考查金属的化学性质,较难题.如果酸过量,由于锌的活动性大于铁,开始时锌产生氢气的速度快,加锌的一端上升,A对;但最终加锌的一端的增重大于加铁的一端的增重,最终加铁的一端上升,D对;如果金属过量,则加锌的一端和加铁的一端增重相同,最终天平仍平衡,C对.
答案:B
10.下列各组离子一定能大量共存的是
( )
A.在含大量Fe3+的溶液中:NH、Na+、Cl-、SCN-
B.在强碱性溶液中:Na+、K+、AlO、CO
C.在c(H+)=10-13 mol/L的溶液中:NH、Al3+、SO、NO
D.在pH=1的溶液中:K+、Fe2+、Cl-、NO
解析:A项中Fe3+与SCN-反应;B项中在有OH-时该组离子能共存;C项中溶液中OH-与NH作用生成NH3·H2O;D项中溶液中有H+时NO会将Fe2+氧化,故只有B符合题意.
答案:B
9.俄罗斯西伯利亚研究人员开发出一种生物活性吸附剂,可以吸附水中的几乎全部微生物和噬菌体.据俄《科学信息》杂志报道,这种新的吸附剂由成本低廉、环保性能好的棉纤维素和主要成分为氢氧化铝的勃姆石制造而成. 下列有关说法中不正确的是
( )
A.Al(OH)3既能够与盐酸反应又能够与NaOH溶液反应
B.纤维素和淀粉不是同分异构体
C.纤维素能够与醋酸发生酯化反应
D.实验室中Al(OH)3可以由偏铝酸盐和氨水制备
解析:Al(OH)3具有两性,可与酸或强碱反应;其实验室制备方法是用铝盐与弱碱氨水反应(氢氧化铝不溶于氨水);纤维素与淀粉都是高分子化合物,可用[(C6H10O5)n]表示,但其聚合度(n)不同,所以不是同分异构体;纤维素中分子中存在醇羟基,所以可以发生酯化反应.
答案:D
8.(2009·许昌调研)一定体积CO2和O2的混合气体通过足量的Na2O2后,所得气体体积变为原来的3/4,则CO2在原混合气体中的体积分数为
( )
A.25% B.40% C.50% D.75%
解析:设原有混合气体共4体积,则反应后气体减少1体积.由
2CO2+2Na2O2===2Na2CO3+O2 ΔV
2 1 1
V(CO2) 1
所以V(CO2)=2
φ(CO2)=2/4×100%=50%
答案:C
7.下列各选项均有X、Y两种物质,将X缓缓滴入(通入)Y溶液中,无论X是否过量,均能用同一离子方程式表示的是
( )
|
|
X |
Y |
|
A |
稀盐酸 |
碳酸钠溶液 |
|
B |
偏铝酸钠溶液 |
硫酸溶液 |
|
C |
硫化钠溶液 |
氯化铁溶液 |
|
D |
二氧化碳 |
苯酚钠溶液 |
解析:A项中X不足时,反应为CO+H+===HCO;X过量时,反应为CO+2H+===CO2↑+H2O.
B项中,X不足时,反应为AlO+4H+===Al3++2H2O;X过量时,反应为AlO+H++H2O===Al(OH)3↓.
C项中,X不足时,反应为2Fe3++S2-===2Fe2++S↓;X过量时,反应为2Fe3++3S2-===2FeS↓+S↓.
D项中无论CO2过量与否,反应均为CO2+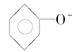 +
+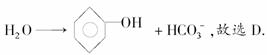
答案:D
6.铁氧体(Fe3O4) 法是处理含铬废水的常用方法.其原理是:用FeSO4把废水中Cr2O还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3·FeO)的复合氧化物(2-xO3·O). 处理含1 mol Cr2O废水至少需要加入a mol FeSO4·7H2O.下列结论正确的是
( )
A.x=1,a=5 B.x=0.5,a=8
C.x=2,a=10 D.x=0.5,a=10
解析:据Cr原子守恒,复合氧化物(2-xO3·O)的物质的量为 mol,由Fe原子守恒有×(3-x)=a,再根据电子守恒得×(2-x)=1×6,联立解得x=0.5,a=10,故选D.
答案:D
5.下列各组溶液,不另加其他试剂就可以将它们分别开的是
( )
A.NaCl,HCl,NaAlO2,NaHCO3
B.Na2SO4,KNO3,(NH4)2SO4,MgCl2
C.FeCl3,NaOH,AlCl3,HNO3
D.AgNO3,NaCl,Na2SO4,NaI
解析:不另加试剂鉴别多种物质有两种主要方法,其一是利用物理性质(主要是颜色)鉴别出其中的一种或几种,再以这种物质作为试剂,看能否区别出余下的物质;其二是假设其中的一种为已知,并以它作为试剂,看能否鉴别余下的物质.本题C中FeCl3呈棕黄色,将其加入其余三种物质中有红褐色沉淀产生的是NaOH,再将NaOH加入其他两种溶液中,有白色沉淀生成的是AlCl3,无变化的是HNO3.
答案:C
4.按下图装置通入X气体,并在管P处点燃,实验结果是澄清石灰水变浑浊,则X、Y可能是
( )
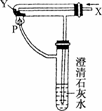
A.H2和Fe2O3 B.CO和CuO
C.H2和Na2CO3 D.CO和Na2CO3
解析:能使澄清石灰水变浑浊的气体应为CO2,可以是CO与CuO在加热条件下反应产生的.
答案:B
3.如图所示装置,试管中盛有水,气球a盛有干燥的固体过氧化钠颗粒,U形管中注有浅红色的水已知,过氧化钠与水反应是放热的.将气球用橡皮筋紧缚在试管口,实验时将气球中的固体颗粒抖落到试管b的水中,将发生的现象是
( )
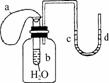
A.U形管内红色褪去 B.试管内溶液变红
C.气球a被吹大 D.U形管水位d<c
解析:2Na2O2+2H2O===4NaOH+O2↑,
因该反应生成O2且放出热量,故气球变大,U形管内液面c端下降,d端上升,故C正确,D错误;该反应是在试管内发生的且无酚酞,故A、B均错误.
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com