
题目列表(包括答案和解析)
3.下列说法正确的是
( )
A.所有的非金属氧化物都是酸性氧化物
B.BaSO4难溶于水,是弱电解质
C.福尔马林、盐酸、明矾、纯碱都是混合物
D.某温度下,NaCl的溶解度为S g,则此温度下,其饱和溶液的质量分数为×100%
解析:A项,CO、NO、NO2不属于酸性氧化物;B项,BaSO4溶解的部分全部电离,属于强电解质;C项,明矾、纯碱属于纯净物.
答案:D
2.下列分散系属于胶体的是
( )
A.淀粉溶液 B.食盐水
C.牛奶 D.碘酒
解析:B、D属于溶液,C属于乳浊液,A属于胶体.
答案:A
1.(2009·烟台调研)用特殊方法把固体物质加工到纳米级(1-100 nm,1 nm=10-9 m)的超细粉末粒子,然后制得纳米材料.下列分散系中的分散质的微粒直径和这种粒子具有相同的数量级的是
( )
A.溶液 B.悬浊液
C.胶体 D.乳浊液
解析:胶体粒子的直径为1 nm-100 nm,纳米材料直径为几纳米至几十纳米,所以胶体中粒子直径与这种超细粉末具有相同的数量级,故C正确.
答案:C
13.现有五种离子化合物A、B、C、D和E,都是由下表中离子形成的:
|
阳离子 |
Ag+ Ba2+ Al3+ |
|
阴离子 |
OH- Cl- SO |
为鉴别它们,分别完成以下实验,其结果是:
①B和D都不溶于水,也不溶于酸;
②A溶于水后,与上述某阳离子反应可生成B,且A溶液与过量氨水反应生成白色沉淀;
③C溶于水后,与上述某阳离子反应可生成D,且C溶液与过量氨水反应生成白色沉淀;
④E溶于水后,与上述某阴离子反应可生成B;
⑤A溶液与适量E溶液反应生成沉淀,再加入过量E溶液,沉淀量减少,但不消失.
请根据上述实验结果,填空:
(1)写出化合物的化学式A________,C________,D________,E________.
(2)A溶液与过量的E溶液反应后,最终得到的沉淀的化学式是________.
解析:解答本题应把局部小规模推断与整体综合判断相结合.①不溶于水、也不溶于酸的物质为BaSO4和AgCl;②、③中可与氨水反应生成白色沉淀的A和C应在Al2(SO4)3和AlCl3中选出;④E中必含有Ba2+;⑤能满足题述条件的只有Al2(SO4)3和Ba(OH)2之间的反应.A为Al2(SO4)3,E为Ba(OH)2.当Ba(OH)2适量时,发生反应Al2(SO4)3+3Ba(OH)2===2Al(OH)3↓+3BaSO4↓;而一旦Ba(OH)2过量,前面生成的Al(OH)3沉淀就会发生溶解,而BaSO4不受影响,反应可表示为Al(OH)3+OH-===AlO+2H2O.结合前面所做推断可确定出B为BaSO4,C为AlCl3,D为AgCl.
答案:(1)Al2(SO4)3 AlCl3 AgCl Ba(OH)2 (2)BaSO4
12.A和B是两种盐,其焰色反应皆为紫色(透过蓝色钴玻璃观察).有关实验及现象如下:

请回答:
(1)写出A、B的化学式________、________.
(2)写出D与FeCl2溶液反应的化学方程式__________________________.
(3)写出A、B反应生成D的离子方程式__________________________________.
(4)H的一种同素异形体的化学式为________.
解析:A、B两种盐,其焰色反应皆为紫色,则均含K元素;A+AgNO3―→白色沉淀C,则可推A是KCl,C是AgCl;B+MnO2气体单质H,则B是KClO3,H是O2;D是Cl2,E是FeCl3,F是KCl、KClO混合物.
答案:(1)KCl KClO3
(2)2FeCl2+Cl2===2FeCl3
(3)5Cl-+ClO+6H+===3Cl2↑+3H2O
(4)O3
11.除去下列各物质中的杂质(括号内为杂质),写出所加试剂(或方法),属离子反应的写出离子方程式.
(1)CO2(HCl)________,__________________________.
(2)KCl(K2CO3)________,________________________.
(3)CO(CO2)________,____________________________.
(4)Cu(CuO)________,____________________________.
解析:除杂的基本原则是除去杂质同时不引入新的杂质.
(1)用饱和NaHCO3溶液,离子反应为
HCO+H+===CO2↑+H2O
(2)用稀HCl溶液,离子反应为
CO+2H+===CO2↑+H2O
(3)足量澄清石灰水,离子反应为
Ca2++2OH-+CO2===CaCO3↓+H2O
(4)用稀H2SO4,离子反应为CuO+2H+===Cu2++H2O
答案:(1)饱和NaHCO3溶液
HCO+H+===CO2↑+H2O
(2)稀盐酸 CO+2H+===CO2↑+H2O
(3)澄清石灰水
Ca2++2OH-+CO2===CaCO3↓+H2O
(4)稀硫酸 CuO+2H+===Cu2++H2O
10.如下图所示,纵坐标表示导电能力,横坐标表示所加溶液的量,以下各组反应,符合该图的是
( )
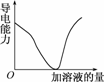
A.Ba(OH)2溶液中滴加稀H2SO4
B.NaOH溶液中滴加稀HCl
C.CH3COOH溶液中滴加KOH溶液
D.Cu(OH)2悬浊液中滴加HNO3溶液
解析:A项,Ba(OH)2+H2SO4===BaSO4↓+2H2O当向Ba(OH)2溶液中滴加稀H2SO4时,最初Ba(OH)2导电;恰好完全反应时生成BaSO4沉淀和水,然后H2SO4导电;B项,反应生成NaCl,导电能力不会减弱为0;C、D两项中开始溶液中因由弱电解质生成强电解质而使导电能力增强,只有A正确.
答案:A
9.下列只能表示一个化学反应的离子方程式的是
( )
A.H++OH-===H2O
B.CO+2H+===H2O+CO2↑
C.Cu(OH)2+2H+===Cu2++2H2O
D.Cu2++2OH-+Ba2++SO===BaSO4↓+Cu(OH)2↓
解析:A表示强酸与可溶性强碱生成可溶性盐的反应,如HCl与NaOH、H2SO4与NaOH;B表示可溶性碳酸盐与强酸反应;D只表示CuSO4溶液与Ba(OH)2溶液的反应;C表示Cu(OH)2与强酸发生反应,故只有D正确.
答案:D
8.(2010·山东德州月考)下列中和反应的离子方程式能以H++OH-===H2O表示的是
( )
A.醋酸和氢氧化钡溶液
B.氢氧化镁和盐酸
C.氢氧化钡溶液和稀硫酸
D.澄清石灰水和硝酸
解析:该离子方程式表示强酸和强碱反应生成可溶性盐和水.A项CH3COOH为弱酸,B项Mg(OH)2难溶,C项生成难溶性盐BaSO4,故A、B、C均错误,只有D正确.
答案:D
7.(2009·广东茂名中学模拟)能正确表示下列反应的离子方程式是
( )
A.足量H2S气体通入Fe2(SO4)3溶液中:
H2S+Fe3+===Fe2++S+2H+
B.足量铁与稀硝酸反应:
Fe+4H++NO===Fe2++2H2O+NO↑
C.醋酸溶液与纯碱溶液:CO+2H+===CO2↑+H2O
D.等物质的量的Ba(OH)2与NaHSO4溶液反应:
Ba2++OH-+H++SO===BaSO4↓+H2O
解析:A项中电荷不守恒;B中电荷不守恒;C中CH3COOH为弱酸,应写化学式,D符合条件.
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com