
题目列表(包括答案和解析)
7.已知1 mol红磷转化为1 mol白磷,吸收18.39 kJ热量.
4P(红,s)+5O2(g)===2P2O5(s) ΔH1
4P(白,s)+5O2(g)===2P2O5(s) ΔH2
则ΔH1与ΔH2的关系正确的是
( )
A.ΔH1=ΔH2 B.ΔH1>ΔH2
C.ΔH1<ΔH2 D.无法确定
解析:据题意知1 mol白磷所具有的能量比1 mol红磷所具有的能量高,因此均为1 mol的白磷和红磷分别与5 mol O2完全反应生成1 mol P2O5固体时,白磷放出的热量更多,但ΔH为负值,故ΔH1>ΔH2,选B.
答案:B
6.2 mol NH3发生反应:2NH3N2+3H2,达到平衡时,测得混合
气体的物质的量为3.6 mol,反应吸收的热量为73.6 kJ,下列表示氮气与氢气反应生成氨气的热化学反应方程式正确的是
( )
A.3H2(g)+N2(g)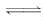
 2NH3(g) ΔH=-92 kJ/mol
2NH3(g) ΔH=-92 kJ/mol
B.3H2(g)+N2(g)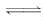
 2NH3(g) ΔH=-368 kJ/mol
2NH3(g) ΔH=-368 kJ/mol
C.3H2(g)+N2(g)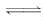
 2NH3(g) ΔH=-73.6 kJ/mol
2NH3(g) ΔH=-73.6 kJ/mol
D.3H2(g)+N2(g)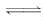
 2NH3(g) ΔH=+73.6 kJ/mol
2NH3(g) ΔH=+73.6 kJ/mol
解析:根据计算,达到平衡时NH3只有0.4 mol,即氨气分解了1.6 mol.当氨气分解了1.6 mol时,吸收73.6 kJ的热量.如果氨气分解了2 mol,则吸收92 kJ的热量.由此可以写出氢气与氮气反应生成氨气的热化学反应方程式.
答案:A
5.(2009·合肥高三质检)已知:
(1)Zn(s)+O2(g)===ZnO(s) ΔH=-348.3 kJ/mol
(2)2Ag(s)+O2(g)===Ag2O(s) ΔH=-31.0 kg/mol
则Zn与Ag2O 反应生成ZnO和Ag的热化学方程式为
( )
A.Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)
ΔH=317.3 kJ/mol
B.Zn+Ag2O===ZnO+2Ag ΔH=317.3 kJ/mol
C.Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)
ΔH=-317.3 kJ/mol
D.2Zn(s)+2Ag2O(s)===2ZnO(s)+4Ag(s)
ΔH=-317.3 kJ/mol
解析:用(1)-(2)得:Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s) ΔH=-348.3 kJ/mol-(-31.0 kJ/mol)=-317.3 kJ/mol,故选C.
答案:C
4.使18 g焦炭发生不完全燃烧,所得气体中CO占1/3体积,CO2占2/3体积,已知:
C(s)+O2(g)===CO(g) ΔH1=-Q1 kJ/mol
CO(g)+O2(g)===CO2(g) ΔH2=-Q2 kJ/mol
与完全燃烧相比较,损失的热量是
( )
A.1/2Q2 kJ B.1/3Q2 kJ
C.1/3(Q1+Q2) kJ D.1/3Q1 kJ
解析:n(C)==1.5 mol,与完全燃烧相比,损失的热量为CO(1.5mol×=0.5 mol)再完全燃烧所对应的热量,即0.5 mol×Q2 kJ/mol=0.5Q2 kJ,故选A.
答案:A
3.下列变化过程放热的是
( )
A.H2O(l)===H2O(g) ΔH=+44.0kJ/mol
B.2HI(g)===H2(g)+I2(g) ΔH=+14.9 kJ/mol
C.形成化学键时共放出能量862 kJ的化学反应
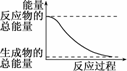
D.能量变化如图所示的化学反应
解析:根据A、B中热化学方程式可知两反应均是吸热反应.本题易误选C,由于选项中未明确在化学反应中断开化学键时所吸收的能量大小,因此不能判断该反应的热效应.
答案:D
2.CH4的燃烧热为890 kJ/mol.下列热化学方程式正确的是
( )
A.CH4(g)+2O2(g)―→CO2(g)+2H2O(l)
ΔH=+890 kJ/mol
B.CH4+2O2―→CO2+2H2O ΔH=-890 kJ/mol
C.CH4(g)+2O2(g)―→CO2(g)+2H2O(l)
ΔH=-890 kJ/mol
D.CH4(g)+2O2(g)―→CO2(g)+2H2O(g)
ΔH=-890 kJ/mol
解析:燃烧放热,ΔH<0,A项错误;热化学方程式中要标明物质的状态,B项错误;据燃烧热的定义知产物水应为液态,故D错误,C正确.
答案:C
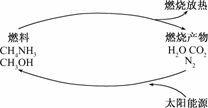
1.有专家指出,如果对燃烧产物如CO2、H2O、N2等利用太阳能使它们重新组合,使之能够实现,那么不仅可以消除对大气的污染,还可以节约燃料,缓解能源危机.在此构想的物质循环中太阳能最终转化为
( )
A.化学能 B.热能
C.生物能 D.电能
解析:根据图示及对光合作用的理解,太阳能量终转化为燃料燃烧所释放的热能,故选项B正确.
答案:B
13.用下面所示的A、B、C三种装置都可制取溴苯.请仔细分析三套装置,然后回答下列问题:

(1)写出三个装置中都发生的反应的化学方程式____________________、____________________;写出B的试管中还发生的反应的化学方程式____________________.
(2)装置A、C中长导管的作用是____________________.
(3)B、C装置已连接好,并进行了气密性检验,也装入了合适的药品,接下来要使反应开始,对B应进行的操作是__________________,对C应进行的操作是____________________.
(4)A中存在加装药品和及时密封的矛盾,因而在实验中易造成的不良后果是____________________.
(5)B中采用了双球吸收管,其作用是________________;反应后双球管中可能出现的现象是________________;双球管内液体不能太多,原因是______________________________________________________.
(6)B装置也存在两个明显的缺点,使实验的效果不好或不能正常进行,这两个缺点是________________、________________.
解析:在FeBr3的作用下,苯与液溴发生取代反应,生成溴苯和HBr;HBr可用AgNO3和HNO3的混合溶液来鉴定;由于反应放热,溴、苯沸点低,易挥发,所以应该有冷凝装置;由于Br2(g)、苯(g)逸入空气会造成环境污染,所以应该有尾气吸收装置.
答案:(1)2Fe+3Br2===2FeBr3
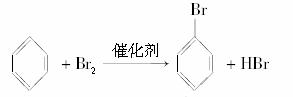
HBr+AgNO3===AgBr↓+HNO3
(2)导气(导出HBr)兼冷凝(冷凝苯和溴蒸气)
(3)打开分液漏斗上端塞子,旋转分液漏斗活塞,使Br2和苯的混合液滴到铁粉上 托起软橡胶袋使Fe粉沿导管倒入溴和苯组成的混合液中
(4)Br2和苯的蒸气逸出,污染环境
(5)吸收反应中随HBr气体逸出的Br2和苯蒸气 CCl4由无色变橙色 被气体压入试管中
(6)随HBr逸出的溴蒸气和苯蒸气不能回流到反应器中,原料利用率低 由于导管插入AgNO3溶液中而产生倒吸
12.(1) 某烷烃的相对分子质量为58,它是由烯烃A与H2加成得到的,则A的结构简式可为__________________.
(2)某烯烃B的相对分子质量为70,这种烯烃与氢气完全加成后,生成有3个-CH3的烷烃,则B的分子式为________,其可能的结构简式分别为________________________________________________.
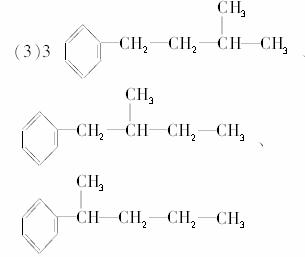
(3)某苯的同系物C的分子式为C11H16,经测定数据表明,分子中除含苯环外不再含其他环状结构,分子中还含有两个-CH3、两个-CH2-和一个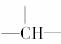 .则C分子由碳链异构所形成的同分异构体有________种.其结构简式为____________________.
.则C分子由碳链异构所形成的同分异构体有________种.其结构简式为____________________.
解析:(1)设烷烃为CnH2n+2,则14n+2=58, n=4,烷烃的

(3)除苯环外,不含其他环状物,由于其余的端基恰好组成一个烷基,说明苯环上只有一个支链.
答案:
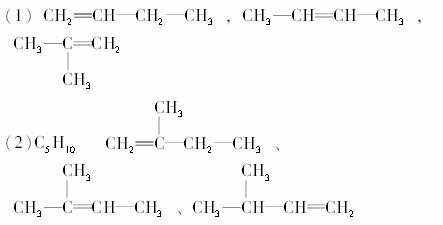
11.(2009·江苏六校联考)由乙烯和其他无机原料可合成环状化合物,其合成过程如下图所示(水及其他无机产物均已省略):
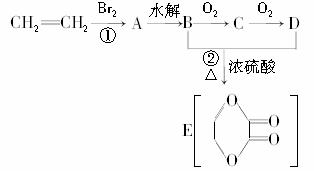
请分析后回答下列问题:
(1)反应的类型分别是①________,②________;
(2)D物质中的官能团为________;
(3)C物质的结构简式为________,物质X与A互为同分异构体,则X的结构简式为________,X的名称为________;
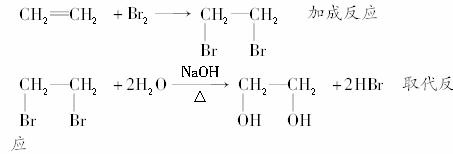
(4)B、D在一定条件下除能生成环状化合物E外,还可反应生成一种高分子化合物,试写出B、D反应生成该高分子化合物的方程式________________.
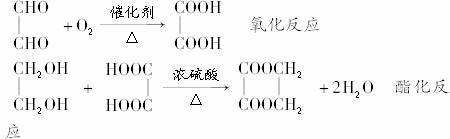
解析:(1)分析框图可知
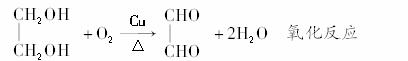


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com