
题目列表(包括答案和解析)
7.可逆反应aA(g)+bB(s) cC(g)+dD(g)在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( )
cC(g)+dD(g)在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( )
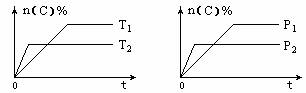
A.温度降低,化学平衡向逆反应方向移动
B.使用催化剂,C的物质的量分数增加
C.化学方程式系数a<c+d
D.无法根据图像确定改变温度后化学平衡移动方向
6. 答案解析:(易)考查学生对化学基本概念的理解能力,物理变化和化学变化的区别是中学化学中必会的基础知识,答案为B。③缓慢氧化是物质发生氧化反应。④品红褪色,是品红与通入气体发生反应生成一种新物质。⑤无水硫酸铜自白变蓝是结合水生成了蓝矾。⑦白磷转化为红磷是生成了一种新单质。⑧浓硝酸久置分解出NO2,NO2又溶解在HNO3中,使得硝酸变黄。以上变化都有新物质生成,属于化学变化。
错点警示:本题尽管简单,但还是会有少部分同学出错,A是干扰性最大的选项。对于②,不能只考虑发生化学反应的爆炸现象,而忽略了属于物理变化的爆炸现象,如给自行车打气,打多了轮胎会爆炸等。
6.下列变化一定属于化学变化的是( )
①导电 ②爆炸 ③缓慢氧化 ④品红褪色 ⑤无水硫酸铜自白变蓝 ⑥工业制O2 ⑦白磷转化为红磷 ⑧久置浓硝酸变黄
A.②③④⑦⑧ B.③④⑤⑦⑧ C.②③⑥⑦ D.④⑤⑦⑧
12. (15分)丁烷的催化裂解可按下列两种方式进行:
C4Hl0 → C2H6+C2H4; C4Hl0 → CH4+C3H6。
化学兴趣小组的同学为探究丁烷裂解气中CH4和C2H6的比例关系,设计实验装置如下图
所示 。
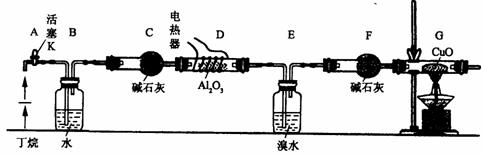
注:CuO能将烃氧化成CO2和H2O;G后面的装置已略去。
请回答下列问题:
(1)如图连接好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的气密性;③排尽装置中的空气。这三步操作的先后顺序依次是 。简要说明排空气和证明空气已排尽的方法
(2)为了调控实验过程中丁烷的气流速度,设置了B装置,操作时应通过观察
 来实现实验的要求。
来实现实验的要求。
(3)若对E装置中的混合物再按以下流程实验:

分离操作I和Ⅱ的操作名称分别是:I ,Ⅱ 。
(4)假设丁 烷完全裂解,且流经各装置中的气体均完全反应,为测定丁烷裂解产物中 n(CH4): n(C2H6)的值,本实验中应该准确获取的数据应有 (选填下列数据序号)。
烷完全裂解,且流经各装置中的气体均完全反应,为测定丁烷裂解产物中 n(CH4): n(C2H6)的值,本实验中应该准确获取的数据应有 (选填下列数据序号)。
①C装置增加的质量 ②E装置增加的质量 ③F装置增加的质量 ④G装置减少的质量
[答案]
(1) ②③① (3分)。
打开活塞K通丁烷气体排出装置中的空气, 以一小试管收集从G装置右端导管口流出的气体,点燃检验其纯度。 (3分)
(2) 气泡的逸出速度
(3) 分液 蒸馏
(4) ②③④ (3分)
11. (18分)高一教材有一演示实验,用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来。
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:
第一, 有氧气生成,第二, 。
Na2O2跟水反应的化学方程式是 。
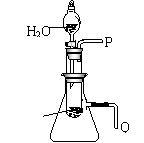
(2)某研究性学习小组拟用右图所示装置(气密性良好)
进行实验,以证明上述结论。
用以验证第一条结论的实验操作是:
;
用以验证第二条结论的实验方法是:
。
(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色。为探究其原因,该小组同学从查阅有关资料中得知:Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性。
请设计一个简单的实验,验证Na2O2跟足量水充分反应后的溶液中有H2O2存在。(只要求写出实验所用的试剂及观察到的现象)
试剂:

 ;
;
现象: 。
(4)该小组同学提出用定量的方法探究Na2O2跟水反应后的溶液中否含有H2O2,其实验方法为:称取2.6g Na2O2固体,使之与足量的水反应,测量产生O2的体积并与理论值比较,即可得出结论。
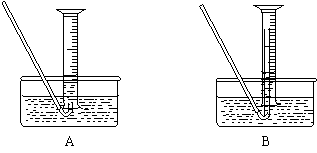
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的(忽略导管在量筒中所占的体积) (填序号),理由是 。
② 若在标准状况下测量气体的体积,应选用的量筒的大小规格为 (选填“100mL”“200 mL”“500 mL”或“1000 mL”)。
[答案]
(1)该反应是放热反应
2Na2O2+2H2O = 4NaOH+O2↑
(2)打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P 处,木条复燃,证明有O2生成。
处,木条复燃,证明有O2生成。

将导管Q浸入水中,反应过程中导管口有气泡冒出。

(3)MnO2 ; 气泡迅速产生,能使带火星的木条复燃。
(4)① B ; 防止气体冷却时发生倒吸现象; ②500mL
10.(13分)用如下图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到 固体B中,回答下列问题:
固体B中,回答下列问题:
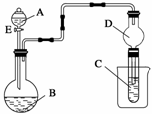
(1)图中D装置在实验中的作用是_____________________________________________。
(2)若 A为30% H2O2溶液,B为MnO2 ,C盛有氢硫酸(H2S)饱和溶液,旋开E后,C中出现浅黄色浑浊的现象,写出C中发生反应的化学方程式为 _________________ 。
。
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀 粉溶液,旋开E后,C中的现象是_________________________;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3(碘酸为强酸),写出该反应的离子反应方程式_______________________________________________________________。
粉溶液,旋开E后,C中的现象是_________________________;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3(碘酸为强酸),写出该反应的离子反应方程式_______________________________________________________________。
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是___________________,C中发生反应的离子方程式为____________________。
[答案]
(1)防倒吸
(2)2H2S+O2===2S↓+2H2O
(3)有气泡出现,同时溶液由无色变成蓝色 6H2O+I2+5Cl2===2IO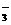 +10Cl-+12H+
+10Cl-+12H+
(4)有白色沉淀生成 Al3++3NH3·H2O===Al(OH)3
↓+3NH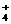
9.(14分)有5瓶白色固体试剂,分别是Ba(NO3)2、KCl、NaOH、CuSO4、(NH4)2SO4,现只提供蒸馏水,通过下面的实验步骤可鉴别它们。请填写下列空白:
(1)各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到的现象是____________________;被检出的物质的化学式是 ____________。
____________。
(2)分别取未检出物质的溶液,往其中加入上述已检出物质的溶液,观察到的现象如下:
①试管中有白色沉淀生成,离子方程式为:____________________;
②试管中有蓝色沉淀生成,离子方程式为:____________________。
(3)最后用一种试剂____________(填所给试剂)的溶液鉴别余下两种未检出的物质,结论为____________。
[解析] (1)题述白色固体溶于水,只有硫酸铜溶液呈蓝色;(2)利用硫酸铜溶液检验出氢氧化钠、硝酸钡;产生白色沉淀的是硝酸钡,产生蓝色沉淀的是氢氧化钠;(3)分别加入硝酸钡溶液,无 现象的是氯化钾;或者,分别加入氢氧化钠溶液,产生刺激性气味的是硫酸铵。
现象的是氯化钾;或者,分别加入氢氧化钠溶液,产生刺激性气味的是硫酸铵。
[答案] (1)均形成溶液,其中一种溶液呈蓝色,其他为无色 CuSO4
(2)①Ba2++SO===BaSO4↓
②Cu2++2OH-===Cu(OH)2↓
(3)Ba(NO3)2(或NaOH) 混合所有白色沉淀产生的是(NH4)2SO4,无现象的为KCl(或混合后产生刺激性气味的是(NH4)2SO4,无现象的是KCl)
8.研究性学习小组做铜与浓硫酸反应实验时,发现试管底部有白色固体并夹杂有少量黑色的物质。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,黑色固体未溶解。过滤、洗涤后,向黑色固体中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,所得溶液加BaCl2溶液后有白色沉淀生成。下列所得结论正确的是 ( )
A.铜与浓硫酸反应所得白色固体是CuSO4·5H2O
B.加BaC l2溶液后所得白色沉淀是BaSO3
l2溶液后所得白色沉淀是BaSO3
C.白色固体中夹杂的少量黑色物质是CuO
D.白色固体中夹杂的少量黑色物质中含元素Cu、S
[解析] 浓硫酸能使CuSO4·5H2O失去H2O,故白色固体应是CuSO4,且CuSO4·5H2O是蓝色的,A项错;因为黑色固体溶于浓硝酸且所得溶液呈蓝色,故含有Cu元素,所得溶液加BaCl2溶液后有白色沉淀生成应为BaSO4,因为浓硝酸有强氧化性,故含有S元素,B错,D项正确。
[答案] D
第Ⅱ卷(非选择题,共60分)
7.下列各组物质中,气体X和气体Y同时通入盛有溶液Z的洗气瓶中(如下图所示),一定没有沉淀生成的是 ( )

|
|
X |
Y |
Z |
|
A |
SO2 |
NO2 |
BaCl2 |
|
B |
O2 |
NH3 |
Al(NO3)3 |
|
C |
SO2 |
CO2 |
CaCl2 |
|
D |
NH3 |
CO2 |
M gSO4 gSO4 |
[解析] A项中NO2将+4价的硫氧化,生成BaSO4沉淀;B项中生成Al(OH)3沉淀;D项中产生Mg(OH)2、MgCO3沉淀;故答案为C。
[答案] C
6.为提纯下列物质(括号内的是杂质),所选用的除杂试剂和 分离方法都正确的是
分离方法都正确的是
( )
|
|
被提纯的物质 |
除杂试剂 |
分离方法 |
|
A |
溴化钠溶液 (NaI) |
氯水、CCl4 |
萃取、分液 |
|
B |
氯化铵溶液 (FeCl3) |
氢氧化钠溶液 |
过滤 |
|
C |
二氧化碳(CO) |
氧化铜粉末 |
通过灼热 的CuO粉末 |
|
D |
苯(苯酚) |
浓溴水 |
过滤 |
[解析] A项中最终所得溶液为NaCl溶液;B项中引入Na+;D项中生成的三溴苯酚溶于苯,不能分离,应用NaOH溶液,分液。故答案为C。
[答案] C
C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com