
题目列表(包括答案和解析)
14.已知25℃、101 kPa条件下:
①4Al(s)+3O2(g)===2Al2O3(s)
ΔH=-2834.98 kJ/mol
②4Al(s)+2O3(g)===2Al2O3(s)
ΔH=-3119.18kJ/mol
由此得出的正确结论是
( )
A.等质量的O2比O3能量低,由O2变O3为吸热反应
B.反应①可确定铝的燃烧热是708.7 kJ
C.O3比O2稳定,由O2变O3为放热反应
D.根据②可确定铝的燃烧热是779.8 kJ/mol
解析:据两热化学方程式知2 mol O3(g)比3 mol O2(g)(等质量)的能量高,所以由O2变为O3为吸热反应,故A正确C错误;据燃烧热的概念可知铝的燃烧热应该由反应①确定,燃烧热为708.7 kJ/mol,故B、D均错误.
答案:A
13.将V1 mL 1.00 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL).下列叙述正确的是
( )
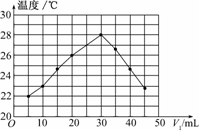
A.做该实验时环境温度为22℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00 mol/L
D.该实验表明有水生成的反应都是放热反应
解析:从图中曲线可以看出,温度为22℃时,V1为5 mL,则V2为45 mL,此时已经开始发生反应,所以22℃一定不是室温,A错.从曲线随V1的增多而升高,随反应的进行,溶液温度升高说明反应放热,化学能转化为热能,B正确.当V1=30 mL时温度最高,说明此时两者恰好完全反应,则c(NaOH)==1.5 mol/L,C错.该实验不能证明有水生成的其他反应也是放热的.
答案:B
12.下列变化中,一定不存在化学能与热能相互转化的是
( )
A.铝热反应 B.金属钝化
C.燃放爆竹 D.干冰气化
解析:D项中干冰的气化属于物质的三态变化,能量变化但物质没变,是物理变化,而A项、B项、C项均属于化学反应,存在化学能与热能的转化.
答案:D
11.下列说法不正确的是
( )
A.化学变化过程是原子的重新组合过程
B.化学反应可分为吸热反应和放热反应
C.化学反应中能量变化多少与其反应量无关
D.化学变化中的能量变化都是以热能形式表现出来的
解析:化学变化过程即原子的重新组合的过程,A正确;据化学反应的热效应可将化学反应分为吸热反应和放热反应,B正确;一个化学反应的能量变化与其反应量有关系,C错误;化学变化中能量变化主要以热能形式表现,还可有光能等,D错误.
答案:CD
10.灰锡(以粉末状存在)和白锡是锡的两种同素异形体.已知:
①Sn(s,白)+2HCl(aq)===SnCl2(aq)+H2(g) ΔH1
②Sn(s,灰)+2HCl(aq)===SnCl2(aq)+H2(g) ΔH2
③Sn(s,灰)  Sn(s,白) ΔH3=+2.1 kJ/mol
Sn(s,白) ΔH3=+2.1 kJ/mol
下列说法正确的是
( )
A.ΔH1>ΔH2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
解析:由③式可以看出,ΔH3>0,灰锡转化为白锡的反应是吸热反应,由此可以说明白锡具有的能量高于灰锡的能量,|ΔH1|>|ΔH2|.由于反应①②都是自发的氧化还原反应,ΔH1<0,ΔH2<0,所以ΔH1<ΔH2.常温下,灰锡将自发地转化为白锡,说明锡在常温下以白锡状态存在.锡制器皿(白锡)长期处于低于13.2℃的环境中,会发生白锡向灰锡转化的反应,由于灰锡以粉末状存在,所以锡制器皿会自行毁坏.由ΔH3=ΔH2-ΔH1>0,也可知A、C项错误.
答案:D
9.(2009·青岛高三质量检测)用CH4催化还原NOx可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)
ΔH=-574 kJ/mol
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)
ΔH=-1160 kJ/mol
下列说法不正确的是
( )
A.反应①②均为放热反应
B.反应①②转移的电子数相同
C.由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH=-a kJ/mol,a<574
D.若用标准状况下4.48 L CH4通过上述反应还原NO2至N2,放出的热量为173.4 kJ
解析:因反应①和②的反应热均为负值,故该两反应均为放热反应,A正确;因两个反应中均有1 mol CH4(g)完全反应其氧化产物均为CO2(g),故转移电子数也相同,B正确;因为等量的H2O(l)比H2O(g)能量低,故a>574,C不正确;D项中,根据盖斯定律,(①+②)/2有:CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ/mol,则0.2 mol CH4反应释放出的热量为0.2 mol×867 kJ/mol=173.4 kJ,故选C.
答案:C
8.已知热化学方程式:
2H2(g)+O2(g)===2H2O(g) ΔH1=-483.6 kJ/mol
则对于热化学方程式:2H2O(l)===2H2(g)+O2(g) ΔH2
下列说法正确的是
( )
A.热化学方程式中化学计量数表示分子个数
B.该反应的ΔH2=+483.6 kJ/mol
C.|ΔH2|<|ΔH1|
D.|ΔH2|>|ΔH1|
解析:热化学方程式中化学计量数只代表物质的量,不代表分子数,A错误;据题意知:2H2O(g)===2H2(g)+O2(g) ΔH3=+483.6 kJ/mol,所以B错误;因2 mol H2O(l)的能量比2 mol H2O(g)的能量低,因此二者均分解生成2 mol H2(g)和1 mol O2(g)所吸收的热量|ΔH2|>|ΔH3|=|ΔH1|,故选D.
答案:D
7.(2009·山东潍坊模拟)在298K、1.01×105Pa下,将22 g CO2通入750 mL 1 mol/L NaOH溶液中充分反应,测得反应放出 x kJ的热量.已知在该条件下,1 mol CO2通入1 L 2 mol/L NaOH溶液中充分反应放出y kJ的热量.则CO2与NaOH溶液反应生成NaHCO3的热化学方程式是
( )
A.CO2(g)+NaOH(aq)===NaHCO3(aq)
ΔH=-(2y-x) kJ/mol
B.CO2(g)+NaOH(aq)===NaHCO3(aq)
ΔH=-(2x-y)kJ/mol
C.CO2(g)+NaOH(aq)===NaHCO3(aq)
ΔH=-(4x-y) kJ/mol
D.2CO2(g)+2NaOH(l)===2NaHCO3(l)
ΔH=-(8x-2y) kJ/mol
解析:0.5 mol CO2与0.75 mol NaOH反应生成0.25 mol Na2CO3和0.25 mol NaHCO3,反应所放出的热量为x kJ,则生成1 mol Na2CO3和1 mol NaHCO3放出4x kJ的热量.1 mol CO2通入含2 mol NaOH溶液中生成1 mol Na2CO3,放出y kJ的热量,则1 mol CO2与含1 mol NaOH的溶液反应所放出的热量为(4x-y)kJ,A项、B项均错;D项中Na2CO3与NaHCO3的状态未标对;只有C正确.
答案:C
6.(2009·广州二中等六校联考)已知下列两个气态物质之间的反应:
C2H2(g)+H2(g)―→C2H4(g)①
2CH4(g)―→C2H4(g)+2H2(g)②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:(Q1、Q2、Q3均为正值)
C(s)+2H2(g)===CH4(g) ΔH=-Q1Ⅰ
C(s)+H2(g)===C2H2(g) ΔH=-Q2Ⅱ
C(s)+H2(g)===C2H4(g) ΔH=-Q3Ⅲ
Q值大小比较正确的是
( )
A.Q1>Q3>Q2 B.Q1>Q2>Q3
C.Q2>Q1>Q3 D.Q3>Q1>Q2
解析:由温度降低时,反应①平衡向右移动,反应①正方向为放热反应,即ΔH1<0;由温度降低时,反应②平衡向左移动,反应②逆方向为放热反应,即ΔH2>0.结合三个反应,可得2(Ⅲ-Ⅱ)=ΔH1<0,即2(-Q3+Q2)<0, Q3>Q2;2(Ⅲ-Ⅰ)=ΔH2>0,即2(-Q3+Q1)>0, Q1>Q3, A项正确.
答案:A
5.下列说法或表示方法中正确的是
( )
A.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多
B.氢气的燃烧热为285.5 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)===2H2O(l) ΔH=-285.8 kJ/mol
C.Ba(OH)2·8H2O(s)+2NH4Cl(s)===BaCl2(s)+2NH3(g)+10H2O(l) ΔH<0
D.已知中和热为57.3 kJ/mol,若将含 0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量要大于57.3 kJ
解析:A项中,硫蒸气放出的热量大于硫磺充分燃烧放出的热量,B项由反应热的定义知ΔH=571.6 kJ/mol,C项反应为吸热反应,故ΔH>0.
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com