
题目列表(包括答案和解析)
6.(2010·四川高考)有关①100 mL 0.1 mol/L NaHCO3、②100 mL 0.1 mol/L Na2CO3两种溶液的叙述不正确的是( )
A.溶液中水电离出的H+个数:②>①
B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:c(CO)>c(H2CO3)
D.②溶液中:c(HCO)>c(H2CO3)
解析:盐类水解可以促进水的电离,而且水解程度越大,这种促进程度越大,故A正确;CO的水解使溶液中阴离子数目增多,B正确;碳酸氢钠溶液中,HCO的水解程度大于电离程度,故c(H2CO3)>c(CO),C错误;CO的第一步水解程度远大于第二步水解,故D正确.
答案:C
5.物质的量浓度相同的下列溶液,pH由大到小排列正确的是( )
A.Ba(OH)2、Na2SO3、FeCl3、KCl
B.Na2SiO3、Na2CO3、KNO3、NH4Cl
C.NH3·H2O、H3PO4、Na2SO4、H2SO4
D.NaHCO3、C6H5COOH、C2H5OH、HCl
解析:FeCl3溶液呈酸性,KCl溶液呈中性,选项A错误;Na2SO4溶液呈中性、H3PO4呈酸性,选项C错误;C2H5OH呈中性,C6H5COOH呈酸性,选项D错误.
答案:B
4.(2010·海淀模拟)下列根据反应原理设计的应用,不正确的是( )
A.CO+H2O HCO+OH- 用热的纯碱溶液清洗油污
HCO+OH- 用热的纯碱溶液清洗油污
B.Al3++3H2O Al(OH)3+3H+ 明矾净水
Al(OH)3+3H+ 明矾净水
C.TiCl4+(x+2)H2O(过量)  TiO2·xH2O↓+4HCl 制备TiO2纳米粉
TiO2·xH2O↓+4HCl 制备TiO2纳米粉
D.SnCl2+H2O Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠
Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠
解析:氯化亚锡易与NaOH溶液反应生成Sn(OH)Cl沉淀.
答案:D
3.(2010·德阳模拟)向0.1 mol/L NaOH溶液中滴加一定量的0.2 mol/L CH3COOH溶液后,测得溶液中c(OH-)>c(H+).则c(OH-)与c(CH3COO-)的大小关系为( )
A.c(OH-)一定大于c(CH3COO-)
B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-)
D.c(OH-)可能大于、小于或等于c(CH3COO-)
解析:当NaOH与CH3COOH刚好反应生成CH3COONa时,c(OH-)<c(CH3COO-);当NaOH过量很多时,c(OH-)>c(CH3COO-);当二者反应到一定程度时,NaOH过量一些,此时有可能c(OH-)=c(CH3COO-).
答案:D
2.(2010·海南高考)常温下,将0.1 mol/L氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,该混合溶液的pH等于( )
A.1.7 B.2.0
C.12.0 D.12.4
解析:c(H+)==0.01 mol·L-1,pH=2.
答案:B
1.(2010·杭州模拟)下列操作会促进H2O的电离,且使溶液pH>7的是( )
A.将纯水加热到90℃
B.向水中加少量NaOH溶液
C.向水中加少量Na2CO3溶液
D.向水中加少量FeCl3溶液
解析:将纯水加热到90℃,水的电离程度增大,c(H+)=c(OH-)>10-7 mol/L,pH<7,A错;向水中加少量NaOH溶液,水中c(OH-)增大,pH>7,但水的电离平衡向逆方向移动,即水的电离受到抑制,B错;向水中加少量Na2CO3溶液,CO水解,水的电离平衡向正方向移动,c(OH-)增大,c(OH-)>c(H+),pH>7,C对;向水中加少量FeCl3溶液,Fe3+水解,水的电离平衡向正方向移动,c(H+)增大,c(H+)>c(OH-),pH<7,D错.
答案:C
5.(2010·石家庄模拟)今有①CH3COOH、②HCl、③H2SO4三种溶液,用序号回答下列问题:
(1)当它们pH相同时,其物质的量浓度由大到小排列是__________________________.
(2)当它们的物质的量浓度相同时,其pH由大到小排列是________________________.
(3)中和等量同一烧碱溶液,需同物质的量浓度的①②③三种酸溶液的体积比为______________________.
(4)体积和物质的量浓度均相同的①②③三溶液,分别与同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积比为________.
解析:(1)CH3COOH是弱酸,HCl、H2SO4是强酸.当它们的pH相同时,其物质的量浓度最大的是CH3COOH,最小的是H2SO4.
(2)当三种酸的物质的量浓度相同时,c(H+)最大的是H2SO4,最小的是CH3COOH,即溶液pH最大的是CH3COOH,最小的是H2SO4.
(3)H2SO4是二元酸,HCl和CH3COOH是一元酸,故中和等量的NaOH溶液,消耗等浓度CH3COOH、HCl、H2SO4的体积比为2∶2∶1.
(4)中和等物质的量的三种酸,消耗NaOH的物质的量的比为1∶1∶2.
答案:(1)①>②>③ (2)①>②>③
(3)2∶2∶1 (4)1∶1∶2
[发展等级评价]
(限时45分钟,满分100分)
4.(2010·杭州模拟)常温下将NaOH溶液与CH3COOH稀溶液混合,不可能出现的结果是( )
A.pH=7且c(CH3COO-)>c(Na+)>c(H+)=c(OH-)
B.pH<7且c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
C.pH>7且c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
D.pH>7且c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
解析:NaOH溶液与CH3COOH稀溶液混合,溶液中含有CH3COO-、Na+、H+、OH-四种离子.pH=7时,c(H+)=c(OH-),根据电荷守恒,则c(CH3COO-)=c(Na+),A错;pH<7时,c(H+)>c(OH-),得到CH3COOH和CH3COONa的混合溶液,且c(CH3COO-)>c(Na+),B对;pH>7时,根据电荷守恒c(CH3COO-)+c(OH-)=c(Na+)+c(H+),C对;pH>7时,当溶质为NaOH和CH3COONa时,可能有c(Na+)>c(OH-)>c(CH3COO-)>c(H+),D对.
答案:A
3.(2010·全国卷Ⅱ)相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )
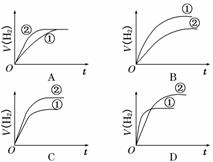
解析:pH相同的一元中强酸的物质的量浓度大于一元强酸的物质的量浓度,所以加入足量锌粉最终产生氢气的量,一元中强酸多,反应过程中,未电离的中强酸分子继续电离,使得溶液中H+浓度比强酸大,反应速率中强酸大于强酸.
答案:C
2.(2010·广东高考)HA为酸性略低于醋酸的一元弱酸.在0.1 mol/L NaA溶液中,离子浓度关系正确的是( )
A.c(Na+)>c(A-)>c(H+)>c(OH-)
B.c(Na+)>c(OH-)>c(A-)>c(H+)
C.c(Na+)+c(OH-)=c(A-)+c(H+)
D.c(Na+)+c(H+)=c(A-)+c(OH-)
解析:HA为一元弱酸,则NaA为强碱弱酸盐,溶液由于A-的水解显碱性,离子浓度大小为:c(Na+)>c(A-)>c(OH-)>c(H+),A、B项均错误;根据溶液中电荷守恒,则c(Na+)+c(H+)=c(A-)+c(OH-),C项错误,D项正确.
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com