
题目列表(包括答案和解析)
3.(2010·杭州模拟)下列实验能达到预期目的的是( )
|
编号 |
实验内容 |
实验目的 |
|
A |
将SO2通入酸性KMnO4溶液中 |
证明SO2的水溶液具有弱酸性 |
|
B |
向少量火柴头的浸泡液中滴加AgNO3、稀HNO3和NaNO2 |
验证火柴头含有氯元素 |
|
C |
在淀粉-KI溶液中滴加少量市售食盐配制的溶液 |
真假碘盐的鉴别 |
|
D |
在少量Fe(NO3)2试样加水溶解的溶液中,滴加稀H2SO4酸化,再滴加KSCN溶液 |
检验Fe(NO3)2试样是否变质 |
解析:SO2通入酸性KMnO4溶液中,由于SO2的还原性使酸性高锰酸钾溶液褪色,A错;用淀粉-KI溶液鉴别市售食盐中是否含有KIO3时,需要加入盐酸酸化:5I-+IO+6H+===3I2+3H2O,C错;在少量Fe(NO3)2试样加水溶解的溶液中滴加稀硫酸,Fe2+会转化为Fe3+,3Fe2++4H++NO===3Fe3++NO↑+2H2O,因此再滴加KSCN溶液无论试样是否变质,溶液均会变为红色,D错.
答案:B
2.(2010·崇文模拟)某课外实验小组设计的下列实验不合理的是( )
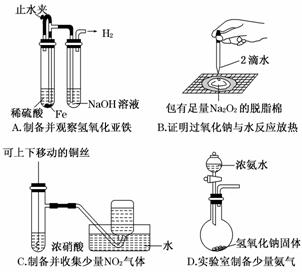
解析:NO2能与水发生反应,不能用排水法收集,选项C错误.
答案:C

[基础等级评价]
1.(2010·邯郸模拟)以下实验能成功的是( )
A.将卤代烃和氢氧化钠溶液混合加热,充分反应后再加入硝酸银溶液观察沉淀的颜色判断卤素原子
B.将铁屑、溴水、苯混合制溴苯
C.在苯酚溶液中滴入少量稀溴水出现白色沉淀
D.将铜丝在酒精灯上加热变黑后,立即伸入无水乙醇中,铜丝恢复成原来的红色
解析:选项A,需加入适量HNO3中和掉 NaOH,否则加入AgNO3溶液时,会生成Ag2O而产生干扰.选项B,溴水不能与苯发生取代反应,应使用液溴.选项C,应使用浓溴水与苯酚反应.选项D,Cu加热时生成CuO,CuO与CH3CH2OH反应时,CuO又被还原为红色的Cu.
NaOH,否则加入AgNO3溶液时,会生成Ag2O而产生干扰.选项B,溴水不能与苯发生取代反应,应使用液溴.选项C,应使用浓溴水与苯酚反应.选项D,Cu加热时生成CuO,CuO与CH3CH2OH反应时,CuO又被还原为红色的Cu.
答案:D
5.(1)如图所示A、B、C、D四种仪器,请选择下列仪器名称的序号,填入相应的空格内:
①烧杯 ②普通漏斗 ③圆底烧瓶 ④锥形瓶 ⑤分液漏斗 ⑥酸式滴定管 ⑦碱式滴定管
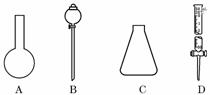
A.________B.________C.________D.________
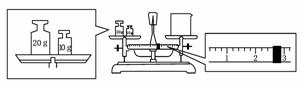
(2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图所示,由图中可以看出,该同学在操作时的一个错误是____________________________,烧杯的实际质量为__________g.
(3)指出下面3个实验中各存在的一个错误:
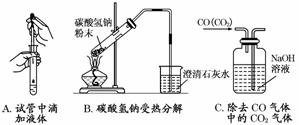
A.____________B.____________C.____________.
解析:使用托盘天平时应将砝码放在右盘,被称量物放在左盘,根据托盘天平的称量原理,左盘质量=右盘质量+游码质量,则烧杯的质量(右盘)=30 g-2.6 g=27.4  g,此时必须注意:标尺的每个小格代表0.2 g.
g,此时必须注意:标尺的每个小格代表0.2 g.
答案:(1)③ ⑤ ④ ⑥
(2)砝码放在左盘,烧杯放在右盘(或砝码和物品的位置放反了) 27.4
(3)胶头滴管口伸入试管中 试管口向上倾斜 混合气体从短导气管进入洗气瓶
4.实验室常用氢氧化钠溶液吸收氯化氢尾气,以防止环境污染.下列既能吸收尾气,又能防止溶液倒吸的装置是( )

解析:A装置虽然能防止倒吸,但会有氯化氢逸入空气而造成环境污染.C、D装置进气管插入了液面以下,不能起到防止倒吸的作用.
答案:B
3. 春运期间,一些易燃、易爆、剧毒品、易腐蚀品等,严禁旅客带上车.下列化学品,可允许旅客带上车的有( )
春运期间,一些易燃、易爆、剧毒品、易腐蚀品等,严禁旅客带上车.下列化学品,可允许旅客带上车的有( )
①浓硫酸 ②氰化钾 ③水银 ④TNT爆药 ⑤汽油 ⑥白磷
A.①②④⑤⑥ B.①②③④
C.①②④ D.没有
解析:凡是危险化学品,均禁止旅客带上车,依据分析,上述所有化学品均属于危险化学品.
答案:D
2.下列说法正确的是( )
A.将量取好的浓硫酸沿器壁缓慢地注入盛有水的量筒中,以配制稀硫酸
B.在实验室中通常将钠保存在煤油里
C.可用过滤法分离氢氧化铁胶体和三氯化铁溶液的混合物
D.将浓硫酸和乙醇按体积比3∶1混合后置于圆底烧瓶中缓慢加热,以制取乙烯
解析:不能在量筒中稀释浓硫酸,A错误;金属钠很活泼,易被氧化,易与水反应,由于密度比煤油大,保存在煤油中可避免被氧化,B正确;过滤分离的是互不相溶的固体与液体的混合物,氢氧化铁胶体和三氯化铁溶液能互溶,且都能通过滤纸,C错误;制取乙烯时应迅速将温度升高至170℃,否则会发生副反应,D错误.
答案:B
1.以下化学试剂的保存方法不当的是( )
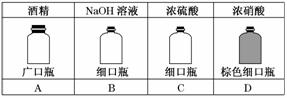
解析:酒精是液体试剂,应保存在细口瓶中.
答案:A
14.(13分)(2010·安徽高考)锂离子电池的广泛应用使回收利用锂资源成为重要课题.某研究性学习小组对废旧锂离子电池正极材料(LiMn2O4、碳粉等涂覆在铝箔上)进行资源回收研究,设计实验流程如下:
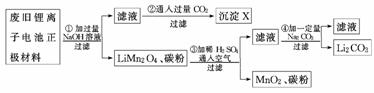
(1)第②步反应得到的沉淀X的化学式为________.
(2)第③步反应的离子方程式是_______________________________________________.
(3)第④步反应后,过滤Li2CO3所需的玻璃仪器有_____________________________.若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:_______________
____________________________________________.
(4)若废旧锂离子电池正极材料含LiMn2O4的质量为18.1 g,第③步反应中加入20.0 mL 3.0 mol·L-1的H2SO4溶液,假定正极材料中的锂经反应③和④完全转化为Li2CO3,则至少有________g Na2CO3参加了反应.
解析:(1)锂离子电池正极材料中的铝箔与NaOH溶液反应生成NaAlO2,在滤液中通入过量CO2时,NaAlO2与CO2反应生成Al(OH)3沉淀.
(2)第③步为LiMn2O4在酸性条件下与氧气反应,该反应中氧气是氧化剂,反应生成硫酸锂、二氧化锰和水.
(3)过滤所用的玻璃仪器有烧杯、漏斗、玻璃棒.若滤液浑浊,则可能是漏斗中液面高于滤纸边缘了,或者是玻璃棒紧靠的不是三层滤纸处,滤纸破损了.
(4)LiMn2O4的物质的量为0.1 mol,最终生成0.05 mol Li2CO3;加入H2SO4一共0.06 mol,与LiMn2O4反应后有剩余;加入的Na2CO3先与剩余的硫酸反应,再与Li+反应生成Li2CO3.
答案:(1)Al(OH)3
(2)4LiMn2O4+4H++O2===8MnO2+4Li++2H2O
(3)烧杯、漏斗、玻璃棒 玻璃棒下端靠在滤纸的单层处,导致滤纸破损,漏斗中液面高于滤纸边缘(其他合理答案均可)
(4)6.4(或6.36)

13.(15分)某化学小组的同学到实验室学习.在实验桌上摆有下列仪器:
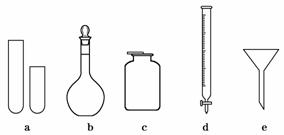
(1)甲同学想用d进行实验,请你说出该仪器使用时的第一步操作:__________________.
(2)关于e的用途,乙同学说可组成防倒吸装置.你还能说出其他两种用途吗?
①________________________________________________________________________;
②________________________________________________________________________.
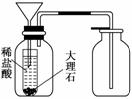
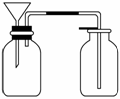 ③丙同学想用右图装置用大理石和稀盐酸反应制取CO2.教师指出,这需要太多的稀盐酸,造成浪费.该同学选用了上面的一种仪器,加在装置上,解决了这个问题,请你把该仪器画在图中合适的位置.
③丙同学想用右图装置用大理石和稀盐酸反应制取CO2.教师指出,这需要太多的稀盐酸,造成浪费.该同学选用了上面的一种仪器,加在装置上,解决了这个问题,请你把该仪器画在图中合适的位置.
解析:(1)仪器d为酸式滴定管,使用时应先检查是否漏液,然后用待装溶液润洗2-3次.(2)仪器e为短颈普通漏斗,其用途还有往细口容器中加液体以及与滤纸组成过滤装置等.(3)为节约药品,结合给出的仪器,只有试管可作反应器,故可在漏斗颈下端接试管来代替广口瓶作反应器.
 答案:(1)检查酸式滴定管是否漏液
答案:(1)检查酸式滴定管是否漏液
(2)①往细口容器中加液体
②组成过滤装置
(3)如图所示(只需画对试管的位置即可)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com