
题目列表(包括答案和解析)
1.铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜。某研究性学习小组模拟工业法对铝片表面进行氧化处理。分别以铅片、铝片为电极,以硫酸溶液为电解液,按照
如图所示装置连接电解池装置,电解40 min后取出铝片,用水冲洗,放在水蒸气中
封闭处理20-30 min,即可得到更加致密的氧化膜。下列有关说法正确的是 ( )
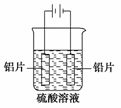
A. 电解时电子从电源负极→导线→铝极,铅极→导线→电源正极
B.在电解过程中,H+向阳极移动,SO向阴极移动
C.电解过程阳极周围溶液的pH下降
D.电解的总反应为2Al+6H+===2Al3++3H2↑
15.(1)Zn(或锌) 正极
(2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀 b
(3)2H++2e-―→H2↑ 87

14.(1)2Fe―→2Fe2++4e- 2H2O+O2+4e-―→4OH-
(2)Fe2++2OH-===Fe(OH)2↓,4Fe(OH)2+O2+2H2O===4Fe(OH)3
(3)4Fe+3O2+6H2O―→4Fe(OH)3
13.正极反应:Ag2O+H2O+2e-―→2Ag+2OH-
负极反应:Zn+2OH-―→ZnO+H2O+2e-
11.C 12.A
16.(12分)如图所示是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,G是灵敏电流计,其指针总是偏向电源正极。
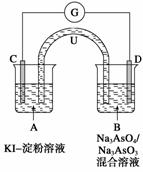
(1)As(砷)位于元素周期表中第4周期ⅤA族,则Na3AsO4溶液的pH____________(填“>7”、“<7”或“=7”)。
(2)向B杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A杯中的主要实验现象是______________________,D电极上的电极反应式为______________________________
________________________________________________________________________。
(3)一段时间后,再向B杯中加入适量的质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置的总的离子方程式为_______________________________
________________________________________________________________________。
(4)再过一段时间后,G的指针逐渐归零,此时实验装置中的化学反应已经达到化学平衡状态,该反应的化学平衡常数的表达式为K=__________________________________。
答案 1.C 2.A 3.B 4.B 5.B 6.A 7.C 8.B 9.C 10.B
15.(12分)(2009·山东理综,29)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是____________。电池工作时,电子流向______________(填“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是________________________________________________________________________。
欲除去Cu2+,最好选用下列试剂中的____________(填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是________________________________________________________________________。
若电解电路中通过2 mol电子,MnO2的理论产量为______________g。
14.(8分)炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便出现了红棕色的锈斑[该锈斑为Fe(OH)3失水的产物]。请用有关的电极反应式、离子方程式和化学方程式表示Fe(OH)3的生成。
(1)负极:_________________________________________________________________,
正极:___________________________________________________________________;
(2)离子方程式:__________________________________________________________;
(3)总的化学方程式:_______________________________________________________。
13.(8分)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极材料分别是Ag2O和Zn,电解质溶液为KOH,总反应为Ag2O+Zn===2Ag+ZnO,试写出该电池的电极反应。
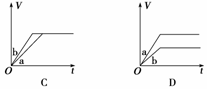
12.将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加少量CuSO4溶液,下图中产生H2的体积V(L)与时间t(min)的关系,其中正确的是 ( )
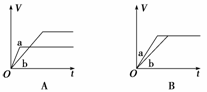
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com