
题目列表(包括答案和解析)
8.(2010·北京市西城区抽样)下列叙述中,正确的是( )
A.在船舶的外壳装上铜块可防止其发生电化学腐蚀
B.MnO2、FeCl3和CuSO4都可加快H2O2的分解速率
C.FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3
D.用惰性电极分别电解CuCl2溶液和MgCl2溶液分别得到单质Cu和Mg
解析:船舶的外壳装上铜块形成原电池,铁作为负极而被腐蚀,A错;FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧分别得到Fe2O3、Fe2(SO4)3,C错;用惰性电极电解MgCl2溶液得到Mg(OH)2、H2和Cl2,D错。
答案:B
7.(2010·江苏卷)下列说法不正确的是( )
A.铅蓄电池在放电过程中,负极质量减小,正极质量增加
B.常温下,反应C(s)+CO2(g)===2CO(g)不能自发进行,则该反应的ΔH>0
C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
D.相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱
解析:本题考查电化学、化学反应速率、离子的氧化性等知识,意在考查考生对化学基本理论的掌握情况。A项,铅蓄电池在放电过程中,负极和正极的质量均减小,故不正确;B项,正确;C项,催化剂可以改变化学反应速率,但不能影响化学平衡,即不能提高转化率,不正确;D项,正确。
答案:AC
6.(2010·四川省诊断性测试)下列说法中一定正确的是( )
A.周期表中同主族元素单质的熔点从上到下逐渐增高
B.12 g金刚石与8 g CH4所含共价键数目相等
C.钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水
D.若将AlCl3溶液、Na2SO3溶液蒸干并灼烧可分别得到Al2O3和Na2SO3
解析:A项周期表中同主族元素单质的熔点从上到下不一定逐渐增高,例如金刚石的熔点比晶体硅的熔点高;C项中钢铁在海水中比在河水中更易腐蚀,主要原因是海水中含大量电解质;D项中Na2SO3溶液在蒸干并灼烧的过程中容易被空气中的氧气氧化生成Na2SO4。
答案:B
5.(2010·重庆市诊断性测试)有下列两种假设:①一种碱溶液与一种盐溶液混合反应后,生成一种强碱性物质;②两种酸溶液混合反应后,溶液的酸性减弱。其中确有具体例证存在的是( )
A.①② B.②
C.① D.都不存在
解析:①可能是Ca(OH)2与Na2CO3反应生成NaOH,②可能是HI与HNO3发生氧化还原反应。
答案:A
4.(2010·成都市检测)在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)⇌2HBr(g);ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法不正确的是( )
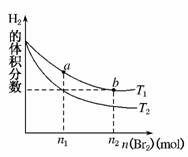
A.由图可知:T1>T2
B.a、b两点的反应速率:b>a
C.为了提高Br2(g)的转化率,可采取将HBr液化并及时移走的方法
D.T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加
解析:选项A,根据反应:H2(g)+Br2(g)⇌2HBr(g);ΔH<0,升温平衡向着逆反应方向移动,H2的体积分数增大,根据图示变化,可知T1>T2。选项B,b点Br2的浓度比a点Br2的浓度大,反应速率也大,正确。选项C,降低生成物HBr(g)的浓度,有利于平衡向着正反应方向移动,Br2(g)的转化率提高。选项D,体积不变时,在Br2(g)物质的量较多的情况下,平衡时HBr的体积分数可能减小。
答案:D
3.如图是元素周期表中短周期的一部分,B原子与C原子核外电子数之和是A的4倍。则下列推断正确的是( )
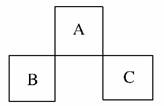
A.A、B、C三者均为非金属元素
B.A、B、C三者可以形成一种离子化合物
C.A、B、C三者核电荷数之和为32
D.B的氢化物比C的氢化物稳定
解析:设A原子的核外电子数为x,则B为(x+7)、C为(x+9),由题意知x+7+x+9=4x,解得x=8,确定A为氧元素、B为磷元素、C为氯元素。故A选项正确。
答案:A
2.(2010·北京卷)下列解释实验事实的方程式不准确的是( )
A.0.1 mol/L CH3COOH溶液的pH>1:CH3COOH⇌CH3COO-+H+
B.“NO2球”浸泡在冷水中,颜色变浅:⇌;ΔH<0
C.铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO===3Fe2++2NO↑+4H2O
D.向Na2CO3溶液中滴入酚酞溶液,溶液变红:CO+H2O⇌HCO+OH-
解析:本题考查方程式的正误判断,意在考查考生运用化学原理分析实验事实的能力。0.1 mol/L CH3COOH溶液的pH>1,则c(H+)<0.1 mol/L,说明醋酸没有完全电离,存在电离平衡:CH3COOH⇌CH3COO-+H+,A项正确;“NO2球”浸泡在冷水中,温度降低,平衡2NO2⇌N2O4向正方向移动,颜色变浅,B项正确;铁溶于稀硝酸,溶液变黄,说明Fe被氧化为Fe3+:Fe+4H++NO===Fe3++NO↑+2H2O,C项错误;Na2CO3溶液中由于CO水解,溶液显碱性,滴入酚酞溶液,溶液变红,D项正确。
答案:C
1.(2010·江西省联考)2009年11月13日,美国NASA特别发表一份声明,称月球上存在大量的水。下列关于水的说法不正确的是( )
A.水分子内存在极性共价键和氢键
B.在某些化学反应中,水可以作氧化剂
C.在常温时,100 mL的水中有1×10-8mol H2O电离
D.在水中加入碳酸钠固体,能促进水的电离
解析:水分子内不存在氢键,分子间存在氢键,故A项错误。
答案:A
18.(10分)芳香族化合物B、C、F与链状有机物A、D、E、G间的转化关系如下图所示。B中苯环上的一溴代物有四种,D可发生银镜反应,C、G属于同类有机物。以下变化中,某些反应条件及产物未标明。C、G组成元素相同,Mr(C)-Mr(G)=76,C中碳、氢、氧原子个数比为5?6?1,G的通式为C2nH4nOn,在某条件下,G蒸气密度是氦气的22倍。X是一种相对分子质量为32的单质。1 mol F与足量碳酸氢钠溶液反应在标准状况下产生气体44.8 L。
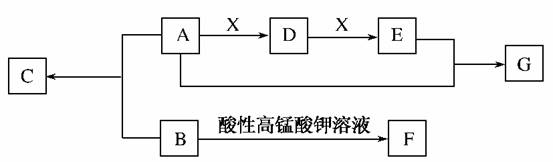
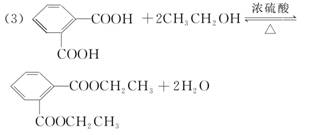
(1)C可能的结构简式为___________________________________________。
(2)写出D发生银镜反应的化学方程式:_______________________________
________,其反应类型是________。
(3)一定条件下F与足量A发生反应的化学方程式为_____________________________。
(4)同时符合下列条件的B的同分异构体有________种。
a.能发生水解反应
b.能与新制氢氧化铜悬浊液在加热条件下反应
c.分子中含有苯环
解析:Mr(G)=22×4=88,G的分子式为C4H8O2,Mr(C)=88+76=164,C的分子式为C10H12O2,X为氧气。由A可进行两步氧化得到E,可知A为醇,E为羧酸,且A与E中碳原子个数相同。又A与E反应生成G,可推得:A为CH3CH2OH,E为CH3COOH,D为CH3CHO。由于G是酯,C与G属于同类有机物,故C也为酯。由A(C2H6O)和B反应可生成酯C(C10H12O2),结合反应前后原子守恒关系,可推得B的分子式为C8H8O2,而B与A可发生酯化反应,可知B为羧酸,故B含有一个羧基和一个甲基,而B中苯环上的一溴代物有四种,那么B苯环上羧基和甲基必处于邻位或间位,故B有两种结构,由此可推知C的结构。根据F与碳酸氢钠反应产生二氧化碳:1 mol F→2 mol CO2→2 mol NaHCO3。说明F是邻苯二甲酸或间苯二甲酸。符合条件的B的同分异构体中含有一个苯环、一个醛基、一个酯基,有两种情况:一种情况,苯环+甲基+甲酸基;另一种情况:苯环+-CH2O-CHO。
答案:(1)
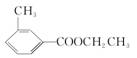
(2)CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag↓+3NH3+H2O 氧化反应
(4)4
17.(10分)(2010·武汉市调研)PET是聚酯类合成材料,以卤代烃为原料合成PET的线路如下(反应中部分无机反应物及产物已省略)。已知RX2(R、R′代表烃基,X代表卤素原子)是芳香族化合物,相对分子质量为175,其中X元素的质量分数为40.6%。
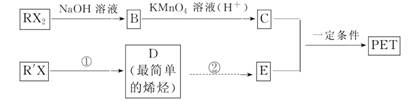
请回答下列问题:
(1)RX2的分子式为________。
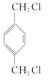
(2)RX2苯环上只有两个取代基,且苯环上的一硝基代物只有一种,则RX2的结构简式为________。
(3)1 mol C与足量的NaHCO3溶液反应可放出________L CO2(标准状况)。
(4)反应①的化学方程式为________________,其反应类型为________;从D到E,工业上一般通过两步反应来完成,若此处原子利用率为100%的角度考虑,假设通过D与某种无机物一步合成E,该无机物是________。
(5)由C与E合成PET的化学方程式为________________________________________。
(6)矿泉水瓶、碳酸饮料瓶等瓶底通常有如图标识,这就是塑料回收标志,其中数字01到07和英文缩写用来指代所使用的树脂种类。有关该标识的判断正确的是(填相应的序号)________。

①PET材料制作的容器可以用来长期盛装酒、油等物质
②PET材料是线性高分子材料,具有热塑性
③PET材料制作的饮料瓶使用一段时间后,可能释放出致癌物,所以这种饮料瓶不能用来作水杯
④塑料回收标志使得塑料品种的识别变得简单容易,还可以降低回收成本
解析:由RX2的相对分子质量为175,其中X元素的质量分数为40.6%,可求得M(X)=175×40.6%/2=35.5,X为Cl元素。M(R-)=175×59.4%=104,烃基R-为C8H8-,则RX2的分子式为C8H8Cl2。RX2苯环上有两个取代基,且苯环上的一硝基代物只有一种,说明苯环上的两个取代基是相同的取代基,且处于对位关系。连两个取代基的苯环为C6H4,结合RX2的分子式C8H8Cl2,则取代基为-CH2Cl。由RX2的结构简式可推知B为对苯二甲醇,则C为对苯二甲酸,1 mol对苯二甲酸与NaHCO3反应生成2 mol CO2。D是最简单的烯烃,最简单的烯烃是乙烯,反应①是氯乙烷转化为乙烯,故反应①是消去反应。E为乙二醇,由乙烯转化为乙二醇,可采用乙烯与H2O2反应。C与E可通过缩聚反应合成PET。用PET塑料长期盛装酒、油,能使塑料溶解,故①错误。
答案:(1)C8H8Cl2
(2)
(3)44.8
(4)CH3CH2Cl+NaOH醇△CH2===CH2↑+NaCl+H2O
消去反应 H2O2
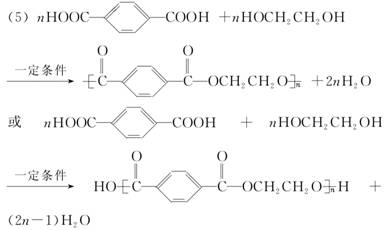
(6)②③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com