
题目列表(包括答案和解析)
4.(2011浙江高考8)下列说法不正确的是
A.变色硅胶干燥剂含有CoCl2,干燥剂呈蓝色时,表示不具有吸水干燥功能
B.“硝基苯制备”实验中,将温度计插入水浴,但水银球不能与烧杯底部和烧杯壁接触
C.“中和滴定”实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗净后,必须干燥或润洗后方可使用
D.除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
解析:A.错误,无水CoCl2呈蓝色,具有吸水性
B.正确,烧杯底部温度高。
C.正确,滴定管和移液管需考虑残留水的稀释影响。
D.正确,利用SO2的还原性,用KMnO4酸性溶液除去。
答案:A
[评析]本题考察实验化学内容。
化学是以实验为基础的自然科学。实验是高考题的重要内容。要解好实验题首先必须要认真做好实验化学实验,在教学中要重视实验的操作与原理,好的实验考题就是应该让那些不做实验的学生得不到分;让那些认真做实验的学生得好分。从题目的分析也可以看出,实验题目中的很多细节问题光靠讲学生是会不了的。必须去做实验学生才能会真正领悟。
3. (2011江苏高考13)下列有关实验原理、方法和结论都正确的是
A.向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体
B.取少量溶液X,向其中加入适量新制氨水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+
C.室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液,可除去苯中少量苯酚
D.已知I3- I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
解析:本题属于常规实验与基本实验考查范畴。
A.饱和FeCl3溶液逐滴滴入沸水中,并继续加热一段时间,可制取Fe(OH)3胶体。滴加过量氨水,就会产生Fe(OH)3沉淀。
B.溶液X中应先滴KSCN溶液,不呈红色,再滴入适量新制氨水,溶液变红,才能说明X溶液中一定含有Fe2+。
C.苯酚与NaOH溶液反应可生成水溶性的苯酚钠,可与苯分层,实现分离除杂。
D.溶解平衡I3- I2+I-中,加入适量CCl4,有利于溶解平衡I3-
I2+I-中,加入适量CCl4,有利于溶解平衡I3- I2+I-向右移动,I2溶解在CCl4中显紫色。
I2+I-向右移动,I2溶解在CCl4中显紫色。
[备考提示]常见物质的制备、分离提纯、除杂和离子检验等都是学生必备的基本实验技能,我们要在教学中不断强化,反复训练,形成能力。
答案:C
2.(2011江苏高考10)下列图示与对应的叙述相符的是
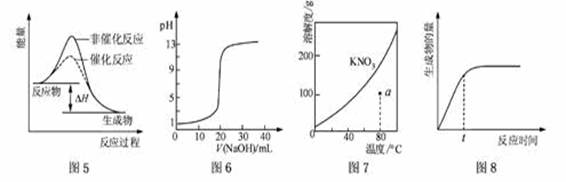
A.图5表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图6表示0.1000 mol·L-1NaOH溶液滴定20.00mL0.1000 mol·L-1CH3COOH溶液所得到的滴定曲线
C.图7表示KNO3的溶解度曲线,图中a点所示的溶液是80 ℃时KNO3的不饱和溶液
D.图8 表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时反应物转化率最大
解析:本题考查学生对化学反应热效应、酸碱中和滴定、溶解度曲线、平衡转化率等角度的理解能力。是基本理论内容的综合。高三复习要多注重这一方面的能力训练。
A.图5表示反应物总能量大于生成物总能量,是放热反应。
B.图6中当NaOH未滴入之前时,CH3COOH的pH应大于1。
C.图7通过a作一条辅助线,与KNO3的溶解度曲线有一交点在a点之上,说明a点溶液是不饱和溶液。
D.图8 表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时曲线并没有达到平衡,所以反应物的转化率并不是最大。
答案:C
1.(2011江苏高考7)下列有关实验原理或实验操作正确的是
A.用水湿润的pH试纸测量某溶液的pH
B.用量筒量取20 mL0.5000 mol·L-1 H2SO4溶液于烧杯中,加水80mL,配制成0.1000 mol·L-1H2SO4溶液
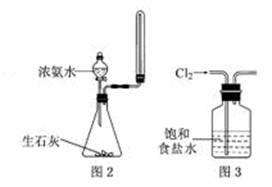
C.实验室用图2所示装置制取少量氨气
D.实验室用图3所示装置除去Cl2中的少量HCl
解析:本题属于基础实验与基本实验操作的考查范畴。
A.pH试纸用水湿润后将冲稀待测溶液。
B.0.5000 mol·L-1 H2SO4溶液与水混合,混合溶液的体积不是两者的简单之和。
C.收集试管带塞子将无法收集到氨气。
D.根据溶解平衡原理,Cl2在饱和食盐水溶解度很小,而HCl极易溶解。
本题以pH试纸试用、常见气体制取、溶液配制、除杂中的实验操作为素材,考查学生对实验操作的熟悉程度和实验原理的应用能力,试图引导中学化学教学关注化学实验操作的真实性。
答案:D
5.(2011江苏高考8)设NA为阿伏伽德罗常数的值。下列叙述正确的是
A.1mol甲醇中含有C-H键的数目为4NA
B.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA
C.标准状况下,2.24L已烷含有分子的数目为0.1NA
D.常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA
解析:本题考查阿伏加德罗常数计算中一些常见问题和注意事项。
A.甲醇的结构简式是CH3OH,故1mol甲醇中含有C-H键的数目为3NA。
B.溶液体积未知,无法计算OH-的数目。
C.标准状况下已烷为液态,不适用于气体摩尔体积,无法计算。
D.Na2O2与足量H2O反应,共生成0.2molO2,O的化合价-1价转变为0价,转移电子1mol,0.2×2=0.4NA。
解决此类问题的关键是:灵活应用各种知识,尤其基本概念与理论中元素守恒、化学键问题、晶体结构问题、氧化还原中电子转移问题、可逆反应问题及物质的量计算中一些特殊物质的状态等。
[备考提示]结合阿伏伽德罗常数为NA,判断一定量的物质所含有的某种粒子数目的多少,是高考命题的热点之一,在近几年的各种高考试题中保持了相当强的连续性。这种题型所涉及的指示非常丰富,在备考复习时应多加注意,强化训练,并在平时的复习中注意知识的积累和总结。
答案:D
4. (2011全国II卷12)NA为阿伏伽德罗常数,下列叙述错误的是
A.18gH2O中含的质子数为10NA
B.12g 金刚石含有的共价键数为4NA
C.46gNO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
解析:金刚石中平均每一个碳原子形成2个共价键,因此12g 金刚石含有的共价键数为2NA
答案:B
3.(2011海南)设NA是阿伏加德罗常数的数值,下列说法正确的是
A.1molAl3+离子含有的核外电子数为3NA
B.1molCl2与足量的铁反应,转移的电子数为3NA[来
C.10LpH=1的硫酸溶液中含有的H+离子数为2NA
D.10LpH=13的NaOH溶液中含有的OH-离子数为NA[来源:ZXXK]
[答案]D
命题立意:阿佛加德罗常数的考查
解析:A选项中Al3+是10电子粒子;B选项中计算要以Cl2为计算依据;C选项中硫酸已经完全电离,不要重复计算;D选项由pH=13计算OH-浓度为0.1mol/L。
[技巧点拨]关于NA于的题主要是陷阱的识别,平时要多注意积累。
2.(2011新课标全国)下列叙述正确的是
A.1.00mol NaCl中含有6.02×1023个NaCl分子
B. 1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023
C.欲配置1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中
D.电解58.5g 熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠
解析:NaCl属于离子化合物,不存在NaCl分子,A不正确;Na+的最外层已经达到8电子稳定结构,所以B正确;1.00L ,1.00mol.L-1的NaCl溶液是指1.00molNaCl即58.5g NaCl溶于水配成1L溶液,而不是指溶剂为1L,C不正确;有原子守恒可知58.5g NaCl只能生成0.5mol氯气,在标准状况下是11.2L,D不正确。
答案:B
1.(2011广东高考9)设nA为阿伏伽德罗常数的数值,下列说法正确的是
A、常温下,23g NO2含有nA个氧原子
B、1L0.1mol•L-1的氨水含有0.1nA个OH―
C、常温常压下,22.4LCCl4含有个nA个CCl4分子
D、1molFe2+ 与足量的H2O2溶液反应,转移2nA个电子
解析:本题考察以物质的量为核心的有关计算和判断。NO2的摩尔质量是46g/mol,所以23g NO2的物质的量是0.5mol,含有0.5mol×2=1mol氧原子,即含有nA个氧原子,A正确;NH3·H2O属于弱电解质,在溶液中部分电离,因此1L0.1mol•L-1的氨水不可能电离出0.1molOH-,B不正确;常温常压下,CCl4是液体,因此不适用于气体的摩尔体积,即22.4LCCl4不是1mol,C不正确;Fe2+ 被氧化,产物是Fe3+ ,因此1molFe2+ 与足量的H2O2溶液反应,转移nA个电子,D也不正确。
答案:A
8.(2011江苏高考20,14分)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知: CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=-247.4 kJ·mol-1
2H2S(g)=2H2(g)+S2(g) △H=+169.8 kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 。
(2)H2S热分解制氢时,常向反应器中通入一定比例空气,使部分H2S燃烧,其目的是
。燃烧生成的SO2与H2S进一步反应,生成物在常温下均非气体,写出该反应的化学方程式: 。
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图11所示。图中A、B表示的物质依次是 。
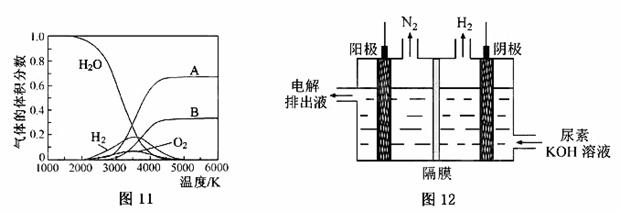
(4)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图12(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为 。
(5)Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为 。
解析:本题以新能源为背景涉及元素化合物性质、热化学方程式和电极反应方程式的书写、读图读表的综合题,是以化学知识具体运用的典型试题。
(1)利用盖斯定律即可得出;(2)H2S热分解制氢属于吸热反应,需要提供能量;(3)在很高的温度下,氢气和氧气会分解生成氢原子和氧原子;(4)阳极失去电子,在碱性溶液中碳原子变成CO32-。
[备考提示]高三复习一定要关注生活,适度加强综合训练与提升。
答案:(1)CH4(g)+2H2O(g) =CO2(g) +4H2(g) △H=165.0 kJ·mol-1
(2)为H2S热分解反应提供热量 2H2S+SO2 =2H2O+3S (或4H2S+2SO2=4H2O+3S2)
(3)H、O(或氢原子、氧原子)
(4)CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O
(5)2Mg2Cu+3H2 MgCu2+3MgH2
MgCu2+3MgH2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com