
题目列表(包括答案和解析)
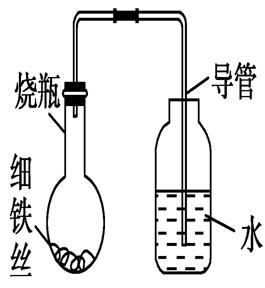
10.某学生在A、B、C、D四只小烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝(并使铁丝完全浸没在食盐水中),然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如下表(表中所列数据为导管中水面上升的高度/cm)所示:
|
时间/小时 |
0 |
0.5 |
1.0 |
1.5 |
2.0 |
2.5 |
3.0 |
|
|
A瓶(盛干燥细铁丝) |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
|
B瓶(盛浸过食盐水的细铁丝) |
0 |
0.4 |
1.2 |
3.4 |
5.6 |
7.6 |
9.8 |
|
|
C瓶(盛浸过清水的细铁丝) |
0 |
0 |
0 |
0.3 |
0.8 |
2.0 |
3.5 |
|
|
D瓶(盛完全浸没在食盐水中的细铁丝) |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
(1)为什么有的导管中水面会上升?________________________________________________________________________
________________________________________________________________________。
(2)上述实验中,铁生锈的速率由大到小的排列顺序为(填小烧瓶的字母编号)________________________________________________________________________。
(3)影响铁生锈的因素除氧气外,还有________________________________________________________________________。
(4)日常生活中常见到铁制品生成铁锈,试写出铁制品生成铁锈(Fe2O3·xH2O)的化学方程式________________________________________________________________________。
(5)通过以上研究你认为在日常生活中应如何保护铁制品?
________________________________________________________________________(至少回答两种方法)
[解析] 铁丝在食盐水中会形成原电池,负极反应为2Fe-4e-===2Fe2+;正极反应为2H2O+O2+4e-===4OH-,由于铁丝腐蚀过程中消耗了O2,使瓶内气体的物质的量减少,压强减小,致使导管中水面上升,产生的Fe2+和OH-结合成Fe(OH)2:Fe2++2OH-===Fe(OH)2,Fe(OH)2进一步氧化生成Fe(OH)3:4Fe(OH)2+O2+2H2O===4Fe(OH)3,2Fe(OH)3===Fe2O3+3H2O,从而形成铁锈。
[答案] (1)氧气消耗后,瓶内气体物质的量减少,导致瓶内压强减小,因此导管中水面上升
(2)B>C>A=D
(3)水、电解质(或电解质溶液)
(4)4Fe+3O2+2xH2O===2Fe2O3·xH2O
(5)洗净擦干涂油;与较活泼的金属锌用导线连接;将铁制品置于通风干燥处,避免将其置于潮湿处等
8.钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在________部分发生反应,在________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为________________________;加入硅、锰和铝的目的是________________________________________________________________________。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹________(填“前”或“后”)加入,原因是________________________________________________________________________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用做________。
[答案] (1)炉身 炉腰
(2)2P+5FeO+3CaOCa3(PO4)2+5Fe
脱氧和调整钢的成分
(3)后 避免Cr被氧化(或“氧吹前加入Cr会形成炉渣被除去”)
(4)CO 燃料(或还原剂)
7.在国际环境问题中,聚苯乙烯等材料的一次性使用带来的“白色污染”是极为严重的环境问题之一,最近研制的一种可降解塑料,代号为3HB,结构简式为
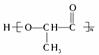 具有良好的生物适应性,能在自然界中自行降解,回答:
具有良好的生物适应性,能在自然界中自行降解,回答:
(1)可降解塑料3HB,在自然界中通过________(填序号)反应降解为该聚合物的单体。
A.加成 B.消去 C.水解 D.氧化
(2)该聚合物的单体为______________,单体中具有的官能团的名称为______________。
(3)各取1 mol该单体分别与钠和碳酸氢钠溶液完全反应时,分别消耗钠和碳酸氢钠的物质的量之比为______。
(4)写出由单体生成降解塑料3HB的化学方程式:
________________________________。
[答案] (1)C (2) 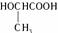 醇羟基、羧基
醇羟基、羧基
(3)2∶1
(4)
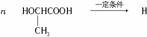
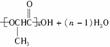
6.

“神舟七号”回收伞(如图)不同于普通的航空伞,它是采用强力高、重量轻、缓冲性好的特制涤纶材料制成的,伞撑开的面积有1 200平方米。下列关于涤纶材料的说法中不正确的是( )
A.涤纶属于高分子材料
B.“神舟七号”回收伞用的这种涤纶材料耐高温
C.涤纶属于合成橡胶
D.合成涤纶的反应属于聚合反应
[答案] C
5.下列关于金属保护方法的说法正确的是( )
A.在铁制品表面涂上搪瓷可以防腐,若搪瓷层破损后仍能起防止生锈的作用
B.镀锌铁制品表面的锌层破损后仍能起到防止铁生锈的作用
C.钢铁制造的暖气管外常涂有一层沥青,这是一种改变金属内部结构的方法
D.轮船外壳水线以下常装有一些锌块,这是利用了牺牲阴极的阳极保护法
[解析] 搪瓷层破损后不能起防止生锈的作用;锌比铁活泼,锌层破损后,发生电化腐蚀时,锌作负极,仍能起到防止铁生锈的作用;涂沥青是表面膜保护法,而不是改变了金属内部结构;轮船外壳装有锌块,是利用了牺牲阳极的阴极保护法。
[答案] B
4.在炼铁、炼钢过程中都有碳参加反应。下列有关碳参加反应的叙述正确的是( )
A.两个过程中碳原子都被氧化,都只起着提供热源的作用
B.炼铁过程中碳被氧化,既起产生热量的作用,又起产生CO的作用
C.炼钢过程中碳被还原,从而达到降低含碳量的目的
D.炼铁过程中碳参加反应,只起产生CO的作用
[解析] 炼铁过程中碳被氧化,既起产生热量的作用,又起产生CO的作用;炼钢过程中碳被氧化,从而达到降低含碳量的目的。
[答案] B
3.下列叙述正确的是( )
①工业上合成非氧化物陶瓷氮化硅(Si3N4)需要在高温、空气气氛中进行
②钢铁制品锈蚀主要是因为钢铁中含有碳而发生原电池反应,因此生铁炼钢时要尽可能完全除去生铁中的碳
③建设三峡大坝需要使用大量水泥,水泥是硅酸盐材料
④夏天人们佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛
⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能
A.①②③ B.②④
C.③④⑤ D.③⑤
[答案] D
2.根据陶瓷的生产原理,可以得出硅酸盐工业的一般特点是( )
①以含硅物质作为原料 ②主要产物是硅酸盐 ③反应条件是高温 ④反应原理是复杂的物理变化和化学变化
A.只有①③ B.只有②③
C.①②③④ D.只有③④
[解析] 陶瓷是利用黏土在高温条件下烧制,得结构致密的多晶烧结体。其生产过程中发生复杂的化学变化和物理变化。故①②③④正确,应选C。
[答案] C
1.下列有关材料的说法不正确的是( )
A.金属材料是指金属及其合金,且合金的性能优于纯金属
B.传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
C.复合材料是由基体和增强体两部分组成的
D.C60也是一种材料
[解析] 新型无机非金属材料的主要成分不是硅酸盐,只有传统无机非金属材料才是硅酸。
[答案] B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com