
题目列表(包括答案和解析)
13.(8分)最近,德国科学家实现了铷原子气体的超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破.已知铷是37号元素,质量数是85.根据材料回答下列问题:
(1)铷位于元素周期表的第________周期第________族.
(2)关于铷的下列说法正确的是________.
①与水反应比钠更剧烈 ②Rb2O在空气中易吸收水和二氧化碳 ③Rb2O2与水能剧烈反应并释放出O2 ④它是极强的还原剂 ⑤RbOH碱性比同浓度NaOH弱
(3)已知RbH+H2O===RbOH+H2↑,则下列叙述正确的是________.
A.氢化铷溶于水显酸性
B.氢化铷与水反应时被还原为氢气
C.氢化铷是离子化合物,其中氢离子最外层有2个电子
D.氢化铷与水反应时,生成1 mol H2将转移2 mol e-
解析:(1)Rb是37号元素,属于碱金属元素,它位于第5周期第ⅠA族;
(2)Rb的结构性质与Na相似,且更活泼,对应的Rb2O,Rb2O2、RbOH的性质分别与Na2O、Na2O2、NaOH相似,所以①②③④正确;
(3)RbH+H2O===RbOH+H2↑,可见反应后溶液为碱性,且H2O作氧化剂,生成1 mol H2转移1 mol e-,C正确.
答案:(1)5 ⅠA
(2)①②③④ (3)C
12.金属K与Na的金属性相近,K与Na盐共熔时,很难将Na从混合物中分离.若调整温度到一定程度,则可用Na与KCl反应制取金属K.已知四种物质的熔、沸点如下:
|
|
K |
Na |
KCl |
NaCl |
|
熔点/℃ |
63.65 |
97.8 |
770 |
801 |
|
沸点/℃ |
774 |
882 |
1500(升华) |
1413 |
根据平衡移动原理,可推知,用Na与KCl反应制K的适宜温度是( )
A.97.8℃-770 ℃ B.770℃-774 ℃
C.774 ℃-882 ℃ D.1413 ℃-1500 ℃
解析:Na+KCl K↑+NaCl,在774 ℃-882℃,钾变成气体逸出使平衡向右移动,且Na与NaCl均未变成气体,所以可以制得K.
K↑+NaCl,在774 ℃-882℃,钾变成气体逸出使平衡向右移动,且Na与NaCl均未变成气体,所以可以制得K.
答案:C
11.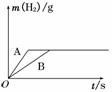 (2011·随州模拟)将一定质量的钠、钾分别投入到装有足量的相同浓度和体积的盐酸的两个烧杯中,产生的气体随时间变化曲线如图所示,则下列说法中正确的是( )
(2011·随州模拟)将一定质量的钠、钾分别投入到装有足量的相同浓度和体积的盐酸的两个烧杯中,产生的气体随时间变化曲线如图所示,则下列说法中正确的是( )
A.投入的Na、K的质量一定相等
B.投入的Na的质量小于K的质量
C.曲线A表示Na与盐酸反应,曲线B表示K与盐酸反应
D.参加反应的HCl的量不一定相等
解析:从图可以看出,Na、K与盐酸反应产生的H2的质量一样多,则消耗的HCl的量一定相符.消耗的Na、K的物质的量一定相等,即投入的Na的质量小于K的质量.K比Na活泼,产生等量H2时,K反应用时较短.故A、C、D选项错误.
答案:B
10.钡的活动性处于钾和钠之间,下列反应可以实现的是( )
A.钡可以从熔融的氯化钾中置换出钾
B.钡可以从氯化钠溶液中置换出钠
C.钡可以从冷水中置换出氢而得到氢气
D.在溶液中钡离子可以氧化金属锌
解析:三种金属的活动性依次为Na<Ba<K,A项错误;三种金属的活泼性较强,都能置换出水中的氢生成氢气,B、D错误.
答案:C
9.由两种金属组成的混合物2 g,投入冷水中充分反应,得到H2 1.12 L(标准状况),则可能的组合是( )
A.Na和Mg B.Rb和Ca
C.K和Na D.Na和Al
解析:Mg不与冷水或碱溶液反应;Na、K、Rb能与冷水反应放出氢气,但要产生1.12 L氢气,所需上述三种金属的质量均大于2 g;Al能与钠和水反应所生成的氢氧化钠溶液反应且产生1.12 L氢气,所需Al的质量为0.9 g.
答案:D
8.碱金属Fr具有放射性,因为不易制得大量单质,对其化学性质没有进行深入研究.根据所学知识推断,下列对Fr的叙述错误的是( )
A.是碱金属中熔点最低的金属
B.0.1 mol/L-1的FrOH溶液与0.1 mol/L的NaOH溶液pH相同
C.Fr在空气中燃烧,生成较复杂的如FrO2一类的氧化物
D.与水反应时,浮在水面上,熔化成闪亮的小球,小球燃烧甚至爆炸
解析:对于碱金属元素的单质,从Li到Cs,熔点依次减小,密度依次增大,但钾反常,密度小于钠,活泼性依次增强,燃烧时生成的氧化物中Li为普通氧化物,Na为过氧化物,K、Cs、Rb为更复杂的氧化物,A、C正确,D不正确,因为Fr的密度比水大,不会浮在水面上.FrOH是强碱,NaOH也是强碱,二者在水溶液中都是完全电离,浓度相同时,溶液pH相同.
答案:D
7.焰火“脚印”、“笑脸”、“五环”使北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关.下列说法中正确的是( )
A.非金属单质燃烧时火焰均为无色
B.所有金属及其化合物灼烧时火焰均有颜色
C.焰色反应均应透过蓝色钴玻璃观察
D.NaCl与Na2CO3灼烧时火焰颜色相同
解析:S在O2中灼烧时产生蓝色火焰,A错误;并不是所有金属元素都存在焰色反应,B错误;只有观察钾元素的焰色反应时需要透过蓝色钴玻璃,C错误;NaCl和Na2CO3的阳离子均为Na+,灼烧时火焰均呈黄色.
答案:D
6.下列关于碱金属与卤素所形成的化合物的性质说法正确的是( )
①大都具有较高的熔、沸点 ②其水溶液都能导电 ③熔融状态都不能导电
A.②③ B.①③
C.①② D.①②③
解析:以NaCl为例判断①、②正确,NaCl熔融状态时存在自由移动的Na+和Cl-,故能够导电.
答案:C
5.试管中装有足量的煤油和水的混合物,静置后投入一小块碱金属.可观察到金属在煤油和水的界面附近上下往复运动.下列说法不正确的是( )
A.此碱金属可能是钾或钠
B.反应一段时间煤油会燃烧
C.碱金属上下运动是由于与水反应产生了氢气
D.若是金属锂则不能观察到上述现象
解析:由题给现象可知,碱金属单质的密度介于煤油和水之间,故可能是钾或钠,若为锂,则浮在煤油上面.碱金属与水接触部分与水反应产生氢气而上浮,脱离水面不再产生氢气而下沉,故上下往复运动,与煤油接触处没有氧气,故不可能燃烧.
答案:B
4.关于铯及其化合物的以下各说法中不正确的是( )
A.氢氧化铯是一种强碱
B.铯与水或酸溶液的反应剧烈,都生成氢气
C.碳酸铯经加热可生成氧化铯和二氧化碳
D.无水硫酸铯的化学式为Cs2SO4
解析:铯的原子半径比钠的更大,对核外电子的束缚力更小,所以铯比钠的金属活动性更强,与水或酸反应生成氢气的强烈程度比钠更高.无水硫酸铯的化学式应与无水硫酸钠的化学式相似.钠或其他碱金属的碳酸正盐加热时不易分解.
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com