
题目列表(包括答案和解析)
6.关于药品的取用有下列说法:①实验中剩余的药品要放回原试剂瓶,以免浪费;②实验中剩余的药品应该扔掉;③实验中剩余的药品要倒入废液桶中;④剩余的固体应放回原试剂瓶,液体应倒入废液桶中。其中不正确的是( )
A.① B.②
C.①② D.全部
[解析] 实验中剩余的药品一般既不能放回原瓶,也不能随意丢弃,更不能带出实验室,应放在指定容器中。
[答案] D
5.如图分别表示四种操作,其中至少有两处错误的是( )
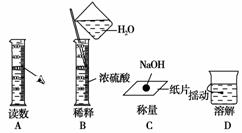
[解析] 量筒读数时应平视,A项有1处错误;B项有两处错误:①不应将H2O加入浓H2SO4中,②不应在量筒中稀释浓H2SO4;C项1处错误,不能用纸片称取NaOH;D项有1处错误,应用玻璃棒搅拌加速溶解。
[答案] B
4.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流。下列有关实验过程中,一般不需要使用玻璃棒进行操作的是( )
①用pH试纸测定Na2CO3溶液的pH ②从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl ③实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀 ④用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验 ⑤将适量氯化铁饱和溶液滴入沸水中制氢氧化铁胶体 ⑥用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验 ⑦探究Ba(OH)2·8H2O晶体和NH4C1晶体反应过程中的能量变化
A.②③⑦ B.③④⑤
C.⑤⑥⑦ D.④⑥⑦
[解析] ①需要用玻璃棒蘸取待测液;②需要玻璃棒搅拌以加速固体的溶解,过滤时需要玻璃棒引流;⑥需要用玻璃棒不断搅拌混合物;⑦需要用玻璃棒搅拌固体混合物。
[答案] B
3.下列实验仪器在实验前,应特别注意是否漏液的是( )
①碱式滴定管,②普通漏斗,③分液漏斗,④蒸馏烧瓶,⑤容量瓶,⑥酸式滴定管。
A.③⑤⑥ B.①③⑤⑥
C.①③④⑤⑥ D.①②③④⑤⑥
[解析] 带有活塞的容器,玻璃接口处易于漏水,使用前必须进行检验操作。
[答案] B
2.准确量取25.00 mL高锰酸钾溶液,可选用的仪器是( )
A.30 mL量筒 B.10 mL量筒
C.30 mL酸式滴定管 D.50 mL碱式滴定管
[解析] 量筒为粗量仪器,只能粗量至0.1 mL,所以A、B不可选,KMnO4溶液有强氧化性腐蚀作用,不能用碱式滴定管。
[答案] C
1.下列仪器:①漏斗,②容量瓶,③蒸馏烧瓶,④天平,⑤分液漏斗,⑥滴定管,⑦燃烧匙。常用于分离物质的仪器是( )
A.①③④ B.①②⑥
C.①③⑤ D.③④⑦
[解析] 常用于分离的装置不能选用②④⑥⑦。
[答案] C
16.(14分)氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域。某不合格氮化铝产品,据合成路线推断杂质可能是碳或氧化铝。现用如下图中装置来进行检验,使氮化铝样品和NaOH溶液反应AlN+NaOH+H2O===NaAlO2+NH3↑,根据反应中所生成氨气的质量来测定样品中氮化铝的质量分数,并根据实验现象来确定杂质的成分。
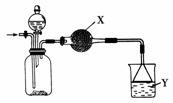
(1)实验操作有:
a.往广口瓶中放入少量的AlN样品
b.从分液漏斗往广口瓶中加入稍过量的NaOH溶液
c.检验装置的气密性
d.测定收集到氨气的质量
e.鼓入空气
正确的操作顺序为________(以字母进行排序)。
(2)①干燥管中X试剂是________(填字母序号)。
A.CaCl2 B.P2O5
C.碱石灰
②烧杯中Y试剂是________(与上同)。
A.稀硫酸 B.苯
C.NaOH溶液
(3)若不鼓入空气,实验测得NH3质量将________(填“偏大”、“偏小”或“不变”)。
(4)实验结束后广口瓶只有无色溶液,则含有杂质是______。
(5)若实验中测得样品的质量为w g,氨气的质量为m g,则样品中AlN的质量分数为________。
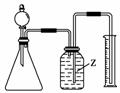
(6)若测量NH3的体积可采用右图所示装置,广口瓶中Z液体是 。
A.水
B.植物油与水
C.CCl4与水
[解析] 本题考查气体的定性定量测定。根据检验探究目的要求推断。
(1)实验操作依据气体制备方法推断顺序应为c→a→b→e→d。
(2)①能干燥NH3的干燥剂只能为碱石灰,NH3可与P2O5和CaCl2反应;②对NH3吸收效果最好为稀硫酸。
(3)若不鼓入空气,有部分NH3残留在装置中,使NH3测定结果偏低。
(4)若含有碳,有残留固体;若有氧化铝只有无色溶液。
(5)由于AlN-NH3
n(AlN)=n(NH3)= mol
a(AlN)=×100%=×100%。
(6)由于NH3极易溶于水,NH3不能直接接触水,可用其他液体隔开,不溶于水且密度小于水的液体符合要求,故应选植物油与水。
[答案] (1)c→a→b→e→d (2)①C ②A
(3)偏小 (4)氧化铝 (5)×100% (6)B
15.(12分)(2009年上海高考稍改动)根据硫化氢气体的实验室制法和性质完成下列填空。
(1)若用启普发生器制取硫化氢气体,则制取气体的原料可选用________。
a.稀硫酸与硫化亚铁 b.稀硝酸与硫化亚铁
c.稀硫酸与硫化钠 d.稀盐酸与硫化亚铁
(2)现要组装一套可以控制硫化氢气体产生速率的装置,请在下图中选择合适的仪器:________(填编号)。
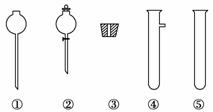
(3)点燃不纯的硫化氢气体可能会生爆炸,为了防止意外,可连接一个安全装置。下图的装置能起到此作用的是____________。
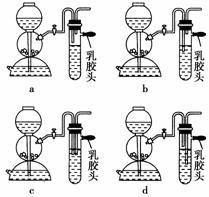
[解析] (1)用启普发生器制取气体,要求反应物是块状固体与液体。HNO3具有强氧化性,与FeS反应不能生成H2S,故答案为a、d。
(2)通过分液漏斗控制酸的滴速来控制反应速率。
(3)安全装置的连接方式是长进短出。
[答案] (1)a、d (2)②③④ (3)b
14.(12分)已知六种白色粉末分别是KNO3、(NH4)2SO4、Al2O3、MgCl2、Ba(OH)2、无水CuSO4中的一种。除蒸馏水外不得使用任何其他试剂对这些物质进行鉴别,并按要求填写下列空白。
(1)待测物+--
实验现象:________________________________________。
被检出物质的化学式:____________。
(2)待测物+--
实验现象:____________。
被检出物质的化学式:____________。
(3)待测物+--
实验现象:__________________________________________________________________________________________________。
被检出物质的化学式:________________________________________________________________________。
[解析] 用蒸馏水可将CuSO4(溶解后溶液呈蓝色)、Al2O3(不溶于水)检出,然后再用已检出的物质作试剂鉴别其余的物质。可与CuSO4溶液反应得淡蓝色沉淀的为Ba(OH)2溶液;可与Ba(OH)2溶液反应只得白色沉淀为MgCl2;既得白色沉淀又有气体放出的为(NH4)2SO4。
[答案] (1)蒸馏水 一种是蓝色溶液;一种不溶于水
CuSO4 Al2O3
(2)CuSO4溶液 蓝色沉淀 Ba(OH)2
(3)Ba(OH)2溶液 白色沉淀;有刺激性气味气体和白色沉淀;无明显现象 MgCl2;(NH4)2SO4;KNO3
27.4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com