
题目列表(包括答案和解析)
2.“纳米材料”(1 nm=10-9 m)是指研究开发直径为几纳米至几十纳米的材料。如将“纳米材料”分散到某液体中,对于所得分散系的叙述不正确的是( )
A.光速通过此分散系时会形成一条光亮的“通路”
B.此分散系中“纳米材料”的粒子在做不停的、无序的运动
C.在外加电场作用下,“纳米材料”的粒子可能向电极做定向运动
D.用滤纸过滤的方法可以从此分散系中分离得到该“纳米材料”
[解析] 由于“纳米材料”的粒子直径是几纳米至几十纳米,即其直径大小在胶体粒子直径的范围内,所以将其分散到某液体中时形成的分散系是胶体,因而也就具有胶体的性质,如丁达尔效应、胶体的电泳以及能透过滤纸等性质,而布朗运动是粒子做无规则运动,胶体、溶液等都有此性质。
[答案] D
1.苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象的发生,这说明维生素C具有( )
A.氧化性 B.还原性
C.碱性 D.酸性
[解析] 现榨的苹果汁在空气中由淡绿色变成棕黄色,说明Fe2+→Fe3+发生了氧化反应。加入维生素C可有效防止这种现象发生,证明维生素C具有还原性,故选B。
[答案] B
0.075 mol 0.15 mol 0.15 mol
所以x=2,y=4,即分子式为C2H4。
[答案] (1)2.7 g (2)C2H4
17.标准状况下1.68 L某气态烃在足量氧气中完全燃烧。若将产物通入足量澄清石灰水中,得到白色沉淀的质量为15.0 g;若用足量碱石灰吸收燃烧产物,增重9.3 g。求:
(1)燃烧产物中水的质量。
(2)通过计算确定该气态烃的分子式。
[解析] 燃烧产物通入澄清石灰水中,得白色沉淀的质量为15.0 g,则n(CaCO3)=n(C)=n(CO2)==0.15 mol,m(CO2)=0.15 mol×44 g·mol-1=6.6 g。
所以碱石灰吸收的水的质量为m(H2O)=9.3 g-6.6 g=2.7 g
n(H2O)==0.15 mol
标准状况下1.68 L的气态烃物质的量为
=0.075 mol
CxHy - xCO2 - H2O
1 x
16.苯是一种重要的化工原料,以下是用苯作为原料制备某些化合物的转化关系图:

已知:①
②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。
(1)A是一种密度比水________(填“小”或“大”)的无色液体;A转化为B的化学方程式是________________________________________________________________________。
(2)在“ ”的反应中属于取代反应的是________,属于加成反应的是________(填字母)。
”的反应中属于取代反应的是________,属于加成反应的是________(填字母)。
[答案] 
(2)ab c
15.某化学课外小组用如图装置制取溴苯。

先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A中(A下端活塞关闭)。
(1)写出A中反应的化学方程式:________________________________________________________________________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 。
写出有关的化学方程式:________________________________________________________________________。
(3)C中盛放CCl4的作用是________________________________________________________________________。
[解析] A中的反应为3Br2+2Fe===2FeBr3

在制备的溴苯中常混有溴,一般加入NaOH溶液中,因发生反应:Br2+2NaOH===NaBr+NaBrO+H2O而除去。HBr中混有的溴蒸气在经过CCl4时被吸收。
[答案]
(1) 
(2)除去溶于溴苯中的溴
Br2+2NaOH===NaBr+NaBrO+H2O
(3)除去溴化氢气体中的溴蒸气
14.实验探究:通过实验事实的验证与讨论,认识苯的结构式。
提出问题:苯分子结构是碳碳单键、双键交替的环状结构吗?
(1)提出假设:从苯的分子式看,C6H6具有不饱和性;从苯的结构式 看,分子中含有碳碳双键,所以,苯一定能使________褪色。
看,分子中含有碳碳双键,所以,苯一定能使________褪色。
(2)实验验证
①苯不能使________褪色。
②经科学测定,苯分子里6个碳原子之间的键________(填“相同”或“不相同”);6个碳原子和6个氢原子都在同一________上。
(3)结论:苯的凯库勒结构式中的双键跟烯烃中的双键______,苯的性质没有表现出不饱和性,反而结构稳定,说明苯分子________一般的碳碳单、双键交替的环状结构(填“同于”或“不同于”)。
(4)应用:为了表示苯分子的结构特点,结构简式用________表示,用 表示苯分子的结构是不确切的。
表示苯分子的结构是不确切的。
[解析] 苯分子若是单、双键交替结构,则一定具有碳碳双键的特征反应:与溴水发生加成反应或使KMnO4溶液褪色,但实际上均不能和二者发生反应,可说明苯分子中的碳碳键比较特殊。
[答案] (1)溴水(或酸性KMnO4溶液)
(2)①溴水(或酸性KMnO4溶液) ②相同 平面
(3)不同 不同于 (4) 
13.

“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如右图所示:
(1)立方烷的分子式为 。
(2)该立方烷的二氯代物具有同分异构体的数目是 。
[解析] (1)立方体为一对称结构,有8个顶点,每个顶点为1个碳原子,这个碳原子和相邻的3个顶点上的碳原子以共价键结合。碳原子有4个价电子,所以每个碳原子还能再和1个氢原子相结合,故立方烷的分子式为C8H8。
(2)该烃的二氯代物的氯原子可以:①占据同一边上的两个顶点;②同一平面对角线的两个顶点;③立方体的对角线的两个顶点,所以共有3种同分异构体。
[答案] (1)C8H8 (2)3
12.
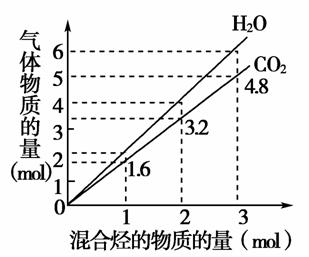
100 ℃时,两种烃蒸气组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃的总物质的量变化如图所示。则下列对该混合烃组成的判断正确的是( )
A.一定含有甲烷
B.一定含有乙烯
C.一定含有苯
D.一定不含乙烯
[解析] 由图象中的线性关系,选取混合烃的总物质的量为1 mol作研究,生成的CO2和H2O的物质的量分别为1.6 mol和2 mol,故其平均分子组成为C1.6H4,由于碳原子数小于1.6的烃只有甲烷一种,因此一定含有甲烷。CH4分子中含4个氢原子,故另一种分子中一定含4个氢原子,且其碳原子数大于1.6,故可能是乙烯,一定不含有苯。
[答案] A
11.两种气态烃的混合气体共1 L,在空气中燃烧生成1.5 L CO2气体和2 L水蒸气(气体体积均在相同状况下测定),关于该混合气体的说法不正确的是( )
A.一定含有甲烷
B.可能有乙烯
C.一定含有乙烷,不一定含有甲烷
D.一定不含有乙烷
[解析] 设平均分子式为CxHy
CxHy - xCO2 - H2O
1 x
1 L 1.5 L 2 L
x=1.5 y=4
所以C1.5H4即按碳原子个数进行十字交叉判断必有CH4,另一种烃一个分子中也必定有4个氢原子。
[答案] C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com