
题目列表(包括答案和解析)
2.52 g 0.28 g 0.28 mol
m(CO2)- m(C)- n(C)
16.(12分)为了测定一种气态烃A的分子式,取一定量的A置于密闭容器中燃烧,定性实验表明产物是CO2、CO和水蒸气。学生甲、乙设计了如下两个方案,均认为根据自己的方案能求出A的最简式。他们测得的有关数据如下(图中的箭头表示气体的流向,实验前系统内的空气已排尽):
甲: 乙:
乙: 试回答:
试回答:
(1)根据甲、乙两方案,你认为能否求出A的最简式?
(2)请根据你选择的方案,通过计算求出A的最简式。
(3)若要确定A的分子式,是否还需要测定其他数据?并说明原因。
[解析] (1)甲:因其能分别求得A燃烧的产物CO、CO2和H2O(g)的质量各是多少,进一步可求出A中C和H的原子个数比,即得A的最简式。乙中通过碱石灰增重5.60 g是CO2、H2O的总质量,无法求m(CO2)、m(H2O),从而无法求出A的最简式。
(2)m(H2O)- m(H)- n(H)
15.(15分)某课外小组设计的实验室制取乙酸乙酯的装置如下图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液。

已知:①无水氯化钙可与乙醇形成难溶于水的
CaCl2·6C2H5OH;②有关有机物的沸点如下:
请回答:
(1)浓硫酸的作用是的__________________________________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:__________________________。
(2)球形干燥管C的作用是________________。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示)______________________________;反应结束后D中的现象是____________________________________________________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出________,再加入________(此空从下列选项中选择),然后进行蒸馏,收集77 ℃左右的馏分,以得到较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰
C.无水硫酸钠 D.生石灰
[解析] (1)酯化反应的机理是酸脱羟基,醇脱氢,若乙醇中的氧为18O,则酯中主链上的氧也应为18O。
(2)饱和Na2CO3溶液吸收挥发出来的乙酸,pH值降低,故溶液颜色变浅,而乙酸乙酯不溶于饱和Na2CO3溶液,故分层。
(3)根据题给信息“①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH”说明加入无水氯化钙可除去乙醇。蒸馏中加入的成分,既要考虑能吸收水,又要与乙酸乙酯不反应,因无机酸碱会催化酯的水解,故选C。
[答案] (1)制乙酸乙酯的催化剂、吸水剂(或干燥剂)
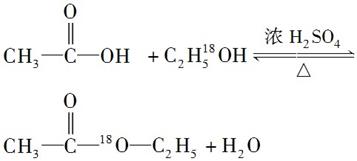
(2)冷凝蒸气,防止倒吸 溶液分层,上层为无色油状液体,下层溶液颜色变浅
溶液分层,上层为无色油状液体,下层溶液颜色变浅
(3)乙醇 C
14.(15分)(1)苯、四氯化碳、乙醇、汽油是常见的有机溶剂,能与水互溶的是________;不溶于水,且密度比水小的是________。
(2)一瓶无色气体,可能含有CH4和CH2===CH2或其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有少量无色油状小液滴。
①由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确,为什么?__________________________________________________________________________________________。
②上述实验可能涉及的反应类型有______________________。
(3)含有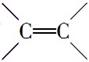 的化合物与CH2===CH2一样,在一定条件下可聚合成高分子化合物。
的化合物与CH2===CH2一样,在一定条件下可聚合成高分子化合物。
①广泛用作农用薄膜的聚氯乙烯塑料,是由CH2CHCl聚合而成的,其化学反应方程式是________________________________________________________________________。
②电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯(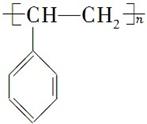 ),它是由________________(写结构简式)聚合而成的。
),它是由________________(写结构简式)聚合而成的。
[解析] (1)乙醇和水互溶,其余三种有机物都不溶于水,其中四氯化碳的密度比水大,苯和汽油的密度都比水小。(2)CH4和Cl2在光照条件下发生取代反应,而使黄绿色逐渐褪去,生成的CH3Cl、CH2Cl2、CHCl3都是油状液体;而CH2CH2可以与Cl2发生加成反应,而使黄绿色逐渐褪去,生成的CH2ClCH2Cl也是油状液体。所以不能确定该瓶气体中是否含有CH4。(3)氯乙烯发生加聚反应生成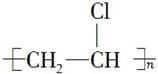 ,而
,而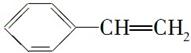 发生加聚反应生成聚苯乙烯。
发生加聚反应生成聚苯乙烯。
[答案] (1)乙醇 苯、汽油
(2)①不正确,因为CH2===CH2也可以与Cl2发生加成反应,而使黄绿色逐渐褪去,生成的CH2ClCH2Cl也是油状液体
②取代反应、加成反应
(3)①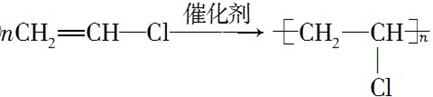 ②
②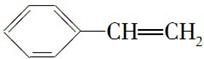
13.(10分)为了提纯下表所列物质(括号内为杂质),请把除杂试剂和分离方法填入相应的表格中。
 [解析] 除去丙烷中的丙烯可将混合气体通过溴水,丙烯被吸收而除去;除去乙醇中的乙酸可通过乙酸与生石灰反应生成醋酸钙,同时生石灰也可吸收水,然后通过蒸馏得到无水乙醇;除去苯中的溴,可利用溴与NaOH溶液反应生成易溶于水的NaBr、NaBrO,然后通过分液而除去;除去乙烯中的CO2、SO2气体,可使用NaOH溶液吸收SO2、CO2,通过洗气除去;除去CO2中SO2,用饱和NaHCO3溶液吸收SO2,通过洗气除去SO2。
[解析] 除去丙烷中的丙烯可将混合气体通过溴水,丙烯被吸收而除去;除去乙醇中的乙酸可通过乙酸与生石灰反应生成醋酸钙,同时生石灰也可吸收水,然后通过蒸馏得到无水乙醇;除去苯中的溴,可利用溴与NaOH溶液反应生成易溶于水的NaBr、NaBrO,然后通过分液而除去;除去乙烯中的CO2、SO2气体,可使用NaOH溶液吸收SO2、CO2,通过洗气除去;除去CO2中SO2,用饱和NaHCO3溶液吸收SO2,通过洗气除去SO2。
[答案]
|
序号 |
除杂试剂 |
分离方法 |
|
1 |
溴水 |
洗气 |
|
2 |
CaO(生石灰) |
蒸馏 |
|
3 |
NaOH溶液 |
分液 |
|
4 |
NaOH溶液 |
洗气 |
|
5 |
饱和NaHCO3溶液 |
洗气 |
12.含有一个羟基的化合物A 10 g,与乙酸反应生成乙酸某酯11.85 g,并回收了未反应的A 1.3 g,则A的相对分子质量约为( )
A.98 B.116
C.158 D.278
[解析] 设A的相对分子质量为M,
R-OH+CH3COOH―→CH3COOR+H2O
M M+42
10 g-1.3 g 11.85 g
=,解得M=116。
[答案] B
11.下列叙述中正确的是( )
A.除去乙酸乙酯中的乙酸,可加入氢氧化钠溶液然后分液除去杂质
B.糖类、油脂、蛋白质是基本营养物质,都能发生水解反应
C.除去乙烷中少量的乙烯可在光照条件下通入Cl2,然后进行气液分离
D.苯、乙醇和乙酸都能发生取代反应
[解析] 乙酸乙酯在NaOH溶液中易发生水解,不能用它除去乙酸杂质,A项错误;糖类中的单糖不能发生水解反应,B项错误;除去乙烷中的乙烯需用溴水,C项错误。
[答案] D
10.下列各组物质不属于同分异构体的是( )
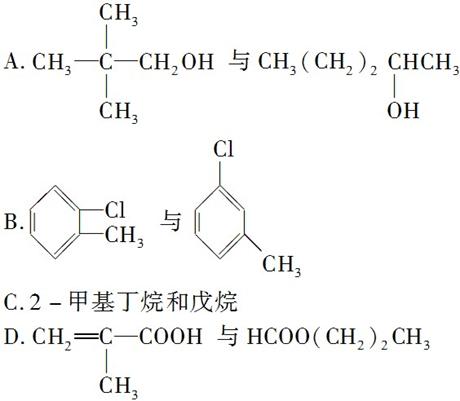
[解析] D项两者的分子式分别为C4H6O2、C4H8O2,它们不属于同分异构体。
[答案] D
9.下列说法中不正确的是( )
①利用葡萄糖的特征反应检查尿液中是否含有尿糖;②乙醇、乙烯、葡萄糖都能使KMnO4酸性溶液褪色;③蔗糖与麦芽糖的水解产物相同;④可以用KIO3与新制氢氧化铜悬浊液检验淀粉水解的程度;⑤等物质的量的CH3COOH分别与足量的C2H516OH与C2H518OH反应,生成的水的质量不相等;⑥苯的硝化反应、C2H4与溴水反应、乙酸与乙醇反应都属于取代反应。
A.①②③④ B.②③④⑤
C.③④⑤⑥ D.③④⑤
[解析] 蔗糖水解得到葡萄糖和果糖,麦芽糖水解只得到葡萄糖,③说法错误;要用I2检验淀粉存在,④说法错误;根据酯化反应规律-COOH脱-OH,-OH脱-H,所以生成的产物都含有H2O,质量相等,⑤说法错误;C2H4与溴水发生加成反应,⑥说法错误。
[答案] C
8.下列说法中,错误的是( )
A.无论是乙烯的加成,还是乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关
B.使用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.使用溴的四氯化碳溶液或酸性KMnO4溶液都可以除去乙烷中混有的乙烯
D.乙烯的化学性质比乙烷的化学性质活泼
[解析] 乙烷不与Br2的CCl4溶液或酸性KMnO4溶液反应,乙烯与溴的CCl4溶液中的Br2发生加成反应,因此可以除去C2H6中的C2H4;而乙烯被KMnO4酸性溶液氧化为CO2;故不能用KMnO4溶液除去C2H6中的C2H4。
[答案] C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com