
题目列表(包括答案和解析)
2.下列关于乙炔性质的叙述中,既不同于乙烯又不同于乙烷的是
( )
A.能燃烧生成二氧化碳和水
B.能发生加成反应
C.能与高锰酸钾溶液发生氧化反应
D.能与氯化氢反应生成氯乙烯
[解析] C2H2、C2H4、C2H6均能燃烧(生成CO2和H2O),C2H2和C2H4均能发生加成反应,均能与KMnO4发生氧化反应。C2H6不与HCl反应,C2H4与HCl反应生成C2H5Cl(氯乙烷),只有C2H2与HCl反应生成CH2=CHCl(氯乙烯)。
[答案] D
1.下列物质不能使KMnO4酸性溶液褪色的是
( )
A.丙烷 B.乙烯
C.乙苯 D.二氧化硫
[解析] 乙烯和乙苯能被KMnO4酸性溶液氧化,SO2具有还原性,能与具有强氧化性的KMnO4酸性溶液反应;丙烷不与KMnO4酸性溶液反应。
[答案] A
14.(2008年江苏)“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有________。(填字母)
a.减少化石燃料的使用 b.植树造林,增大植被面积
c.采用节能技术 d.利用太阳能、风能
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2+6H2OC6H12O6+6O2
b.CO2+3H2催化剂△CH3OH+H2O
c.CO2+CH4催化剂△CH3COOH
d.2CO2+6H2催化剂△H2CCH2+4H2O
以上反应中,最节能的是________,原子利用率最高的是________。(填字母)
(3)文献报道某课题组利用CO2催化氢化制甲烷的研究过程如下:

反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4。CH4、HCOOH、H2的产量和镍粉用量的关系如下图所示(仅改变镍粉用量,其他条件不变):

研究人员根据实验结果得出结论:
HCOOH是CO2转化为CH4的中间体,即CO2HCOOHCH4
①写出产生H2的反应方程式:_____________________________________________。
②由图可推知,镍粉是________。(填字母)
a.反应Ⅰ的催化剂 b.反应Ⅱ的催化剂
c.反应Ⅰ、Ⅱ的催化剂 d.不是催化剂
③当镍粉用量从1 mmol增加到10 mmol,反应速率的变化情况是________。(填字母)
a.反应Ⅰ的速率增加,反应Ⅱ的速率不变
b.反应Ⅰ的速率不变,反应Ⅱ的速率增加
c.反应Ⅰ、Ⅱ的速率均不变
d.反应Ⅰ、Ⅱ的速率均增加,且反应Ⅰ的速率增加得快
e.反应Ⅰ、Ⅱ的速率均增加,且反应Ⅱ的速率增加得快
f.反应Ⅰ的速率减小,反应Ⅱ的速率增加
[解析] 本题从温室效应展开,讨论控制和治理CO2的一些有效途径。(1)由于减少化石燃料的使用,采用节能技术和开发利用太阳能、风能等,均可减少CO2的排放,植物的光合作用会消耗CO2,所以植树造林,增大植被面积可降低大气中CO2浓度,故可选abcd;(2)最节能的应该是常温常压下进行的反应,原子利用率最高的反应,应该是化合反应,所以答案分别为a和c;(3)①根据流程图信息,产生H2的反应应是Fe和水蒸气,故反应式为:3Fe+4H2O(g)Fe3O4+4H2;②根据曲线图信息,镍粉用量对CH4、H2和HCOOH的产量都产生影响,且最后仍检测到镍粉,所以镍粉应该是反应Ⅰ、Ⅱ的催化剂;③镍粉从1 mmol增加到10 mmol的过程中,图示表明速率均增大,但甲烷和氢气变化不大,甲酸变化较大,所以选e。
[答案] (1)abcd (2)a c (3)①3Fe+4H2O(g)Fe3O4+4H2 ②c ③e
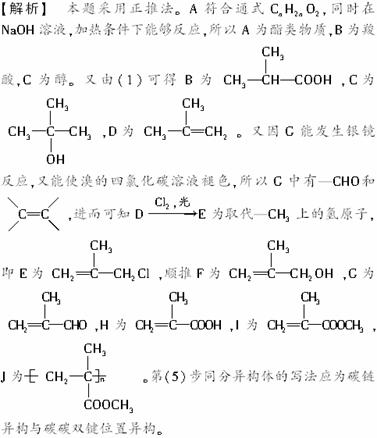
13.(2008年全国Ⅱ理综)A、B、C、D、E、F、G、H、I、J均为有机化合物。根据以下框图,回答问题:

(1)B和C均为有支链的有机化合物,B的结构简式为__________________;C在浓硫酸作用下加热反应只能生成一种烯烃D,D的结构简式为________________;
(2)G能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式为____________;
(3)⑤的化学方程式是_______________________________________________________;
⑨的化学方程式是_________________________________________________________;
(4)①的反应类型是____________;④的反应类型是____________;⑦的反应类型是______________;
(5)与H具有相同官能团的H的同分异构体的结构简式为
________________________________________________________________________。
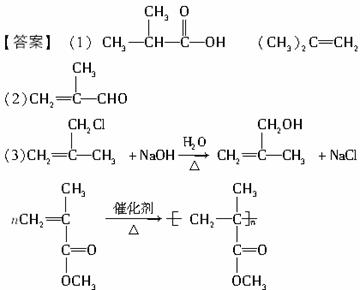
12.(2007年吉林)实验测得A、B、C三种有机物的相对分子质量均为72。
(1)已知A中只含C、H两种元素,且质量比为5∶1,则其分子式为________,它有________种同分异构体,在它的同分异构体中,沸点最高的是______________________(写结构简式);一氯代物只有一种的是__________________(写名称)。
(2)已知B是烃的含氧衍生物,分子中只有一个官能团,且能发生银镜反应。请写出B可能的结构简式为________________________。
(3)C能发生如下变化
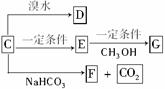
已知E和G都是高分子化合物,其中G是一种重要的有机合成材料。请按要求填空:
①C的结构简式为___________________________________________________。
②E→G的化学方程式为______________________________________________。
此反应类型为_______________________________________________________。
[解析] (1)A分子中C原子数为72××=5,H原子数为12,A的分子式为C5H12,沸点最高的是正戊烷。
(2)B中只有-CHO,应为饱和一元醛,符合CnH2nO的通式,将相对分子质量代入解得分子式为C4H8O,有两种可能结构。
(3)C能与溴水反应,含不饱和碳碳键,能与NaHCO3反应放出CO2分子结构中有-COOH,可推知为CH2===CHCOOH。
[答案] (1)C5H12 3 CH3CH2CH2CH2CH3 新戊烷或2,2二甲基丙烷
(2)CH3CH2CH2CHO (CH3)2CHCHO
(3)①CH2===CHCOOH
② ?酯化反应或取代反应
?酯化反应或取代反应
11.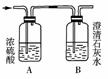 如右图所示某气体X可能由H2、CO、CH4中的一种或几种组成,将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶。试回答下列问题:
如右图所示某气体X可能由H2、CO、CH4中的一种或几种组成,将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶。试回答下列问题:
(1)若A洗气瓶的质量增加,B洗气瓶的质量不变,则气体X是________。
(2)若A洗气瓶的质量不变,B洗气瓶的质量增加,则气体X是__________。
(3)若A、B两个洗气瓶的质量都增加,则气体X可能是
________________________________________________________________________。
[解析] 此题主要考查根据洗气瓶中质量的变化,确定原气体X的成分。
由2H2+O22H2O,2CO+O22CO2,
CH4+2O2CO2+2H2O
浓H2SO4吸收水,石灰水吸收CO2得
(1)若A瓶质量增加,B瓶质量不变,说明气体X燃烧只生成水,故X为H2。
(2)若A瓶质量不变,B瓶质量增加,说明气体X燃烧只有CO2生成,故X为CO。
(3)若A、B两瓶质量增加,说明气体X燃烧产物既有H2O又有CO2,故X气体为不确定成分。它可以是CH4或下列组合:H2、CO;H2、CH4;CO、CH4;H2、CO、CH4。
[答案] (1)H2 (2)CO (3)CH4或H2、CO或H2、CH4或CO、CH4或H2、CO、CH4
10.从理论上分析,碳原子数为10或小于10的烷烃分子中,其一卤代物不存在同分异构体的烷烃分子共有的种类是
( )
A.2种 B.3种
C.4种 D.5种
[解析] 最简单的烷烃是甲烷,若烷烃的一卤代物不存在同分异构体,则烷烃分子中所有的氢原子在空间的位置完全等同,这样的烷烃显然有CH4、CH3CH3。按照氢原子在空间位置等同原则,有下列变换过程:
CH4(甲烷) 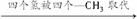 C(CH3)4,分子式为C5H12;
C(CH3)4,分子式为C5H12;
CH3CH3(乙烷)  C(CH3)3C(CH3)3
C(CH3)3C(CH3)3
分子式为C8H18,由题给条件限定碳原子为10或小于10。可得答案为C。
[答案] C
9.2005年1月,欧洲航天局的惠更斯号探测器首次成功登陆土星的最大卫星--土卫六。科学家对探测器发回的数据进行了分析,发现土卫六的大气层中含有95%的氮气,剩余的气体为甲烷和其他碳氢化合物。下列关于碳氢化合物的叙述正确的是
( )
A.碳氢化合物的通式为CnH2n+2
B.石油的主要成分是碳氢化合物
C.乙炔是含碳量最高的碳氢化合物
D.碳氢化合物中的化学键都是极性键
[解析] 碳氢化合物(烃)有多种,通式为CnH2n+2的只是其中的烷烃。石油主要是由各种烷烃、环烷烃和芳香烃的混合物。烃分子中例如C10H8的含碳量高于乙炔(C2H2)。烃分子中C-C是非极性键。所以A、C、D错误,答案选B。
[答案] B
8.一些烷烃的燃烧热(kJ·mol-1)如下表:
|
化合物 |
燃烧热 |
化合物 |
燃烧热 |
|
甲烷 |
891.0 |
正丁烷 |
2 878.0 |
|
乙烷 |
1 560.8 |
异丁烷 |
2 869.6 |
|
丙烷 |
2 221.5 |
2甲基丁烷 |
3 531.3 |
下列表达正确的是
( )
A.热稳定性:正丁烷>异丁烷
B.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)===4CO2(g)+6H2O(g);ΔH=-1 560.8 kJ·mol-1
C.正戊烷的燃烧热大约在3 540 kJ·mol-1左右
D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
[解析] 对A项,从正丁烷和异丁烷的燃烧热可以看出,正丁烷的能量状态高于异丁烷,故其稳定性不如异丁烷。B项中出现两处错误水应为液态,ΔH与系数不匹配。对D项,经计算不对。
[答案] C
7.金刚烷的结构如右图所示,它可看做是由四个等同的六元环组成的空间构型。请根据中学学过的异构现象判断由氯原子取代金刚烷中的亚甲基(-CH2-)中的氢原子所形成的二氯代物的种类
( )

A.4种 B.3种
C.2种 D.5种
[答案] B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com