
题目列表(包括答案和解析)
10.CuS和Cu2S都能溶于硝酸,它们高温灼烧的产物相同。以下鉴别CuS和Cu2S两种黑色粉末的方法合理的是 ( )
A.将两种样品分别溶于硝酸,区别所产生的气体
B.将两种样品分别溶于硝酸,区别溶液的颜色
C.取两种同质量的样品分别在高温下灼烧,区别残留固体的质量
D.取两种同质量的样品分别在高温下灼烧,区别残留固体的颜色
[解析] 两种样品分别溶于硝酸,生成的产物相同,如:
3CuS+8HNO3(稀)3Cu(NO3)2+2S↓+2NO↑+4H2O
3Cu2S+16HNO3(稀)6Cu(NO3)2+3S↓+4NO↑+8H2O
因此,用区别溶液的颜色或区别所产生的气体不能鉴别CuS和Cu2S,选项A、B均不合理。等质量的CuS和Cu2S分别在高温下灼烧都生成CuO和SO2,但质量变化不同,CuS灼烧后质量减小,Cu2S灼烧后残留固体质量不变,故C对,D错。
[答案] C
9.只用水就能鉴别的一组物质是 ( )
A.苯、乙酸、四氯化碳 B.乙醇、乙醛、乙酸
C.乙醛、乙二醇、硝基苯 D.苯酚、乙醇、甘油
[解析] 选项A是利用三种有机物的溶解性和密度大小加以区分,苯难溶于水比水轻,乙酸能溶于水,四氯化碳难溶于水但比水重。选项B中乙醇、乙醛、乙酸均能溶于水,难以区分;选项C中乙醛、乙二醇和选项D中乙醇、甘油皆能溶于水,无法区分。
[答案] A
8.某溶液含有较多的Na2SO4和少量的Fe2(SO4)3,若用该溶液制取芒硝,可供选择的操作如下,正确的操作步骤是 ( )
①加适量H2SO4溶液 ②加金属Na ③结晶 ④加过量NaOH溶液 ⑤加强热脱结晶水 ⑥过滤
A.②⑥③ B.④⑥①③
C.④⑥③② D.②⑥①③⑤
[解析] 一种盐溶液精制的过程,不可能用金属钠;芒硝的化学式是Na2SO4·10H2O,不能加热脱去结晶水。由此可见,凡是涉及到②、⑤两个操作步骤的选项都是不正确的选项。
[答案] B
7.下列除杂质的方法不可行的是 ( )
A.用过量氨水除去Al3+溶液中的少量Fe3+
B.将混合气体通过灼热的铜网除去N2中的少量O2
C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水
D.用盐酸除去AgCl中少量的Ag2CO3
[解析] A项中Al3+、Fe3+与氨水反应生成Al(OH)3、Fe(OH)3沉淀二者都不溶于氨水,所以过量的氨水不能用来除去Al3+溶液中的Fe3+。B项由于2Cu+O22CuO,而Cu与N2不反应,故可以除去O2。C项除去乙醇中的少量水比较特殊,要加新制的生石灰,目的是吸收水,CaO+H2O===Ca(OH)2,蒸馏得到无水乙醇。D项Ag2CO3+2HCl===2AgCl+H2O+CO2↑,所以可行。本题既有除杂质离子、杂质气体,又有特殊的蒸馏,还有杂质转化为目的的物质。是多角度考查除杂原理的题目,需要同学们对除杂的基本要求、原理透彻掌握。
[答案] A
6.为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性气味、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。
根据实验以下推测正确的是 ( )
A.一定有SO
B.一定有CO
C.不能确定Cl-是否存在
D.不能确定HCO是否存在
[解析] 由实验①知,该溶液中不含有与OH-反应的弱碱阳离子和弱酸的酸式酸根离子等,排除D选项;由实验②可知溶液中一定含有CO,而一定不含SO或HSO,由实验③知溶液中一定含有SO,由实验④和③中所得溶液中含有Cl-,可能是原溶液中含有的,也可能不是(因②中加入了HCl),故本题答案为B、C。
[答案] BC
5.关于某无色溶液中所含离子的鉴别,下列判断正确的是 ( )
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在
B.通入Cl2后,溶液变为棕黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在
C.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有SO存在
D.加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO存在
[解析] Cl-、SO均能与Ag+形成不溶于稀盐酸的白色沉淀,A错;I2遇淀粉变蓝,通入Cl2后,溶液变为棕黄色,加入淀粉溶液后溶液变蓝,则溶液中有I-存在,B对;SO与Ba(NO3)2反应形成的BaSO3沉淀在加入稀盐酸时会转化为BaSO4沉淀,C错;能使澄清石灰水变浑浊的气体是CO2或SO2,原溶液中可能存在的离子是CO、HCO、SO或HSO,D错。
[答案] B
4.下列符合化学实验“绿色化”的有 ( )
①在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水 ②在铜与浓硫酸反应的实验中,将铜片改为可调节高度的铜丝 ③将实验室的废酸液与废碱液中和后再排放
A.①② B.①③
C.②③ D.①②③
[解析] 因为溴易挥发,所以在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水。在铜与浓硫酸反应的实验中为避免生成过量的SO2污染空气,将铜片改为可调节高度的铜丝。将实验室的废酸液与废碱液中和后再排放,可减少水体污染。
[答案] D
3.用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
|
选项 |
操作及现象 |
溶液 |
|
A |
通入CO2,溶液变浑浊。再升温至65
℃以上,溶液变澄清 |
C6H5ONa 溶液 |
|
B |
通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失 |
Na2SiO3 溶液 |
|
C |
通入CO2,溶液变浑浊。再加入品红溶液,红色褪去 |
Ca(ClO)2 溶液 |
|
D |
通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。再加入足量NaOH溶液,又变浑浊 |
Ca(OH)2 溶液 |
[解析] A项,CO2+C6H5ONa―→C6H5OH+NaHCO3,升温至65 ℃以上,C6H5OH完全溶解,溶液变澄清。B项,CO2+Na2SiO3+H2O===Na2CO3+H2SiO3↓,H4SiO4与CO2不反应,浑浊不会消失。C项,CO2+Ca(ClO)2+H2O===CaCO3↓+2HClO,所以溶液变浑浊。加入品红,被HClO氧化褪色。D项,首先,CO2+Ca(OH)2===CaCO3↓+H2O,继续通CO2,产生可溶于水的Ca(HCO3)2,再加入足量的NaOH,则:2NaOH+Ca(HCO3)2===CaCO3↓+Na2CO3+2H2O,溶液又变浑浊。
[答案] B
2.用过量的H2SO4、NaOH、NH3·H2O、NaCl等溶液,按下图所示步骤分开五种离子,则溶液①,②,③,④是 ( )
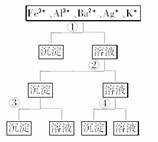
A.①NaCl ②NaOH ③NH3·H2O ④H2SO4
B.①H2SO4 ②NaOH ③NH3·H2O ④NaCl
C.①H2SO4 ②NH3·H2O ③NaOH ④NaCl
D.①NaCl ②NH3·H2O ③NaOH ④H2SO4
[解析] 从题图所示步骤综合分析,可以看出第①步分离五种离子中的一种离子,只能是Ag+与Cl-结合生成AgCl沉淀。第②步产生的沉淀和剩余的溶液分别分离出两种离子,应用NH3·H2O沉淀出Fe3+和Al3+,然后用强碱NaOH溶液将Fe(OH)3和Al(OH)3分离。第④步用SO将Ba2+和K+分离,故答案为D。
[答案] D
1.(2008年新课程)下列除去杂质的方法正确的是 ( )
A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体
B.除去CO2中的少量HCl:通入Na2CO3溶液,收集气体
C.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
[解析] A项中灼热的CuO不能除去O2。B项中碳酸钠溶液在除去HCl的同时,也和CO2反应,生成碳酸氢钠。D项中加入NaOH虽然可以把氯化镁除去,但同时又生成了氯化钠,引入了新的杂质,不合题意。
[答案] C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com