
题目列表(包括答案和解析)
25.(2010安徽卷)(14分)
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
|
元素 |
相关信息 |
|
X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
|
Z |
Z和Y同周期,Z的电负性大于Y |
|
W |
W的一种核素的质量数为63,中子数为34 |
(1)Y位于元素周期表第 周期表 族,Y和Z的最高价氧化物对应的水化物的酸性较强的是 (写化学式)。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键。在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子核外电子排布式是  。W2Y在空气中煅烧生成W2O的化学方程式是
。
。W2Y在空气中煅烧生成W2O的化学方程式是
。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
XO(g)+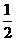 O2(g)=XO2(g)
O2(g)=XO2(g) 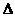 H=-283.0 kJ·mol-2
H=-283.0 kJ·mol-2
Y(g)+ O2(g)=YO2(g) 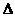 H=-296.0 kJ·mol-1
H=-296.0 kJ·mol-1
此反应的热化学方程式是 。
答案:(1)3 VIA HClO4
(2)2 H-Z H-Y
(3)[Ar]3d104s1 2Cu2S+3O2=2Cu2O+2SO2
(4)2CO(g)+SO2(g)=S(s)+2CO2 (g) △H=-270kJ/mol
解析:由表中可知,X为C Y为 S Z为 Cl W为Cu
8.(2010江苏卷)下列说法不正 确的是
确的是
A.铅蓄电池在放电过程中,负极质量减小,正极质量增加
B.常温下,反应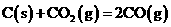 不能自发进行,则该反应的
不能自发进行,则该反应的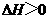
C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
D.相同条件下,溶液中 、
、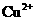 、
、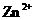 的氧化性依次减弱
的氧化性依次减弱
[答案]AC
[解析]本题主要考查的是相关的反应原理。A项,铅蓄电池在放电过程中,负极反应为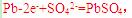 其质量在增加;B项,该反应是典型的吸热反应,在常温下不能自发进行;C项,催化剂能改变反应速率,不一定加快,同时它不能改变转化率;D项,
其质量在增加;B项,该反应是典型的吸热反应,在常温下不能自发进行;C项,催化剂能改变反应速率,不一定加快,同时它不能改变转化率;D项,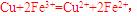 可知
可知 的氧化性大于
的氧化性大于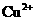 ,综上分析可知,本题选AC项。
,综上分析可知,本题选AC项。
17.(2010上海卷)据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实。
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) 下列叙述错误的是
CH3CH2OH(g)+3H2O(g) 下列叙述错误的是
A.使用Cu-Zn-Fe催化剂可大大提高生产效率
B.反应需在300℃进行可推测该反应是吸热反应
C.充入大量CO2气体可提高H2的转化率
D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
答案:B
解析:此题考查化学反应速率和化学平衡知识。催化剂能提高化学反应速率,加快反应进行,也就是提高了生产效率,A对;反应需在300℃进行是为了获得较快的反应速率,不能说明反应是吸热还是放热,B错;充入大量CO2气体,能使平衡正向移动,提高H2的转化率,C对;从平衡混合物中及时分离出产物,使平衡正向移动,可提高CO2和H2的转化率,D对。
易错警示:利用化学平衡知识判断反应吸热还是放热时,一定要注意温度的变化使反应正向移动还是逆向移动,倘若给出的知识温度条件则无法判断。
14.(2010上海卷)下列判断正确的是
A.测定硫酸铜晶体中结晶水含量时,灼烧至固体发黑,测定值小于理论值
B.相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量
C.0.1 mol·L-1的碳酸钠溶液的pH大于0.1 mol·L-1的醋酸钠溶液的pH
D.1L 1 mol·L-1的碳酸钠溶液吸收SO2的量大于1L mol·L-1硫化钠溶液吸收SO2的量
答案:C
解析:此题考查了实验操作、化学反应中的能量变化、溶液的pH、元素化合物等知识。测定硫酸铜晶体中结晶水含量时,灼烧至固体发黑,说明部分硫酸铜分解生成了氧化铜,测定值大于理论值,A错;氢原子转化为氢分子,形成化学键放出能量,说明2mol氢原子的能量大于1molH2,B错;碳酸的酸性弱于醋酸,故此相同浓度的碳酸钠溶液的pH大于醋酸钠溶液,C对;1L 1mol.L-1的溶液中含有溶质1mol,前者发生:Na2CO3+SO2+H2O=2NaHSO3+CO2↑;后者发生:2Na2S+5SO2+2H2O=4NaHSO3+3S↓;分析可知,很明显后者大于前者,D错。
易错警示:此题解答是的易错点有二:一是对化学键的形成断开和吸热放热的关系不清,要能够准确理解断键吸热成键放热;二是忽视亚硫酸的酸性强于氢硫酸,不能准确判断硫化钠中通入二氧化硫时要生成氢硫酸,造成氢硫酸和亚硫酸能发生氧化还原反应生成单质硫。
12.(2010浙江卷) 下列热化学方程式或离子方程式中,正确的是:
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
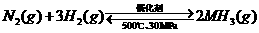 △H=-38.6kJ·
△H=-38.6kJ· mol-1
mol-1
C. 氯化镁溶液与氨水反应: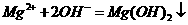
D. 氧化铝溶于NaOH溶液: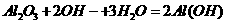
试题解析:
本题考查热化学方程式与离子方程式的书写。A、标准燃烧热的定义,1mol可燃物完全燃烧生成稳定氧化物时方出的热量(标准指298K,1atm)。水液态稳定,方程式系数就是物质的量,故A错。B、根据热化学方程式的含义,与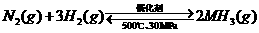 对应的热量是1mol氮气完全反应时的热量,但次反应为可逆反应故,投入0.5mol的氮气,最终参加反应的氮气一定小于0.5mol。所以△H的值大于38.6。B错。D、氢氧化铝沉淀没有沉淀符号。
对应的热量是1mol氮气完全反应时的热量,但次反应为可逆反应故,投入0.5mol的氮气,最终参加反应的氮气一定小于0.5mol。所以△H的值大于38.6。B错。D、氢氧化铝沉淀没有沉淀符号。
本题答案:C
教与学提示:
化学用语的教学是化学学科技术规范,强调准确性,强调正确理解与应用。特别重视热化学方程式的系数与反应热的对应关系。重视离子方程式的拆与不拆的问题。热化学方程式的书写问题由:聚集状态、系数、系数与反应热数值对应、反应热单位、可逆反应的反应热等内容构成。离子方程式的书写问题由:强弱电解质、最简整数比、定组成规律、离子方程式正误判断、守恒、定量离子方程式等内容组成。
9.(2010广东理综卷)
在298K、100kPa时,已知:2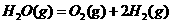 ⊿
⊿
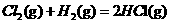 ⊿
⊿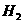
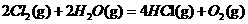 ⊿
⊿
则⊿ 与⊿
与⊿ 和⊿
和⊿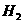 间的关系正确的是
间的关系正确的是
A .⊿ =⊿
=⊿ +2⊿
+2⊿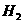 B ⊿
B ⊿ =⊿
=⊿ +⊿
+⊿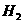
C. ⊿ =⊿
=⊿ -2⊿
-2⊿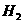 D. ⊿
D. ⊿ =⊿
=⊿ - ⊿
- ⊿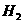
解析:第三个方程式可 由第二个方程式乘以2与第一个方程式相加,有盖斯定律可知
由第二个方程式乘以2与第一个方程式相加,有盖斯定律可知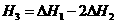
答案:A
6.(2010天津卷)下列各表述与示意图一致的是
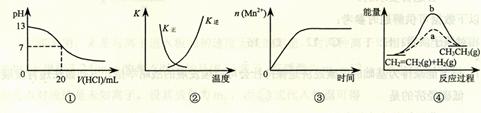
A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2 (g)
+ O2(g)
(g)
+ O2(g)  2SO3(g);ΔH
< 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH
< 0 正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol·L-1 KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2
(g) + H2(g)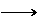 CH3CH3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化
CH3CH3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化
解析:酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,故A错;正逆反应的平衡常数互为倒数关系,故B正确;反应是放热反应,且反应生成的Mn2+对该反应有催化作用,故反应速率越来越快,C错;反应是放热反应,但图像描述是吸热反应,故D错。
答案:B
命题立 意:综合考查了有关图像问题,有酸碱中和滴定图像、正逆反应的平衡常数图像,反应速率图像和能量变化图像。
意:综合考查了有关图像问题,有酸碱中和滴定图像、正逆反应的平衡常数图像,反应速率图像和能量变化图像。
12. 答案D
[解析]本题考查盖斯定律的计算。由已知得:Br2(l)=Br2(g) DH=+30KJ/mol,则H2(g) + Br2(g) = 2HBr(g);DH= -102KJ/mol。436+a-2×369=-102;a=―200KJ,D项正确。
12.(2010重庆卷)已知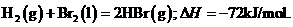 蒸发1mol Br2(l)需要吸收的
蒸发1mol Br2(l)需要吸收的 能量为30kJ,其它相关数据如下表:
能量为30kJ,其它相关数据如下表:

则表中a为
A.404 B.260 C.230 D.200
8.(2011江苏高考20,14分)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知: CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=-247.4 kJ·mol-1
2H2S(g)=2H2(g)+S2(g) △H=+169.8 kJ·mol-1
(1)以甲烷为原 料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
。
料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
。
(2)H2S热分解制氢时,常向反应器中通入一定比例空气,使部分H2S燃烧,其目的是
。燃烧生成的SO2与H2S进一步反应,生成物在常温下均非气体,写出该反应的化学方程式: 。
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图11所示。图中A、B表示的物质依次是 。
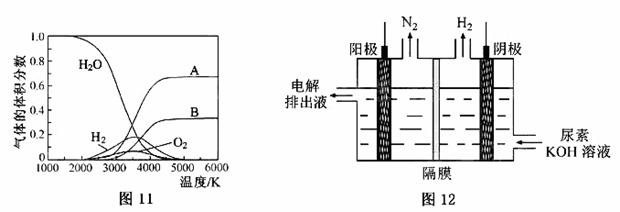
(4)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图12(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为 。
(5)Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为 。
解析:本题以新能源为背景涉及元素化合物性质、热化学方程式和电极反应方程式的书写、读图读表的综合题,是以化学知识具体运用的典型试题。
(1)利用盖斯定律即可得出;(2)H2S热分解制氢属于吸热反应,需要提供能量;(3)在很高的温度下,氢气和氧气会分解生成氢原子和氧原子;(4)阳极失去电子,在碱性溶液中碳原子变成CO32-。
[备考提示]高三复习一定要关注生活,适度加强综合训练与提升。
答案:(1)CH4(g)+2H2O(g) =CO2(g) +4H2(g) △H=165.0 kJ·mol-1
(2)为H2S热分解反应提供热量 2H2S+SO2 =2H2O+3S (或4H2S+2SO2=4H2O+3S2)
(3)H、O(或氢原子、氧原子)
(4)CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O
(5)2Mg2Cu+3H2 MgCu2+3MgH2
MgCu2+3MgH2
2010年高考化学试题
(2010山东卷)10下列与化学反应能量变化相关的叙述正确的是
A 生成物能量一定低于反应物总能量
B 放热反应的反应速率总是大于吸热反应的反应速率
C 英语盖斯定律,可计算某些难以直接侧脸房的反应焓变
D 同温同压下,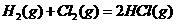 在光照和点燃条件的
在光照和点燃条件的 不同
不同
解析:生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反,故A错;反映速率与反应是吸热还是放热没有必然的联系,故B错;C是盖斯定律的重要应用,正确;根据 =生成物的焓-反应物的焓可知,焓变与反应条件无关,故D错。
=生成物的焓-反应物的焓可知,焓变与反应条件无关,故D错。
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com