
题目列表(包括答案和解析)
3.电解水实验(水中加少量硫酸或NaOH,增强水的导电性)
① 水通电(正极O2 负极H2 ,体积比1:2) 2H2 O===2H2 ↑ + O2 ↑
②证明物质里是否含水方法:白色的无水硫酸铜遇水变蓝色
③.除去混合气体中的水蒸气,通常放在最后除,如除去氢气中含有(HCl、水蒸气、CO2),先通过 再通过 。
④.要验证混合气体中是否含有水蒸气,通常应先检验,如证明氢气中含有HCl、水蒸气、CO2,应先让混合气体通过 (填仪器和其中的药品),观察到
时,则说明含有 ;再通过 ,当观察到 ,则含有 ,接着通过 ,当观察到 ,则说明含有 。
2. 污染水质的因素:工业生产中的废渣、废水、废气(即“三废”)和生活污水的任意排放,
农业生产中施用的农药、化肥随雨水流入河流。
1.水、蒸馏水是纯净物、化合物和氧化物。矿泉水、海水、河水、糖水和盐水都属于混合物
32.常见的盐
a.氯化钠(NaCl 食盐的主要成分) NaCl+AgNO3 =NaNO3 +AgCl↓
粗盐提纯的步骤:1.溶解 2.过滤 3.蒸发 4.结晶
实验仪器:药匙、烧杯、玻璃棒、蒸发皿、漏斗、量筒、酒精灯、
b.碳酸钠(俗名:纯碱,Na2 CO3 类别:盐, 不是碱)
① 碳酸钠+酸→盐+H2 O + CO2 ↑
例: Na2 CO3 +2HNO3 =2NaNO3 +H2 O+CO2 ↑
② 2AgNO3 +Na2 CO3 =2NaNO3 +Ag2 CO3 ↓
CaCl2 +Na2 CO3 =2NaCl+CaCO3 ↓
BaCl2 +Na2 CO3 =2NaCl+ BaCO3 ↓
③ Ca(OH)2 +Na2 CO3 =2NaOH+CaCO3 ↓
c.硫酸铜(硫酸铜晶体俗名:蓝矾、胆矾)
①加热蓝色硫酸铜晶变为白色 无水硫酸铜是白色固体,遇水变蓝色
CuSO4·5H2O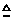 CuSO4 +5H2O CuSO4 +5H2O=
CuSO4·5H2O
CuSO4 +5H2O CuSO4 +5H2O=
CuSO4·5H2O
硫酸铜溶液跟可溶性碱反应有蓝色沉淀生成物:
CuSO4+2NaOH=Cu(OH)2↓+Na2 SO4
③ 置换反应Fe+CuSO4 =FeSO4 +Cu Zn + CuSO4 =ZnSO4 + Cu
31.氢氧化钙(俗名:消石灰、熟石灰 化学式Ca(OH)2 )
白色固体,微溶于水,溶解度随温度升高而降低。用生石灰跟水反应制得。
用途:与硫酸铜配制农药“波尔多液”,可用来降低土壤酸性,制建筑业的三合土
氢氧化钠和氢氧化钙不同点:氢氧化钙跟二氧化碳、碳酸钠、碳酸钾反应有白色沉 淀生成,氢氧化钠则无沉淀生成。
CO2+ Ca(OH)2=CaCO3↓+H2O Na2CO3+ Ca(OH)2 =CaCO3↓+2NaOH
写出下列转变的化学方程式:CaCO3→CaO→Ca(OH)2→CaCO3
30.氢氧化钠(俗名:烧碱、火碱、苛性钠 化学式:NaOH)
物理性质: 白色固体,极易溶于水且放出大量热,有吸水性,易潮解
氢氧化钠易潮解,称量时必须放在玻璃器皿(如烧杯、表面皿)里称量。
NaOH会吸收空气中的水分,又会跟二氧化碳反应,所以必须密封保存
用途:作中性或碱性气体的干燥剂,不能干燥二氧化硫、二氧化碳、氯化氢,
可干燥H2、O2、N2、CO、NH3 、CH4等;用于肥皂、石油、造纸等工业
化学性质:(KOH的化学性质跟NaOH相同)
①二氧化碳、二氧化硫分别通入氢氧化钠溶液里(无明显现象)
CO2+2NaOH=Na2CO3+H2O
SO2+2NaOH=Na2SO3+H2O SO3+2NaOH=Na2SO4+H2O
②硫酸和硝酸分别跟氢氧化钠溶液发生中和反应(无明显现象)
③氢氧化钠跟盐反应
a. 氢氧化钠溶液跟氯化铁、硫酸铁、硝酸铁溶液的现象和方程式:
现象有红褐色沉淀生成:6NaOH+Fe2(SO4)3=3Na2SO4+2Fe(OH)3↓
b. 氢氧化钠溶液跟氯化铜、硫酸铜、硝酸铜溶液的现象和方程式:
现象有蓝色沉淀生成:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
c. 氢氧化钠溶液跟氯化镁、硫酸镁、硫酸铝溶液的现象有白色沉淀生成
方程式:2NaOH+MgSO4=Na2SO4+Mg(OH)2↓
29.硝酸(HNO3 )有酸的通性,但跟金属反应不生成氢气 磷酸H3 PO4
28.浓硫酸的稀释:稀释浓硫酸时,必须把浓硫酸沿着容器壁慢慢地注入水里,并不断搅拌,使产生的热量迅速扩散,切不可把水倒入浓硫酸里。
盐酸(或氯化物)和硫酸(硫酸盐)的区别方法:最好用可溶性钡的化合物氯化钡 (硝酸钡或氢氧化钡),有白色沉淀生成的是硫酸(硫酸盐),无现象的是盐酸
不能用硝酸银溶液,因硝酸银跟硫酸反应有硫酸银白色沉淀生成。
27.盐酸和硫酸用途:硫酸和盐酸可除去金属表面的锈,都是重要的工业原料
盐酸(氢氯酸,HCl气体的水溶液,无色液体) 浓盐酸有挥发性,会挥发出HCl
硫酸(H2 SO4 ) 浓硫酸有吸水性,可作气体的干燥剂
26.氧化物的性质:
①有四种碱性氧化物跟水反应生成碱,其他的碱性氧化物不溶于水跟水不反应
Na2 O+H2 O=2NaOH CaO+H2 O=Ca(OH)2
K2 O+H2 O=2KOH BaO+H2 O=Ba(OH)2
②酸性氧化物:大部分非金属氧化物都是酸性氧化物,跟水化合生成同价的含氧酸。
CO2 +H2 O=H2 CO3 SO2 +H2 O=H2 SO3 SO3 +H2 O=H2 SO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com