
题目列表(包括答案和解析)
35.(5分)t℃时,向100克质量分数为20%的氢氧化钠溶液中加入等质量的硫酸溶液,恰好完全反应,并测得反应后溶液的pH等于7,然后蒸发掉39.5克水,再冷却到t℃,恰好成为饱和溶液。求:(1)硫酸溶液中溶质的质量分数。(2)t℃时生成物的溶解度。
34.63.8%
34.(5分)为了制取氧气,取一定量的氯酸钾和二氧化锰的混和物,二氧化锰在混和物中的质量分数为20%,加热后,二氧化锰质量分数提高到25%,则此时氯酸钾分解的百分率是____________。
33. NaOH;H2SO4;Na2SO4 ;Ba(OH)2 ;Cu(OH)2
33.(5分)A、B、C、D、E分别是常见的酸、碱、盐中的某种物质,并且已知A是含钠元素的化合物。它们之间有如下关系: 2A+B=C+2H2O (2) C+D=BaSO4↓+2A (3) D+CuSO4=BaSO4↓+E↓;根据以上反应,推断各物质的化学式:
A____________;B____________;C____________;D____________;E________。
32. 固体表面逐渐形成溶液;潮解; Na2CO3 ;;CO2+2NaOH====Na2CO3+H2O;有无色气体析出;Na2CO3+2HCl==== 2NaCl+H2O+CO2↑
32.(4分)氢氧化钠固体暴露在空气中,观察到的现象是______________________,这现象叫______________。在空气中久置一段时间,能生成白色粉末物质,此物质主要含有____________,用化学方程式表示发生的变化:______________________________。
若向白色粉末物质滴加盐酸时,现象是______________________________,化学方程式为_______________________________________________。
31. (1)B; D; C;
A; E
(2)炭粉;大理石、稀盐酸 (3)氧化 (4)用酒精灯将尾气点燃(或用气球收集后统一处理)。 ⑸:CO+CuO 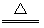 CO2+Cu; CaCO3+2HCl ===CaCl2 +CO2↑+H2O; CO2+C
CO2+Cu; CaCO3+2HCl ===CaCl2 +CO2↑+H2O; CO2+C 2CO; Ca(OH)2+CO2===CaCO3↓+H2O;
2CO; Ca(OH)2+CO2===CaCO3↓+H2O;
31.(10分)(1)用下列所提供的仪器装配成一套“一氧化碳(干燥的)与氧化铜反应”的实验装置,从左到右的顺序是(用代号填写)________________。
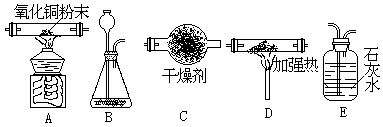
(2)D中应放的物质是__________________,B中应放的物质是________________。
(3)A中氧化铜是________剂。
(4)最后尾气应作如何处理________________________________
(5)写出有关化学方程式:
A中:___________________、
B中:___________________、
D中:___________________、
E中:___________________。
30.⑴CaO+H2O=Ca(OH)2 ⑵CaCO3 CaO+CO2↑ ⑶Fe+2HCl==== FeCl2+H2↑
⑷Na2CO3+Ca(OH)2====CaCO2↓+2NaOH
CaO+CO2↑ ⑶Fe+2HCl==== FeCl2+H2↑
⑷Na2CO3+Ca(OH)2====CaCO2↓+2NaOH
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com