
题目列表(包括答案和解析)
10.某学生在A、B、C、D四只小烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝,并使铁丝完全浸没在食盐水中,然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如下表
|
时间/小时 |
0 |
0.5 |
1.0 |
1.5 |
2.0 |
2.5 |
3.0 |
|
A瓶(盛干燥铁丝) |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
B瓶(盛沾了食盐水的铁丝) |
0 |
0.4 |
1.2 |
3.4 |
5.6 |
7.6 |
9.8 |
|
C瓶(盛沾了清水的铁丝) |
0 |
0 |
0 |
0.3 |
0.8 |
2.0 |
3.5 |
|
D瓶(盛完全浸没在食盐水中的铁丝) |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
(表中所列数据为导管中水面上升的高度/cm)所示。
 (1)导管中水面为什么会上升?
(1)导管中水面为什么会上升?
(2)上述实验中,铁生锈的速率由大到小的排列顺序为(填小烧杯号): __ 。
(3)影响铁生锈的因素有:
___________________ _ _ ___ _。
(参考答案:(1)铁生锈时跟空气中的氧气反应,消耗了氧气而使小烧杯中气体压强降低。(2)B>C>A=D (3)①跟氧气接触;②有水分存在;③有电解质(或答盐)存在,三者同时具备时铁生锈速度最快。)
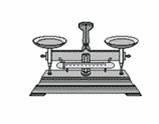
9.右图中的天平在称量物体时,若指针往左偏,应如何操作?(加砝码或向右移游码。)
8.某农民承包一鱼塘(鱼塘里有水草),因技术不精,常有鱼发生死亡。经过学习养鱼技术,他采取了以下措施:①及时清除鱼池底部淤泥(也称清塘);②投放饵料或有机肥料先堆沤足够时间,使其充分发酵后再投入鱼池;③闷热的夏天,后半夜或凌晨使用增氧泵。
(1)鱼池生态系统中,供氧源有 ,耗氧的是 。
(2)①、②两个措施具有相同的作用,即减少有机物 ,从而使水中溶解氧 。
(3)闷热的夏天,由于温度 ,气压 ,气体的溶解度 。
(4)后半夜或凌晨,水中溶解氧降低是由于 。
 参考答案:(1)水生植物、溶解氧;水生生物。(2)氧化;消耗减少。(3)升高;降低;减少。(4)水生植物不进行光合作用,只进行呼吸作用。
参考答案:(1)水生植物、溶解氧;水生生物。(2)氧化;消耗减少。(3)升高;降低;减少。(4)水生植物不进行光合作用,只进行呼吸作用。
7.碳酸氢盐是属于酸式盐,它可以与碱反应生成正盐,例如,Ca(HCO3)2与NaOH反应生成CaCO3沉淀,它受热后易发生分解反应,如Ca(HCO3)2== CaCO3↓+CO2↑+H2O,现有某活泼金属A的四种化合物W、X、Y、Z,其中A是日常生活中去污粉的主要成分,根据以下关系推断(用化学式表示)
(1)A+H2O→Y+H2↑ (2)W→X+CO2↑+H2O (3)Y+CO2→X+H2O (4)Z+H2O→Y
(5)X+Ca(OH)2→Y+CaCO3↓
则X为 Y为 W为 化学方程式W+Y→
6、铜锈的主要成分是铜绿[Cu2(OH)2CO3],为了研究生锈条件,某化学兴趣小组进行了如下图示出的实验。一个月后,才发现B中的铜丝缓慢生锈,且水面处铜丝生锈较为严重。而A、C、D中的铜丝基本无变化。试根据图中铜丝生锈的实验回答下列问题:
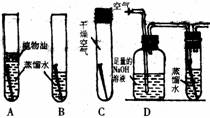 (1)铜生锈所需要的条件实际上是铜与 相互作用发生化学反应的结果。
(1)铜生锈所需要的条件实际上是铜与 相互作用发生化学反应的结果。
(2)写出广口瓶中发生反应的化学方程式
。
(3)铜生锈产生铜绿的化学方程式
。
(4)铜和铁相比, 更易生锈,由此得出的结论是 。
5.已知碳酸氢钙易溶于水,受热易分解,分解反应的化学方程式为:
Ca(HCO3)2=CaCO3↓+CO2↑+H2O
现要用实验方法证明上述反应的产物。请回答下列有关问题:
(1)写出分解碳酸氢钙所需的主要仪器名称。
(2)在实验中,有人提出必须先检验分解产物碳酸钙,再检验二氧化碳和水,你认为该建议是否正确?
(3)简述如何用实验方法证明分解产物中有二氧化碳?
(4)简述如何用实验方法证明分解产物中含有碳酸钙?
4.某研究者要用实验证明碳酸(二氧化碳的水溶液)具有酸性,而二氧化碳不具有酸性。其实验方法是:向一只洁净的干燥的试管,里放人一条干燥的蓝色石蕊试纸,向试管中加入水,观察现象;然后再往试管中通入二氧化碳气体,再观察现象。此研究者仅由此实验能得出满意的结论吗?若能,请你说明理由。若不能,请你简述还需要进行的实验操作步骤和实验。
3、实验室里有一瓶标签残缺的盐酸,请你来共同探究。
(1)怎样立即确定它是不是浓盐酸?你认为,应该用下述中的____方法(填选项编号)确认。
A. 讨论 B.调查 C.实验 D.上网
具体的做法是 。
(2)粗略测定该盐酸每毫升溶液中含溶质HCl的质量。同学们依据酸碱中和反应的原理,设计了一种可行的实验方案,具体操作步骤如下:
 第1步,在小烧杯中加入10g 5%的NaOH溶液;第2步,向上述小烧杯中滴人2滴酚酞试液;第3步,向10mL的量筒中注入该盐酸至一定刻度;第4步,用胶头滴管吸取量筒中的盐酸,逐滴滴入上述烧杯中,……一直到溶液由红色刚刚变成无色为止;第5步,记录实验数据;第6步,计算,确定每毫升盐酸中含溶质HCl的质量。
第1步,在小烧杯中加入10g 5%的NaOH溶液;第2步,向上述小烧杯中滴人2滴酚酞试液;第3步,向10mL的量筒中注入该盐酸至一定刻度;第4步,用胶头滴管吸取量筒中的盐酸,逐滴滴入上述烧杯中,……一直到溶液由红色刚刚变成无色为止;第5步,记录实验数据;第6步,计算,确定每毫升盐酸中含溶质HCl的质量。
请根据以上实验过程,回答下面问题:
①本实验为什么要用指示剂(酚酞)?②第3步中向量筒注入盐酸,量筒中液面的位置如图1所示,A与召、B与C刻度间均相差1mL,如果刻度A为8,量筒中盐酸的体积是 mL。③第4步要用到玻璃棒,它是作 用,目的是 。停止滴入盐酸后,胶头滴管中残留的盐酸应 。④第5步要记录的实验数据是 。
(3)测定每毫升该盐酸中含溶质HCl的质量的原理和方法还有多种,为此大家继续进行探究。有人提出用KOH等碱类试剂代替上述NaOH与盐酸进行中和反应,测定耗去盐酸的体积,通过计算确定盐酸中HCl的含量,这和上述实验属同一种方法。你能写出三种其他可行的方法吗?若能,请写在下面(用文字简述所依据的原理和要测定的数据,不需要写出化学方程式):
方法一: ;方法二: ;方法三: 。
(4)请你在上述三种方法中,选一种,并写出按此法实验所需要的玻璃仪器。
我选的是方法 ,所需要的玻璃仪器是 。
2、某课外活动小组为探究钢铁制品生锈的条件,进行了研究性学习。他们准备了以下实验用品:刚洗净的4支试管、3枚铁钉、植物油、久制的蒸馏水、镊子、滤纸,还需要的实验用品为_________________。
做实验时发现铁钉上有锈,为了迅速除去铁锈,他们进行了下述实验操作:
(1)取一支试管,将生锈的铁钉放入试管;(2)向试管中倒入2ml稀盐酸;(3)用试管夹夹持试管在酒精灯上加热;(4)当铁钉上的锈消失并变得光亮时,将试管内废液倒入废液缸内;(5)用镊子夹取铁钉用蒸馏水冲洗干净,在酒精灯外焰上烘干铁钉。
你认为水述操作中存在的问题是什么?应该怎样做?
除了给铁钉除锈外,上述给出的实验用品还有哪些不符合实验要求应该怎样处理?
1、研究发现,铝元素能损害人的脑细胞,因此世界卫生组织规定,每日对铝元素的摄入量应控制在0.004g以下。油条是中国北方常见的食品之一,100g油条中约含0.33g明矾[KAl(SO4)2 12H2O]。问:
⑴明矾的相对分子质量是多少?
⑵若按一天食用100g油条,铝元素的摄入量是否超过安全摄入量?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com