
题目列表(包括答案和解析)
(一)相对分子质量的计算:
(1)求(NH4)2SO4和Na2CO3•10H2O的分子质量。
(NH4)2SO4=(14+4)×2+96
=132
Na2CO3•10H2O=23×2+12+16×3+10×(2+16)
=106+180
=286
(二)酸、碱、盐鉴别
(1)酸、碱、盐用紫色石蕊鉴别
(2)盐酸盐(可溶性)鉴别
试剂:AgNO3和稀HNO3
 步骤:(1)取少量待测液于试管中(2)滴入几滴稀HNO3(3)有白色沉淀产生,该沉淀不能溶于稀HNO3中说明是盐酸盐即含有CI-
步骤:(1)取少量待测液于试管中(2)滴入几滴稀HNO3(3)有白色沉淀产生,该沉淀不能溶于稀HNO3中说明是盐酸盐即含有CI-
(3)硫酸盐鉴别:
试剂:BaCI2和稀HNO3
步骤:(1)取少量待测液于试管中(2)滴入BaCI2并加稀HNO3,若产生沉淀则说明是硫酸盐即含SO42-
(4)可溶性钡盐鉴别:(略)
(5)碳酸盐鉴别:(略)
(6)铵盐(NH4+)鉴别:(略)
(一)常见气体鉴别方法
 O2
燃烧更旺:O2
O2
燃烧更旺:O2

 H2
木条熄灭:CO2 分别往集 变红:CO2
H2
木条熄灭:CO2 分别往集 变红:CO2
 CO2
NH3 气瓶中滴少
变蓝:NH3
CO2
NH3 气瓶中滴少
变蓝:NH3
CO 燃着木条分别 N2 许石蕊试液 不变:N2

 CH4 伸到各集气瓶内
H2O
CH4 伸到各集气瓶内
H2O


 NH3
有水珠:
NH3
有水珠:
 N2
被点燃气体:H2 于火焰上方
CH4
N2
被点燃气体:H2 于火焰上方
CH4
 CO 罩干冷烧杯
CO 罩干冷烧杯
 CH4
无水珠:CO
CH4
无水珠:CO

 产生气体 变浑:CH4
产生气体 变浑:CH4
 通入石灰水中
不变浑:H2
通入石灰水中
不变浑:H2
(1)化学变化(2)物理变化(3)稀有气体(4)氧化反应(5)催化剂(6)燃烧(7)混合物(8)化合物(9)纯净物(10)单质(11)氧化物(12)酸性氧化物(13)碱性氧化物(14)酸(15)碱(16)盐(17)结晶水合物(18)原子量(19)风化(20)质量守恒定理(21)饱和溶液(22)溶解度(23)有机化合物(24)温室效应(25)工业血液、工业粮食(26)生铁、钢(27)合金(28)溶液、溶质、溶剂(29)过滤、结晶(30)PH值
(三)主要反应类型
(1)碳酸盐与酸的反应:反应都生成CO2
即:MSO4+2HCI====MCI2+CO2↑+H2O
(2)硫酸盐与钡盐的反应:反应后都生成难溶于酸的BaSO4↓
即:MSO4+BaN====BaSO4↓+MN
(3)盐酸盐与AgNO3反应:生成难溶酸的AgCI↓
即:盐酸盐+AgNO3====AgCI↓+酸
(4)金属氧化物一般难溶水(除K2O、Na2O、CaO)外易溶于酸
(5)非金属氧化物一般易溶碱溶液中
 (6)酸+碱 盐+水 (中和反应)
(6)酸+碱 盐+水 (中和反应)
(二)主要反应方程式:


 S+O2===SO2 (气) Fe2O3+3CO====2Fe+3CO2
S+O2===SO2 (气) Fe2O3+3CO====2Fe+3CO2



4P+5O2======2P2O5(固) Fe 3O4+4CO=====3 Fe+4CO2




3 Fe+2O2===== Fe3O4(固) 2KCIO3====2KCI+3O2↑



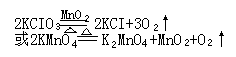 Mg+O2=====2MgO(固) 2KMnO4=====K2MnO4+MnO2+O2↑
Mg+O2=====2MgO(固) 2KMnO4=====K2MnO4+MnO2+O2↑
C+O2====CO2 Zn+2HCI====ZnCI2+H2↑
 Zn+H2SO4===ZnSO4+H2↑
Zn+H2SO4===ZnSO4+H2↑
2C+O2====2CO Fe+2HCI===FeCI2+H2↑


2CO+O2=====2CO Fe+H2SO4====FeSO4+H2↑

CO2+C====2CO Cu+O2====2CuO

CO2+Ca(OH)2====CaCO3↓+H2O CuO+H2===Cu+H2O

CO2+H2O====H2CO3 CuO+CO====Cu+CO2
CO2+2NaOH===Na2CO3+H2O CuO+2HCI====CuCI2+H2O
CaCO3====CaO+CO2↑ Cu(OH)2+HCI===CuCI2+H2O
CaCO3+2HCI===CaCI2+H2O+CO2↑ CuSO4+2NaOH===Cu(OH)2+Na2SO4
CaO+H2O====Ca(OH)2 Na2CO3+CaCO3↓+2NaOH


CH4+2O2====CO2+2H2O C2H5OH+3O2====2CO2+3H2O

CH3OH+ O2====CO2+2H2O
(一)四个反应类型:
化合反应:多各物质经化学变化合为一种物质的反应
 分解反应:由一种物质分妥成多种物质的化学反应
分解反应:由一种物质分妥成多种物质的化学反应
 即:BAC条件 B+A+C
即:BAC条件 B+A+C
 置换反应:单质与化合物发生化学变化生成新的单质与新的化合物的反应:即:单+化合物 条件 新单+新化合物
置换反应:单质与化合物发生化学变化生成新的单质与新的化合物的反应:即:单+化合物 条件 新单+新化合物
 分解反应:化合物A+化合物B 化合物C+化合物D
分解反应:化合物A+化合物B 化合物C+化合物D
(二)实验室制法:
 药品:1KCIO3和MnO2(催化剂)或2KMnO4(紫色)
药品:1KCIO3和MnO2(催化剂)或2KMnO4(紫色)
反应原理:
仪器:


步骤:(1)检查气密性(2)装药品 (3)加热 (4)收集 (5)移去水中导气管(6)熄灭酒精灯
实验中常注意问题:(1)酒精灯加热用外焰加热(2)试管夹夹持试管位置于离试管口1/3处(3)试管口略向下斜(4)导气管伸进橡皮塞2-3厘米(5)先移去导管、再移去酒精灯。
2、氢气(H2)制法
(1) 工业制氢气的原料:天然气(主要成分CH4)或水煤气(主要成分CO和H2)
(2) 实验实制氢气:
药品:锌粒(Zn)和稀盐酸或稀硫酸
反应原理:Zn+2HCI==ZnCI2+H2↑
或Zn+H2SO4==ZnSO4+H2↑
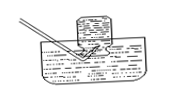

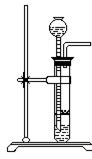 仪器:
仪器:
步骤:略
3、二氧化碳(CO2)制法:
药品:石灰石(大理石)和稀硫酸
反应原理:CaCO3+2HCI==CaCI2+CO2↑+H2O
仪器:其仪器与氢气的仪器大致相同、不同为在CO2收集中不用排水法收集。(所以CO2的制取装置可用来制取H2)
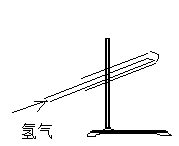 步骤:略
步骤:略
4、氢气还原氧化铜实验:
药品:H2和黑色CuO
△
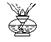 反应原理:H2+CuO===Cu+H2O
反应原理:H2+CuO===Cu+H2O
仪器:

步骤:(1)先通H2一段时间(以防止通入
的H2与试管内空气混合遇火发生爆炸
(2)加热 (3)移去酒精灯 (4)再通氢气一段时间(以防止还原出的Cu在高温下又被氧化为CuO)
注意:(1)实验中的“两通”的目的
(2)导气管位置:不用橡皮塞;试管口略向下倾斜
(3)看到实验现象:A、试管壁有水珠生成B、黑色物质变成红色物质
5、Cu(OH)2CO3的加热实验:
A、反应原理:Cu(OH)2CO3==2CuO+H2O+CO2↑
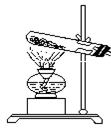 B、仪器: Cu(OH)2CO3
B、仪器: Cu(OH)2CO3
 石灰水
石灰水
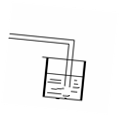
C、实验现象:绿色物质变成黑色物质:在试管壁上有水珠生成;将产生气体通入澄清石水,石灰水变浑浊。
6、电解水实验:
所需物质及仪器:水、直流电、电解仪器
电解
反应原理:2H2O==2H2↑+2O2↑
现象:在阳极和阴极分别有气体产生且有V阳:V阴=2:1
(即VH2:VO2=2:1)
注意:电解水产生氢气和氧气得出结论是:(略)
(一)工业制法:分离液态空气
1、氧气(O2)制法
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com