
题目列表(包括答案和解析)
5、将一铁片投入CuSO4溶液中,过一会儿取出,洗净干燥后称量,发现增重6.3克,析出铜( )g
A、50.4 B、6.4
C、2 D、6.3
4、实验室常用MnO2与KClO3共热制氧气,表示混合物中二氧化锰的质量分数随反应时间的变化图象(横坐标表示时间,纵坐标表示混合物中MnO2的质量分数)是()
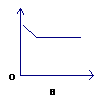
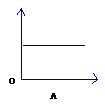
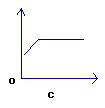
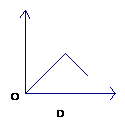
3、某试管中含有a克氧化铜,通入氢气加热一段时间后停止加热,冷却称量剩余固体质量为b克,则参加反应的氢气的质量为()
A、 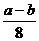 B、(a-b)克
B、(a-b)克
C、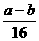 D、
D、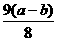
2、下列有关数量关系的判断中错误的是()
A、ag镁和bg氧气恰好完全反应,生成cg氧化镁,则a+b=c
B、mg镁放ng稀硫酸中,充分反应后,溶液为wg,则n﹤w
C、hg铁放人sg硫酸铜溶液中,充分反应后,溶液为eg,则s>e
D、mg氯化钡溶液加入pg硫酸钠溶液中,生成qg溶液,则m+p=q
1、纯净的KClO3和Mn2O2的混合物mg,受热制取O2,完全反应后剩余固体的质量为ng,则反应所得的KCl质量为()
A、ng B、149/64(m-n)g
C、(m-n)g D、149/96(m-n)g
例1.在托盘天平的两盘上,各放一盛有等质量分数足量稀盐酸的烧杯,调节天平至平衡。向左盘烧杯中加入8克氧化镁,若使天平仍然平衡,需向右盘烧杯中加人多少克铝?
解析:由MgO+2HCl=MgCl2+H2O可知,左盘烧杯中增加的质量就是所加的MgO的质量。要使天平仍然平衡,右盘烧杯中物质的质量也应增加8克。而铝会与稀盐酸反应并生成H2逸出,所以加入铝的质量必定大于8克。
例2.某样品为铜和氧化铜的混合物,为测定该样品中氧化铜的含量,取用20克此样品,分四次向其中加入稀盐酸与之充分反应。每次所用盐酸的体积与反应后剩余固体的质量见下表:
|
|
加入稀盐酸的体积/ml |
剩余固体的/g |
|
1 |
40 |
16 |
|
2 |
40 |
12 |
|
3 |
40 |
8 |
|
4 |
40 |
8 |
求:①20g此样品中铜的质量;
②样品中氧化铜的质量分数;
③用氢气充分还原5g此样品可得固体多少克?
解析:根据表格中的数据分析可知第三、四次剩余团体均为8克,说明该剩余固体不能与盐酸反应,这8克固体一定是铜。
例3.为了对海水的氯化物(假设NaCl以计算)进行成分分析。甲、乙、丙三位同学分别进行实验.他们的实验数据如下,请仔细观察分析,回答下列问题。
|
|
甲 |
乙 |
丙 |
|
所取海水样品的质量(g) |
100 |
50 |
50 |
|
加入AgNO3溶液的质量(g) |
50 |
50 |
75 |
|
反应后所得沉淀物的质量(g) |
1.435 |
1.435 |
1.435 |
①两溶液恰好完全反应的是 的实验。
②请计算海水中的氯化物(以氯化钠计算)的质量分数是多少?(结果保留3位有效数字)
解析:根据表中的实验数据,分析可知甲、乙、丙三位同学实验后所得沉淀物的质量相等,则说明三位同学所取的两种反应物的质量至少有一种所取质量正确,全部参加了反应,海水样品乙、丙两同学取质量相同,则说明甲同学取多了。AgNO3溶液的质量甲、乙同学所取相同,则说明丙同学取多了。所以所取溶液恰好完全反应的是乙同学。
4、有关计算公式
①纯净物的质量=混合物的质量×物质的纯度(或质量分数)
②纯净物的质量分数=1-杂质的质量分数
③
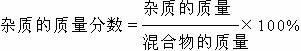
3、根据化学方程式计算应注意的事项
①正确书写化学方程式,准确列出有关反应物或生成物的质量比。
②列式时,各物质的质量单位必须统一,对应关系要正确。
③反应物、生成物必须是纯净物,如果不是纯净物,应将不纯物质的质量按题意换算成纯净物的质量。
④在溶液中进行的反应,应用溶质的质量代入化学方程式进行计算,而不能用溶液的质量代入计算。
⑤解题过程要完整规范。
2、解题步骤
①设未知量;
②正确写出有关化学方程式;
③找出已知量和未知量的质量关系;
④列出比例式,求出未知量;
⑤检查结果,写出答案。
1、有关化学方程式计算的基本类型
①反应物、生成物都是纯净物的计算
②反应物或生成物中含有一定量的杂质的计算
③关于混合物的计算(只要求掌握混合物中有一种成分参加反应的计算)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com