
题目列表(包括答案和解析)
1、H2的工业制法①电解水 ②水煤气转化及分离 ③天然气
|
|
H2 |
C |
CO |
|||||||||||||||||
|
状态 |
气 |
固 |
气 |
|||||||||||||||||
|
类别 |
非金属单质 |
非金属单质 |
非金属氧化物 |
|||||||||||||||||
|
(1)可燃性 |
2H2+O2===2H2O |
C+O2===CO2 2C+O2===2CO |
2CO+O2===2CO2 |
||||||||||||||||
|
(2)还原性 |
yH2+CuxOy==xCu+YH2O |
C+2CuO==2Cu+CO2↑ |
CO+CuO==Cu+CO2 3CO+Fe2O3==2Fe+2CO2 |
|||||||||||||||||
|
(3)不同之处 |
H2、C常温下性质稳定;CO还有毒性 |
|
|
H2 |
CO2 |
|
|
原料及条件类型 |
锌粒、稀硫酸常温反应,置换反应 |
石灰石或大理石与稀盐酸常温反应,复分解反应 |
|
|
化学反应原理 |
Zn+H2SO4=ZnSO4+H2↑ |
CaCO3+2HCl=CaCl2+H2O+CO2↑ |
|
 气体发生装置 气体发生装置 |
这两种气体制备时,原料都是用块状难溶于水的固体与液体常温制气体,所以气体的发生装置可以完全相同,如下几图均可,其中d可做到随时加酸,e甚至还可让反应随时发生或停止 课本中出现的是a与d,其中d的长颈漏斗最下端一定要浸入到液面以下 |
||
|
收集装置及方法 |
由气体的溶解性和密度共同决定 |
||
|
排水法 -难溶于水 或向下排空气法 -密度很小 |
一般只用向上排空气法-密度比空气大 (验满:燃烧木条伸到瓶口) |
||
|
操作过程 |
都是连接装置,检查气密性,然后装药品(固及液)固定后收集 |
||
|
生成物的验证 |
点燃后有淡蓝色火焰,只生成水 |
通入石灰水、石灰水变浑浊 |
|
|
|
H2 |
CO2 |
||||||||
|
物理性质 |
密度 |
比空气小得多 |
比空气大,约是空气密度的1.5倍 |
|||||||
|
溶解性 |
难溶解于水 |
能溶解于水 |
||||||||
|
(1)常温下比较稳定 (2)可燃性 2H2+O2===2H2O (3)还原性 H2+CuO===Cu+H2O yH2+FexOy===xFe+yH2O |
(1)“三不”:不能燃烧,不能支 持一般物质燃烧不能供给呼吸 (2)酸性氧化物的性质 CO2+H2O=H2CO3 CO2+Ca(OH)2=CaCO3↓+H2O CO2+2NaOH=Na2CO3+H2O (3)一定条件下有氧化性 CO2+C===2CO (4)参与光合作用 |
||||||||
|
用 途 |
气体燃料、高能燃料 冶金工业的还原剂,保护气 制盐酸,合成氨等 |
用于灭火(原理) 化工原料,制纯碱,汽水,尿素 干冰作致冷剂,人工降雨,舞台布景,保藏易腐败的食物。 温室肥料 |
42、25克含碳酸钙80%的大理石恰好与100克某盐酸溶液完全反应(杂质不与盐酸反应,且不溶于水)。求:
⑴生成二氧化碳的质量?
⑵原盐酸溶液中溶质的质量分数?
⑶反应后溶液中溶质的质量分数?

41、完全中和25克氢氧化钠溶液,用去质量分数为20%的稀硫酸24.5克,求氢氧化钠中溶质的质量分数?
40、有A、B、C、D、E五种无色气体:H2、O2、CO、CO2、HCl。为区别它们,进行如下实验:
a. 将五种气体分别通入AgNO3溶液,只有E出现沉淀。
b. 将盛有A、B的混合气体的集气瓶移近火焰,发出爆鸣声
c. 将C通入灼热的碳层可得D,D通过加热的CuO可得C
d. E的水溶液与大理石反应产生C
e. 一种暗红色粉末在B中燃烧生成大量白烟
根据上述事实,回答:
⑴这五种气体,A B C D E 。
⑵顺次写出上述各步反应的化学方程式:
a. 。
b. 。
c. 、 。
d. 。
e. 。
39、如图所示,向盛有少量固体的试管里持续通入气体Y,过一会儿在W导管口点火(假设点着得火焰可以达到高温),一定时间后,试管中的固体变成光亮的红色,而澄清的石灰水变浑浊。
⑴若X是CuO、Fe2O3和Cu2(OH)2CO3中的一种,
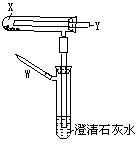
而Y是O2、H2和CO中一种,试推断X和Y
的组合可能有哪几种
。
⑵若X是C和CuO的混合物,Y是CO2,这种组
合行不行?为什么?
38、在实验室中选用下列药品和仪器,制取并收集氢气和氧气。
药品:浓硫酸、锌粒、稀硝酸、铜片、高锰酸钾、水
仪器(可重复使用):
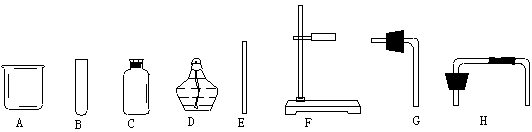
回答下列问题:
⑴写出有关仪器的名称A C D F
⑵若制取和收集氧气,写出选用上述药品的名称 ,需用仪器(填序号) 。
写出反应的化学方程式 。在盛放药品的试管口,应放置一团疏松棉花,原因是 。
⑶若制取和收集氢气,写出选用上述药品的名称 ,需用仪器(填序号) 。
37、手机中使用的锂电池电板是新型的高能电池,以质量轻、电容大而受到普遍重视。目前已制成多种功能的锂电池。某种锂电池的总反应可表示为Li+MnO2=LiMnO2。在上述反应中锂元素的化合价从0价转变为 价,锰元素的化合价从+4价转变为 _价。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com