
题目列表(包括答案和解析)
| 熔点/K | 沸点/K | 水中溶解度(标况) | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
| | 熔点/K | 沸点/K | 标准状况时在水中的溶解度 |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
(15分)
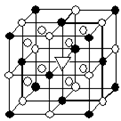
(1)如图所示为冰晶石(化学式为 Na3AlF6)的晶胞。图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种。图中●、○分别指代哪种粒子 、 ;大立方体的体心处▽所代表的是 (用化学式表示)。
Na3AlF6)的晶胞。图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种。图中●、○分别指代哪种粒子 、 ;大立方体的体心处▽所代表的是 (用化学式表示)。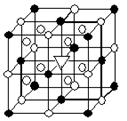
(2)H2S和H2O2的主要物理性质比较如下:
| | 熔点/K | 沸点/K | 标准状况时在水中的溶解度 |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
一 二、选择题
题号
1
2
3
4
5
6
7
8
答案
B
A
D
B
B
A
D
D
题号
9
10
11
12
13
14
答案
D
BD
CD
C
AD
AC
15.(1)防止暴沸 冷凝回流
(2)3.2
(3)温度过高发生副反应。
(4)除去产物中的丁醇。(每空2分)
16.(1)SO2
(1分) 
 (1分) (2)第四周期第Ⅷ族(2分)
(1分) (2)第四周期第Ⅷ族(2分)
(3)2Al+Fe2O3 Al2O3+2Fe (2分) 0.1 mol (1分)
Al2O3+2Fe (2分) 0.1 mol (1分)
(4) ③(1分)
(5) 3Fe2++NO3- +4H+ = 3Fe3++NO↑+2H2O(2分)
(6) Fe2O3+3KNO3+4KOH  2K2FeO4+3KNO2+2H2O(2分)
2K2FeO4+3KNO2+2H2O(2分)
17.(共8分)
(1)0.075mol/L?min(1分)
(2)放热, CO(g)+2H2(g) → CH3OH(g) +91KJ, 不能(各1分,共3分)
(3)K = ,减小;(各1分,共2分) (4)c(2分)
18.
(1)反应速率突然减小(或铁片表面生成的气泡突然减少)(2分)
(2)过滤(1分)
(3)b、d(2分),Fe和Cu(1分)
(4)抑制Fe2+、NH4+水解(2分)
(5)避免加热过程中晶体受热分解(或被氧化)(2分)
19.(每空2分)
(1) 氧化还原反应 (2)
氧化还原反应 (2)
(3)C10H12O4
(4)
20.(每空2分,共10分)
(1)2.8×105 ;18
(2)86.96%
(3) ;138
;138
21.A(1)●:AlF6- ○:Na+ AlF6- 电解炼铝的助熔剂(各1分)
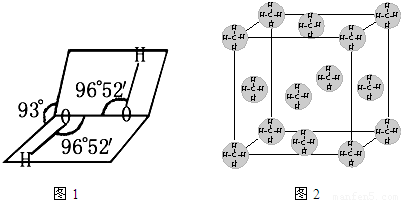
(2).H2O2分子间存在氢键(1分),与水分子可形成氢键(1分)。
(3)3d104s1(1分) Cr(1分) 共价键、配位键(2分)
降低Cu(NH3)4SO4?H2O的溶解度(2分)
B.(1) Fe + 2H+ → Fe2+ + H2↑;CuO + 2H+ → Cu2+ + H2O (各2分)
(2) ① (1分)
(3) ③ (1分)
(4) ①③ (2分)
(5) ②④① (2分)
(6)二; (1+3分)
(1+3分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com