
题目列表(包括答案和解析)


| ||
| ||
| 1 |
| 2 |
| 1 |
| 2 |
 某实验小组拟用50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:
某实验小组拟用50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:
对于反应:H-+NH3=H2+NH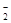 的说法正确的是
的说法正确的是
A.该反应属于置换反应
B.NH3是氧化剂
C.NH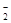 是还原产物
是还原产物
D.若反应中有1 mol电子转移,则必然生成22.4 L H2
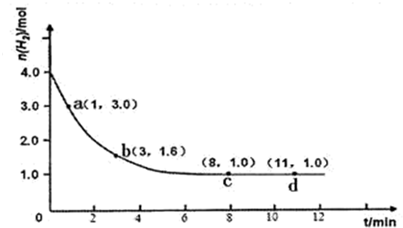
在容积为1L的密闭容器中,充入1 mol N2和4 mol H2,一定条件下反应N2+3H2 2NH3 达到平衡,此时N2和H2的物质的量之比恰好为 1:5。试回答下列问题:
(1)平衡时混合气体的压强与起始时混合气体的压强相比 (填“偏高”、“偏低”或“相等”)。
(2)该平衡混合气中NH3的体积分数是 。
(3)平衡时,H2的转化率为
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com