
题目列表(包括答案和解析)
(Ⅰ)下列实验操作或对实验事实的描述正确的是 (填序号);
① 实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉。
② 配制一定浓度的溶液时,俯视容量瓶的刻度线,会使配制的浓度偏高;实验室测定中和热时,过早读数会使测定结果偏低。
③ 将Fe2(SO4)3溶液加热蒸发至干并灼烧,最后得到红棕色粉末
④ 实验室用铜片与稀硝酸反应产生的气体可用排水法收集
⑤ 试管中加入少量淀粉,再加入一定量稀硫酸,加热3-4分钟,然后加入银氨溶液,片刻后管壁上有“银镜”出现
⑥ 向氨水中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液中滴加氨水现象相同
⑦ 苯与溴水在铁粉的催化作用下制备溴苯
⑧ 分别向体积和pH均相同的盐酸和醋酸中滴加等浓度的氢氧化钠溶液,完全中和时消耗的氢氧化钠溶液的体积一样多
Ⅱ.在中学化学实验中,通常用无水硫酸铜来检验少量水的存在。由于无水硫酸铜吸湿性很强,需要现制现用。
方法甲:取2药匙细小的硫酸铜晶体置于_______中研碎后放入坩埚,将坩埚放在______上用小火慢慢加热并用玻璃棒不停搅拌,最后将坩埚移入___________中进行冷却(请选用合适仪器填空:表面皿、研钵、烧杯、通风橱、试管夹、干燥器、泥三角)。
方法乙:取2药匙研碎的硫酸铜晶体于小烧杯中,加入20 mL浓硫酸(质量分数不低于98%),并用玻璃棒搅拌,静置5 min后倾去浓硫酸,用无水乙醇洗涤数次,倒在滤纸上晾干。
【交流与讨论】
(1)方法甲中,加热温度稍高时会出现变黑现象,原因是_________(用化学方程式表示)。
(2)方法乙中,浓硫酸的作用是__________;为了不浪费药品,对无水乙醇洗涤液进行再生的方法是______ ,所用的主要玻璃仪器有烧瓶、接液管、锥形瓶、酒精灯________________等。
(3)用制得的无水硫酸铜检验某双氧水中是否含水时,除了发现固体变蓝外,还发现该双氧水中有气泡产生,对此你有何猜想______________。
 (4)目前工业上正积极探索用浓HNO3作氧化剂,用Cu与浓H2SO4、浓HNO3反应,采取间歇加热、逐渐加入浓HNO3的方法来制备CuSO4•5H2O的新工艺。模拟制备装置如下图所示。
(4)目前工业上正积极探索用浓HNO3作氧化剂,用Cu与浓H2SO4、浓HNO3反应,采取间歇加热、逐渐加入浓HNO3的方法来制备CuSO4•5H2O的新工艺。模拟制备装置如下图所示。
【问题一】如图装置中,分液漏斗内装的液体是________,反应结束时,获取CuSO4•5H2O的操作过程是先________________,趁热将三颈瓶中的液体倒入烧杯中冷却,析出晶体CuSO4?5H2O ,过滤、晾干。
【问题二】工业上用石灰乳吸收尾气,除了防止环境污染外,还能得到了有经济实用价值的副产品―― 亚硝酸钙。尾气吸收生成亚硝酸钙的化学方程式是_______________。
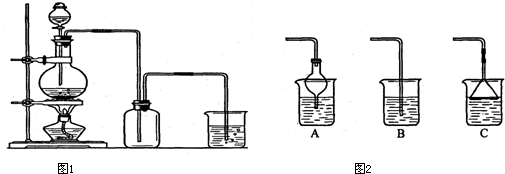
(1)实验室制取氯气也可用下图装置

①实验原理(写化学方程式):______________________________。
②收集原理:因Cl2溶于水,密度比空气大,故用向上排空气法;因Cl2在饱和食盐水中的溶解度小,故可用排饱和食盐水法收集。A、B为两个位置上的止水夹,采用向上排空气法和排饱和食盐水法收集Cl2时的正确操作是_________________________________________。
A.采用向上排空气法收集Cl2时应将A关闭,B打开
B.采用向上排空气法收集Cl2时应将B关闭,A打开
C.采用排饱和食盐水法收集Cl2时应将A关闭,B打开
D.采用排饱和食盐水法收集Cl2时应将B关闭,A打开
③尾气处理,氢氧化钠溶液的作用是处理尾气,防止氯气污染空气,该反应的离子方程式为:__________________________________________________________________。
(2)科学研究中可以用多种方法来测定阿伏加德罗常数。X射线衍射法就是其中的一种。X射线法是通过X射线衍射仪测出离子化合物离子间的间隔,再根据该化合物质量与体积的关系(密度)来确定。已知:X射线衍射仪测出的NaCl晶体中相邻钠离子与氯离子间距为a cm,NaCl相对分子质量为b。某同学为了测定阿伏加德罗常数,做了如下实验:用分析天平称取一定质量研细的NaCl固体,装入25 mL容量瓶中,然后用滴定管向容量瓶中滴加苯并不断振荡,使苯、氯化钠晶体充分混匀,标定,其实验结果如下表:
实验序号 | m NaCl/g | 消耗苯体积/cm3 | VNaCl | NA |
1 | 5.879 3 | 22.27 |
|
|
2 | 9.456 6 | 20.67 |
|
|
根据实验数据,请填写第一次实验中的空格(阿伏加德罗常数项只要求写出计算式,对原始数据不进行处理)。
如图中A、B、C是常见的化学实验装置,请回答下列问题:
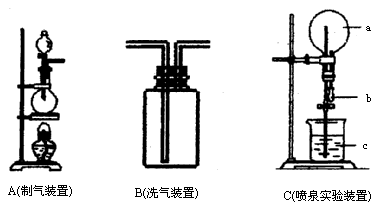
(1)利用A装置,当不加热时,可制取的一种气态单质是________;当加热时,可制取的一种化合物是________.
(2)化学实验室用A装置加热制取氯气,化学方程式为:
________.
为得到纯净、干燥的氯气,可让A中出来的气体在进入收集装置前依次通过分别装有________和________的两个洗气瓶B.
(3)实验室制取氯气和二氧化碳都可用瓶口向上排空集气法收集,具体操作有何不同?为什么?
________
(4)有一烧瓶纯净、干燥的氯气,用装置C做喷泉实验,如何操作才能形成喷泉?
________.
(本题共12分)
氯气和氯乙烯都是重要的化工产品,年产量均在107t左右。氯气的实验室制备和氯乙烯的工业生产都有多种不同方法。
完成下列填空:
(1)实验室制取纯净的氯气,除了二氧化锰、浓盐酸和浓硫酸,还需要_________、________(填写试剂或溶液名称)
(2)实验室用2.00mol/L的盐酸和漂粉精[成分为Ca(ClO)2、CaCl2]反应生成氯气、氯化钙和水,若产生2.24L(标准状况)氯气,发生反应的盐酸为_________m,l。
(3)实验室通常用向上排空气法收集氯气。设计一个简单实验,验证所收集的氯气中是否含有空气。
_________________
4)工业上用电石-乙炔法生产乙烯的反应如下:
CaO+3C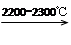 CaC2+CO
CaC2+CO
CaC2+2H2O→HC≡CH↑+Ca(OH)2
HC≡CH↑+HCl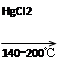 CH2=CHCl
CH2=CHCl
电石-乙炔法的优点是流程简单,产品纯度高,而且不依赖于石油资源。
电石-乙炔法的缺点是___________________、_____________________。
(5)乙烷和氯气反应可制得ClCH2CH2Cl,ClCH2CH2Cl加热分解得到氯乙烯和氯化氢。设计一种以乙烯和氯气为原料制取氯乙烯的方案(其他原料自选),用化学方程式表示(不必注明反应条件)。
要求:①反应产生的氯化氢必须用于氯乙烯的制备;②不再产生其他废液。
___________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com