
题目列表(包括答案和解析)
(注意:在试题卷上作答无效)现拟用下图所示装置(尾气处理部分略)来制取一氧化碳,并用以测定某铜粉样品(混有CuO粉末)中金属铜的含量。
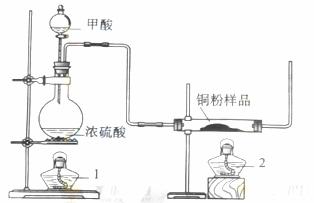
(1)制备一氧化碳的化学方程式是 ;
(2)试验中,观察到反应管中发生的现象时 ;
尾气的主要成分是 ;
(3)反应完成后,正确的操作顺序为 (填字母)
a.关闭漏斗开关 b.熄灭酒精1 c.熄灭酒精灯2
(4)若试验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,则原样品中单质铜的质量分数为 ;
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案;
①设计方案的主要步骤是(不必描述操作过程的细节) ;
②写出有关反应的化学方程式 。
(注意:在试题卷上作答无效)
化合物A(C11H8O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B和C。回答下列问题:
(1) B的分子式为C2H4O2,分子中只有一个官能团。则B的结构简式是________,B与乙醇在浓硫酸催化下加热反应生成D,该反应的化学方程式是________________________,该反应的类型是________;写出两种能发生银镜反应的B的同分异构体的结构简式________________________。
(2) C是芳香化合物,相对分子质量为180,其碳的质量分数为60.0%,氢的质量分数为4.4%,其余为氧,则C的分子式是________。
(3)已知C的芳环上有三个取代基,其中一个取代基无支链,且还有能使溴的四氯化碳溶液退色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则该取代基上的官能团名称是
。另外两个取代基相同,分别位于该取代基的邻位和对位,则C的结构简式是 。
(4)A的结构简式是 。
(注意:在试题卷上作答无效)
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,在将滤液按下图所示步骤进行操作。
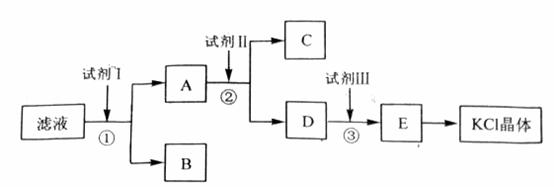
回答下列问题:
(1) 起始滤液的pH_____________7(填“大于”、“小于”或“等于”),其原因是_________________________________________________。
(2) 试剂I的化学式为______________________,①中发生反应的离子方程式为____________________________________________。
(3) 试剂Ⅱ的化学式为______________________,②中加入试剂Ⅱ的目的是__________________________________________________________________;
(4) 试剂Ⅲ的名称是______________________,③中发生反应的离子方程式为__________________________________________________________________;
(5) 某同学称取提纯的产品0.7759g,溶解后定定容在100mL容量瓶中,每次取25.00mL溶液,用0.1000mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62mL,该产品的纯度为____________________________________________。(列式并计算结果)
(注意:在试题卷上作答无效)原子序数依次增大的短周期元素a、b、c、d和e中,a的最外层电子数为其周期数的二倍;b和d的A2B型氢化物均为V形分子,c的+1价离子比e的-1价离子少8个电子。
回答下列问题:
(1) 元素a为________;c为_______
(2) 由这些元素形成的双原子分子为__________________。
(3) 由这些元素形成的三原子分子中,分子的空间结构属于直线形的是_______,非直线形的是_______________________。(写2种)
(4) 这些元素的单质或由他们形成的AB型化合物中,其晶体类型属于原子晶体的是_______,离子晶体的是_______,金属晶体的是_______,分子晶体的是_______;(每空填一种)
(5) 元素a和b形成的一种化合物与c和b形成的一种化合物发生的反应常用于防毒面具中,该反应的化学方程式为_______________________。
(09全国卷Ⅱ28)(15分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。

回答下列问题:
(1)A中加入的物质是_____________①_____________________________.
发生反应的化学方程式是_______________②_______________________;
(2)B中加入的物质是_____③________,其作用是_________④_______________:
(3)实验时在C中观察到得现象是_____________⑤_________________,
发生反应的化学方程式是_________________⑥____________________;
(4) 实验时在D中观察到得现象是________________⑦__________________,
D中收集到的物质是_______⑧_______,检验该物质的方法和现象是_________⑨_____________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com