
题目列表(包括答案和解析)
| 化合价 | -2 | -1 | 0 | +2 | +4 | +6 | +7 |
| 代表物的化学式 | Na2S等 Na2S等 |
FeS2 | S | Na2S2O3 | SO2等 SO2等 |
SO3或H2SO4或Na2SO4 | Na2S2O8 |

| 化合价 | -2 | -1 | 0 | +2 | +4 | +6 | +7 |
| 代表物的化学式 | ______ | FeS2 | S | Na2S2O3 | ______ | SO3或H2SO4或Na2SO4 | Na2S2O8 |
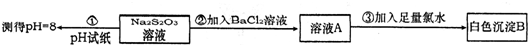
| 化合价 | -2 | -1 | 0 | +2 | +4 | +6 | +7 |
| 代表物的化学式 | FeS2 | S | Na2S2O3 | SO3或H2SO4或Na2SO4 | Na2S2O8 |
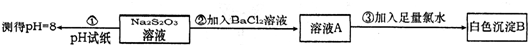
| 叙述1 | 叙述2 | |
| A | 明矾可用于净水 | 硫酸铁可用于净水 |
| B | 浓硝酸要密封并保存阴凉处 | 漂白粉要密封保存在阴凉处 |
| C | 少量与铁反应生成氯化亚铁 | 少量碘蒸汽与铁反应生成碘化亚铁 |
| D | 苯酚的水溶液显弱酸性 | 氯化铵溶液显弱酸性 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com