
题目列表(包括答案和解析)
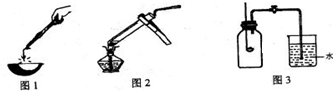
| 反应前镁带的质量 | 反应的固体产物的质量 | |
| 第一次 | 2.4046g | 3.8854g |
| 第二次 | 2.4024g | 3.8839g |
| 第三次 | 2.4063g | 3.8857g |
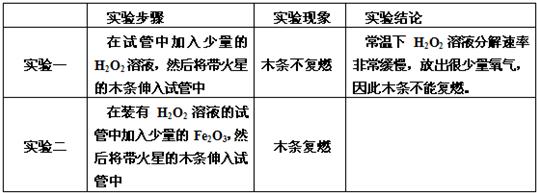

| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 在试管中加入少量的H2O2溶液,然后将带火星的木条伸入试管中 | 木条不复燃 | 常温下H2O2溶液分解速率非常缓慢,放出很少量氧气,因此木条不能复燃. |
| 实验二 | 在装有H2O2溶液的试管中加入少量的Fe2O3,然后将带火星的木条伸入试管中 | 木条复燃 | 加入能加快过氧化氢溶液分解的速率,所以可作过氧化氢溶液分解反应的催化剂. 加入能加快过氧化氢溶液分解的速率,所以可作过氧化氢溶液分解反应的催化剂. |
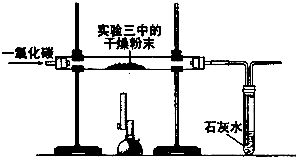

| 反应前镁带的质量 | 反应的固体产物的质量 | |
| 第一次 | 2.4046g | 3.8854g |
| 第二次 | 2.4024g | 3.8839g |
| 第三次 | 2.4063g | 3.8857g |
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 在试管中加入少量的H2O2溶液,然后将带火星的木条伸入试管中 | 木条不复燃 | 常温下H2O2溶液分解速率非常缓慢,放出很少量氧气,因此木条不能复燃. |
| 实验二 | 在装有H2O2溶液的试管中加入少量的Fe2O3,然后将带火星的木条伸入试管中 | 木条复燃 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com