
题目列表(包括答案和解析)

| ||
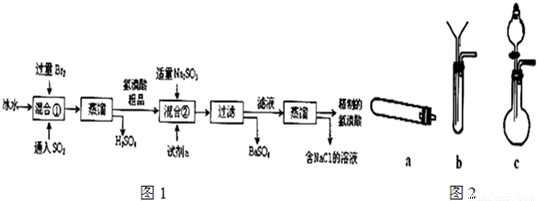
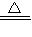 2NaHSO4+MnSO4+Br2↑+2H2O 制取Br2最好选用下列装置中的______ (填写字母,固定和加热装置均已省略).简述检验图2装置气密性的方法______.
2NaHSO4+MnSO4+Br2↑+2H2O 制取Br2最好选用下列装置中的______ (填写字母,固定和加热装置均已省略).简述检验图2装置气密性的方法______.
 2NaHSO4+MnSO4+Br2↑+2H2O 制取Br2最好选用下列装置中的______ (填写字母,固定和加热装置均已省略).简述检验图2装置气密性的方法______.
2NaHSO4+MnSO4+Br2↑+2H2O 制取Br2最好选用下列装置中的______ (填写字母,固定和加热装置均已省略).简述检验图2装置气密性的方法______.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com