
小璐和小磊合作测定盐酸、硫酸组成的混合酸中溶质的质量分数,设计进行了如下两个探究实验:
[实验1]取20g该混合酸并分成4等份,分别加入一定量未知质量分数的BaCl
2溶液,记录如下:
|
第1份 |
第2份 |
第3份 |
第4份 |
| 加入BaCl2溶液的质量/g |
15 |
20 |
25 |
30 |
| 反应得到的沉淀的质量/g |
1.398 |
1.864 |
2.330 |
2.330 |
[实验2]将实验1中的第4份反应液过滤,再向滤液中逐滴加入10%的NaOH溶液,通过pH测定仪打印出加入NaOH溶液的质量与烧杯中溶液pH的关系如图:
[数据处理]
小璐依据[实验1]沉淀的质量计算出混合酸中H
2SO
4的质量分数.
小磊依据[实验2]求混合酸中HCl的质量分数,过程如下:
解:设混合酸中HCl的质量分数为ω.
HCl+NaOH=NaCl+H
2O
36.5 40
×ω 10g×10%
解得:ω=0.1825=18.25%
现请你参与探究并完成相关问题.
(1)[实验1]中发生反应的化学方程式为
BaCl2+H2SO4=2HCl+BaSO4↓.
BaCl2+H2SO4=2HCl+BaSO4↓.
.
(2)根据小璐的计算,测出原混合酸中H
2SO
4的质量分数为多少?(保留三位有效数字).
[反思交流]小磊计算出混合酸中HCl的质量分数会
偏高
偏高
(填“偏高”、“偏低”或“无影响”),理由是
因为BaCl2与H2SO4反应后有盐酸生成,从而使滤液中的盐酸的质量增大.
因为BaCl2与H2SO4反应后有盐酸生成,从而使滤液中的盐酸的质量增大.
(如“无影响”,本空不作答).

 小璐和小磊合作测定盐酸、硫酸组成的混合酸中溶质的质量分数,设计进行了如下两个探究实验:
小璐和小磊合作测定盐酸、硫酸组成的混合酸中溶质的质量分数,设计进行了如下两个探究实验: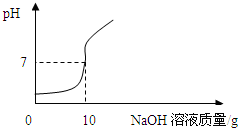




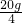 ×ω 10g×10%
×ω 10g×10%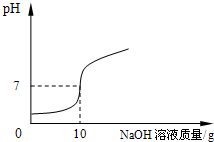 小璐和小磊合作测定盐酸、硫酸组成的混合酸中溶质的质量分数,设计进行了如下两个探究实验:
小璐和小磊合作测定盐酸、硫酸组成的混合酸中溶质的质量分数,设计进行了如下两个探究实验: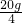 ×ω 10g×10%
×ω 10g×10%