
题目列表(包括答案和解析)
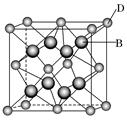
有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对电子,F原子核外电子数是B 与C核外电子数之和,D 是主族元素且与E同周期,E能形成红色或砖红色E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示。请回答下列问题:
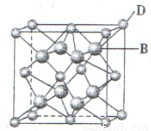
(1)E+离子基态时的电子排布式为_______________
(2)A2F的分子空间构型为_____________,FO3分子中F原子的杂化方式 ______________
(3)CA3极易溶于水,其原因主要是______________
(4)从图中可以看出,D 与B形成的离子化合物的化
学式为______________(用元素符号表示),该离子晶体的
密度为ag·cm-3,则晶胞的体积是____________(写出表达式即可,不用化简)
(5)已知E单质的晶体为面心立方最密堆积 (在晶胞的顶点和面心均含有一个E原子),则 E的晶体中E原子的配位数为
有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示.请回答下列问题.
(1)E元素原子基态时的电子排布式为________.
(2)A2F分子中F原子的杂化类型是________,F的氧化物FO3分子空间构型为________.
(3)CA3极易溶于水,试判断CA3溶于水后,形成CA3·H2O的合理结构:________(填字母代号),推理依据是_________________________.

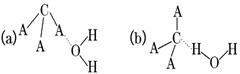
(4)从图中可以看出,D跟B形成的离子化合物;该离子化合物晶体的密度为a g·cm-3,则晶胞的体积是______________________(写出表达式即可).
 有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大 的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E20和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如右图所示.请回答下列问题.
有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大 的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E20和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如右图所示.请回答下列问题.
(1)E元素原子基态时的电子排布式为 .
(2)A2F分子中F原子的杂化类型是
(3)CA3极易溶于水,其原因主要是 ,
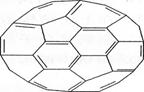
 (4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如右图,分子中碳原子轨道的杂化类型为 ;1 molC60分子中σ键的数目为 .
(4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如右图,分子中碳原子轨道的杂化类型为 ;1 molC60分子中σ键的数目为 .
(5)多元化合物薄膜太阳能电池材料为无机盐,其主要包括
砷化镓、硫化镉、硫化锌及铜铟硒薄膜电池等.
①第一电离能:As Se(填“>”“<”或“=”).
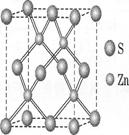
②硫化锌的晶胞中(结构如下图所示),硫离子的配位数
是 与S距离最近且等距离的S之间的距离为
(密度为ρg/cm3)
③二氧化硒分子的空间构型为 .

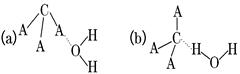
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com