在体积为1L的两个恒容密闭容器中,分别充入1molCO和1molH
2O(g)的混合气体,进行如下化学反应:CO(g)+H
2O(g)?CO
2(g)+H
2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
| 0min | 10min | 20min | 30min | 40min | 50min |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
(1)1100℃时,前10min该反应的化学反应速率v(CO
2)=______,830℃平衡后CO转化率的为______.
(2)1100℃时化学平衡常数K=______,该反应为______反应(填“吸热”和“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是______.
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v
逆(H
2)=v
正(H
2O) (d)c(CO
2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH
2O(g),平衡______
______移动(选填“向正反应方向”或“向逆反应方向”或“不”),再达到平衡时,H
2百分含量______(选填“增大”或“减小”或“不变”).
(5)830℃时,若在体积为2L的密闭容器中充入1molCO
2和1molH
2的混合气体,60min时反应达平衡状态,画出c(CO)和c(H
2)随时间变化而变化的趋势图.


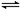 CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题: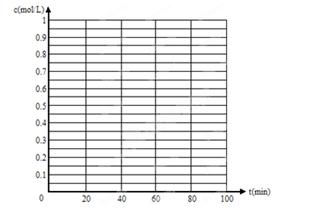

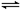 CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题: