
题目列表(包括答案和解析)

| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量悬浊液,过滤,充分 洗涤后,取滤渣于试管中, 加入过量2mol/L的盐酸溶液,充分振荡,再滴加几滴0.1mol/L氯化钡溶液 加入过量2mol/L的盐酸溶液,充分振荡,再滴加几滴0.1mol/L氯化钡溶液 |
说明悬浊液中混 有白色沉淀生成 有白色沉淀生成 ,有Cu4( 0H)6S04. |
| 步骤2:另取少量悬浊液于试管中, 将试管放入装有沸水的小烧杯中水浴加热一段时间取出试管观察 将试管放入装有沸水的小烧杯中水浴加热一段时间取出试管观察 |
试管中有黑色固体生成 试管中有黑色固体生成 ,说明悬浊液中混有Cu( 0H) 2. |
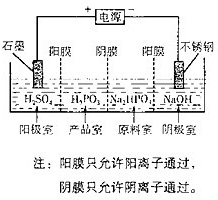 (2013?广州一模)亚憐酸(H3PO3)是二元酸,与足量NaOH溶液反应生成Na2HPO3.
(2013?广州一模)亚憐酸(H3PO3)是二元酸,与足量NaOH溶液反应生成Na2HPO3.
| ||
| ||
| ||
| ||
- 2 |

| △ |
| △ |
 (任写一种)
(任写一种) (任写一种)
(任写一种) 也可与III发生类似反应③的反应生成有机物V.V的结构简式是
也可与III发生类似反应③的反应生成有机物V.V的结构简式是

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com