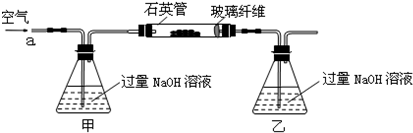
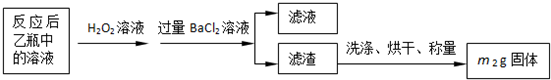
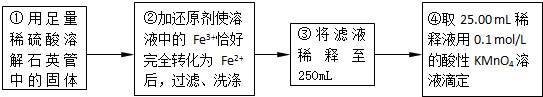
(2011?延庆县一模)硫酸亚铁晶体(FeSO
4?7H
2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量.实验步骤如下:
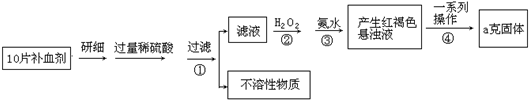
请回答下列问题:
(1)证明步骤①滤液中含有Fe
2+的方法是
取少量滤液加入试管中,先滴加KSCN溶液,溶液不变色,再滴加氯水(或双氧水、稀硝酸),溶液变为血红色
取少量滤液加入试管中,先滴加KSCN溶液,溶液不变色,再滴加氯水(或双氧水、稀硝酸),溶液变为血红色
.
(2)写出②中的离子反应方程式:
2Fe2++H2O2+2H+═2Fe3++2H2O
2Fe2++H2O2+2H+═2Fe3++2H2O
.
(3)步骤③中反应的离子方程式:
Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
.
(4)步骤④中一系列处理的操作步骤:过滤、
洗涤
洗涤
、灼烧、冷却、称量.
(5)该小组有些同学认为用KMnO
4溶液滴定也能进行铁元素含量的测定.(5Fe
2++MnO
4-+8H
+→5Fe
3++Mn
2++4H
2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO
4溶液250mL,配制时需要的仪器除药匙、天平(附砝码)、玻棒、烧杯、胶头滴管外,还需
250mL容量瓶
250mL容量瓶
.
②滴定到终点时的颜色为
紫
紫
色.
(6)正常人每天应补充16.8mg左右的铁.其中绝大部分来自于食物.如果全部通过服用含FeSO
4?7H
2O的片剂.来补充铁,则正常人每天服需用含
83.4
83.4
mgFeSO
4?7H
2O片剂.