2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的.因此锂离子电池回收具有重要意义,其中需要重点回收的是正极材料,其主要成分为钴酸锂(LiCoO
2)、导电乙炔黑(一种炭黑)、铝箔以及有机粘接剂.某回收工艺流程如下:
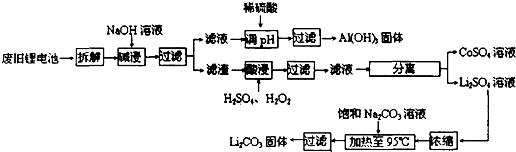
(1)上述工艺回收到的产物有
Al(OH)3.CoSO4.Li2CO3
Al(OH)3.CoSO4.Li2CO3
(2)Li原子的最外层电子数是
1
1
,废旧电池可能由于放电不完全而残留有原子态的锂,为了安全对拆解环境的要求是
隔绝空气和水分
隔绝空气和水分
(3)碱浸时主要反应的化学方程式为
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
.
(4)最后一步过滤应趁热过滤,原因是
防止析出硫酸钠晶体
防止析出硫酸钠晶体
.

