
题目列表(包括答案和解析)
 (2013?重庆一模)(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
(2013?重庆一模)(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:| 实验组 | 温度 ℃ |
起始量/mol | 平衡量/mol | 达到平衡所需时间/min[ | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
 (2013?珠海一模)(1)将不同量的CO(g)和H2O(g)分别通入体积2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如下两组数据:
(2013?珠海一模)(1)将不同量的CO(g)和H2O(g)分别通入体积2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如下两组数据:| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
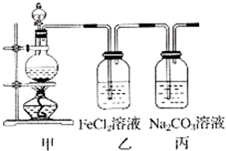 (2013?滨州一模)(1)某学习小组利用下图装置制取氯气并探究其性质.
(2013?滨州一模)(1)某学习小组利用下图装置制取氯气并探究其性质.
| ||
| ||
| 实验步骤 | 预期现象和结论 | |
| ① | 用A试管取少量澄清石灰水备用,用B试管取少量样品,再向B试管 加入适量1mol/L的盐酸,塞上带导管的单孔塞,将导管的另一端插入A试管中 加入适量1mol/L的盐酸,塞上带导管的单孔塞,将导管的另一端插入A试管中 |
若无气体放出且澄清石灰水未见浑浊,则假设一成立; 若有气泡冒出,且澄清石灰水变浑浊则假设一步成立,假设二、三成立 若有气泡冒出,且澄清石灰水变浑浊则假设一步成立,假设二、三成立 |
| ② | 用胶头滴管向上述步骤后的B试管中滴入几滴品红试液,振荡 用胶头滴管向上述步骤后的B试管中滴入几滴品红试液,振荡 |
若品红溶液不褪色,则假设二成立,若品红溶液褪色,则假设三成立 若品红溶液不褪色,则假设二成立,若品红溶液褪色,则假设三成立 |
| ||
| ||
| 时间/min浓度(mol/L) | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0?30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com