
题目列表(包括答案和解析)
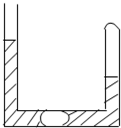 (2013?浦东新区三模)如图一段封闭的U形管,封闭的一端有一段CH4和Cl2的混合气体,在水平部分有一段气柱,其他两段为液体,已知液体与气体不反应,使CH4和Cl2在一定的光照下缓慢反应,则中间气柱的位置和长度的变化情况是(假定中间气柱未移出U形管的水平部分)( )
(2013?浦东新区三模)如图一段封闭的U形管,封闭的一端有一段CH4和Cl2的混合气体,在水平部分有一段气柱,其他两段为液体,已知液体与气体不反应,使CH4和Cl2在一定的光照下缓慢反应,则中间气柱的位置和长度的变化情况是(假定中间气柱未移出U形管的水平部分)( )| NaCl | NaHCO3 | NH4Cl | |
| 10℃ | 35.8 | 8.15 | 33.0 |
| 45℃ | 37.0 | 14.0 | 50.0 |
| b∕a的取值范围 | 溶质 | 溶质物质的量 | ||||
0<b∕a<5∕4 0<b∕a<5∕4 |
NH3 NH3 |
(a-4b∕5)mol (a-4b∕5)mol | ||||
|
-- | -- | ||||
5∕4<b∕a<2 5∕4<b∕a<2 |
HNO3 HNO3 |
(4b-5a)∕3mol (4b-5a)∕3mol | ||||
b∕a≥2 b∕a≥2 |
HNO3 HNO3 |
amol amol |


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com