(2011?大兴区二模)某学生设计下列实验来制取、检验HCl气体溶水性及证明酸性:盐酸>碳酸>苯酚

(1)装置III的实验目的是
证明酸性:盐酸>碳酸>苯酚
证明酸性:盐酸>碳酸>苯酚
.
(2)装置I倒置漏斗的作用是
防止倒吸
防止倒吸
.
(3)如何检验装置II的气密性
将导管下端插入水中,用手捂住烧瓶,看是否有气泡冒出或在水面下的导管内是否形成一段稳定的空气柱
将导管下端插入水中,用手捂住烧瓶,看是否有气泡冒出或在水面下的导管内是否形成一段稳定的空气柱
.“喷泉”实验的操作方法是
打开止水夹挤出胶头滴管中的水
打开止水夹挤出胶头滴管中的水
.
(4)装置III要达到实验目的有设计上的不足,请设计出改进方案
从E装置中导出的气体先通入饱和的碳酸氢钠溶液中,再将从饱和碳酸氢钠溶液中出来的气体通入苯酚钠溶液
从E装置中导出的气体先通入饱和的碳酸氢钠溶液中,再将从饱和碳酸氢钠溶液中出来的气体通入苯酚钠溶液
.
(5)写出F中反应的离子方程式

+CO
2+H
2O→
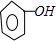
+NaHCO
3;

+CO
2+H
2O→

+NaHCO
3;
,F装置的溶液中电荷守恒的离子浓度关系式
C(HCO3-)+2C(CO32- )+C(OH-)+C(C6H5O-)=C(Na+)+C(H+).
C(HCO3-)+2C(CO32- )+C(OH-)+C(C6H5O-)=C(Na+)+C(H+).
.


 ,则苯氯乙酮不可能具有的化学性质是
,则苯氯乙酮不可能具有的化学性质是







 (2011?大兴区二模)短周期元素A、B、C、D、E、F、G其核外电子总数依次增多,A原子是元素中电子总数最少的,B的最外层电子数是次外层电子数的二倍,C最外层电子数是其电子层数的三倍,G与C同族且两元素核外电子总数之和与D、E两元素核外电子总数之和相等,F的最外电子数是次外层电子数的二分之一.
(2011?大兴区二模)短周期元素A、B、C、D、E、F、G其核外电子总数依次增多,A原子是元素中电子总数最少的,B的最外层电子数是次外层电子数的二倍,C最外层电子数是其电子层数的三倍,G与C同族且两元素核外电子总数之和与D、E两元素核外电子总数之和相等,F的最外电子数是次外层电子数的二分之一.


 +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3; +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3;

